JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
제한된 침구와 둥지는 생쥐의 초기 삶의 역경에 대한 모델입니다.
요약
이 프로토콜은 출생 후 초기에 빈곤한 환경과 예측할 수 없는 산모의 보살핌으로 인한 초기 삶의 역경이 뇌 발달과 정신 장애의 미래 위험에 어떻게 영향을 미치는지 연구하기 위한 동물 모델을 설명합니다.
초록
학대, 방치, 자원 부족, 예측할 수 없는 가정 환경과 같은 초기 삶의 역경(ELA)은 우울증과 같은 신경 정신 질환 발병의 위험 요인으로 알려져 있습니다. ELA에 대한 동물 모델은 만성 스트레스가 뇌 발달에 미치는 영향을 연구하는 데 사용되어 왔으며, 일반적으로 인간을 포함한 포유류의 초기 생활 경험의 주요 원인이기 때문에 모성 관리의 품질 및/또는 양을 조작하는 데 의존합니다. 여기에서는 마우스에 LBN(Limited Bedding and Nesting) 모델을 사용하기 위한 자세한 프로토콜이 제공됩니다. 이 모델은 새끼를 위한 둥지를 짓기 위해 댐에 제공되는 둥지 재료의 양을 제한하고 케이지의 메쉬 플랫폼을 통해 쥐를 침대에서 분리함으로써 중요한 발달 기간(출생 후 2-9일) 동안 단편적이고 예측할 수 없는 모성 관리 패턴을 유발하는 자원이 부족한 환경을 모방합니다. LBN 모델로 인한 모성 행동의 변화, 강아지 체중 감소 및 기저 코르티코스테론 수치의 장기적 변화를 설명하기 위해 대표 데이터가 제공됩니다. 성인이 되었을 때 LBN 환경에서 자란 자손은 비정상적인 스트레스 반응, 인지 결핍 및 무쾌감증과 같은 행동을 보이는 것으로 나타났습니다. 따라서 이 모델은 스트레스에 민감한 뇌 회로의 성숙이 ELA에 의해 어떻게 변화되고 정신 장애에 취약성을 부여하는 장기적인 행동 변화를 초래하는지 정의하는 중요한 도구입니다.
서문
출생 후 초기는 환경적 영향이 발달 궤도를 바꿀 수 있는 중요한 발달 시기입니다. 예를 들어, 어린 시절의 역경(ELA)은 뇌 발달을 변화시켜 인지 및 정서적 기능의 장기적인 변화를 유발할 수 있습니다. ELA의 예로는 신체적 또는 정서적 학대, 방치, 부적절한 자원, 아동기 또는 청소년기에 발생하는 예측할 수 없는 가정 환경등이 있다 1. ELA는 우울증, 약물 사용 장애, 외상 후 스트레스 장애(PTSD) 및 불안과 같은 장애를 발병시키는 위험 요인으로 알려져 있습니다 2,3,4,5. 이는 미국의 아동 빈곤 수준이 2021년 5.2%에서 2022년 12.4%로 최근 두 배 이상 증가했다는 점을 감안할 때 중요합니다6, 빈곤 자체가 반드시 ELA는 아니지만 다양한 유형의 ELA의 가능성을 증가시킵니다7.
동물 모델은 어린 시절의 스트레스가 뇌 발달과 성인의 결과에 미치는 영향을 이해하는 데 오랫동안 필수적이었습니다. 최근 몇 년 동안 이 현상을 해부하기 위해 사용된 두 가지 주요 동물 모델은 모성 분리(MS)와 제한된 침구 및 둥지 재료(LBN)로 인한 빈곤한 환경입니다. 다발성경화증은 부모의 결핍의 모델로 개발되었다8. 그 안에서 설치류 댐은 젖을 뗄 때까지 매일 몇 시간 동안 새끼로부터 빼앗깁니다8. 다발성경화증 패러다임은 성인기에 우울증 및 불안과 유사한 행동을 유발하는 것으로 밝혀졌습니다.9 뿐만 아니라 만성 스트레스에 대한 비정상적인 반응을 보입니다10,11. 반면에, 바람 실험실(12)에서 처음 개발된 LBN 모델은 댐과 새끼를 분리하는 것이 아니라, 오히려 새끼가 사육되는 환경을 수정하여 자원이 적은 환경(12,13)을 모방한다. 이 모델에서는 둥지 재료의 양을 줄이고 침구에 직접 접근하는 것을 방지하면 댐으로 인한 모성 보호가 중단된다3. 인지 및 정서적 뇌 회로의 적절한 발달을 위해서는 견고하고 예측 가능한 모성 관리가 필요하기 때문에14, LBN의 단편적인 모성 관리는 과잉 활동성 시상하부-뇌하수체-부신(HPA) 축, 여러 뇌 영역에서의 흥분-억제 균형 변화, 부신피질자극호르몬 방출 호르몬(CRH) 수치 증가, 자손의 우울과 유사한 행동 등 다양한 결과를 초래할 수 있다13, 15,16,17,18,19.
ELA가 신경 정신 장애의 위험을 증가시키는 정확한 메커니즘은 완전히 이해되지 않았습니다. 이는 HPA 축 회로(19,20)의 변화와 관련이 있는 것으로 생각되며, 최근의 증거는 이것이 미세아교세포 시냅스 가지치기(19)의 변화에 의해 야기될 수 있음을 보여준다. LBN 모델은 주산기 환경이 뇌 발달과 장기적인 행동 결과에 미치는 영향을 이해하는 데 중요한 도구인 것으로 나타났습니다. 이 모델은 처음에는 랫트를 위해 개발되었지만, 기존의 형질전환 도구(12,13)를 활용하기 위해 마우스에도 적용되었다. 주목할 만한 점은, 이 모델은 두 종 모두에서 매우 유사하며, HPA 축의 변화, 인지 결핍 및 우울증과 같은 행동과 같은 매우 수렴적인 결과를 유발하여 종 간 유용성과 번역 잠재력을 강조합니다. 이 기사에서는 마우스에서 제한된 침구 및 둥지 모델을 사용하는 방법에 대한 자세한 설명을 제공하고, 모델의 효능과 예상 결과를 검증하기 위해 모성 행동 및 자손 결과를 수집 및 분석합니다.
프로토콜
동물과 관련된 모든 절차는 미국 국립보건원(National Institutes of Health)의 실험동물 관리 및 사용 가이드(National Institutes of Health Guide for the Care and Use of Laboratory Animals)에 따라 수행되었으며, 조지아 주립 대학의 기관 동물 관리 및 사용 위원회(Institutional Animal Care and Use Committee)의 승인을 받았습니다(승인 번호 A24011). 생쥐는 조지아 주립 대학의 동물 시설에서 사육되고 관리되었습니다. 실험은 주산기(출생 후 일[P] 2-10) 동안 C57BL/6J 균주에 대해 수행되었으며 남성과 여성을 포함했습니다. 이 연구에 사용된 시약 및 장비는 재료 표에 나열되어 있습니다.
1. 재료 설정
- 케이지의 치수에 따라 메쉬 디바이더를 자르고 긴 쪽에 3cm를 초과하여 남겨 둡니다.
알림: 재료 표에 제공된 메쉬는 제조업체에서 절단한 것입니다. - 초과분을 포함하여 가장자리를 케이지 가장자리에 정확하게 맞고 바닥에서 ~2.5cm 높이로 플랫폼을 만드는 방식으로 접습니다. 이렇게 하면 소변과 대변이 그물망 칸막이를 통과할 수 있으며 동물은 옥수수 속대 침구를 회수할 수 없습니다. 마지막으로, 동물에게 해를 끼치 지 않도록 모든 날카로운 모서리가 접혀 있는지 확인하십시오.
알림: 메쉬 디바이더는 재사용이 가능하며 사용 사이에 뜨거운 물과 비누로 철저히 청소한 다음 70% 에탄올을 뿌려야 합니다. - 삼각대에 카메라를 설치하고 녹화 시스템을 준비합니다.
참고: 비디오 관리 소프트웨어를 사용하는 것이 좋습니다. 이러한 녹화로 인해 .mp4 파일이 자동으로 1시간 세그먼트로 비닝됩니다. - 연속 녹화로 설정을 조정합니다.
참고: 추가 권장 설정은 1920 x 1080 해상도 및 30프레임/초입니다. - 영상 관리 소프트웨어에 의해 자동으로 수행되지 않는 경우 결과 .mp4 파일을 1시간 세그먼트로 나누도록 설정합니다.
- 소등 기간을 분석하는 경우 적외선을 사용하십시오.
참고: 케이지 측면의 녹화 눈부심을 줄이려면 카메라에서 적외선(IR)을 비활성화하는 것이 좋습니다. 대신, 어두운 위상 녹화 중에 방에서 IR 투광 조명을 사용하십시오.
2. LBN(Limited bedding and nesting) 패러다임
- 1-4 마리의 암컷을 단일 주택 수컷 사육자와 쌍을 이룹니다.
참고: 실험용 암컷의 첫 번째 짝짓기에 권장되는 연령은 P75입니다. nulliparous 암컷을 사용하는 것이 이상적이지만, 이것이 가능하지 않은 상황에서, 예를 들어 귀중한 형질전환 마우스 라인과 같은 상황에서는 다수의 암컷이 그 후 약 4개월 동안 번식을 계속할 수 있습니다. 필수는 아니지만 짝짓기 날(배아일[E]0)을 확인하기 위해 매일 질 마개를 확인하는 것이 좋습니다.- 댐이 임신하면 교란을 최소화하십시오.
참고: 다태 암컷은 일반적으로 생식력이 감소하기 전에 최대 5마리의 새끼를 낳기 위해 재사용할 수 있습니다. 댐이 실험에 재사용되는 경우, 댐에 대한 LBN의 장기적 잔여 영향을 피하기 위해 매번 동일한 조건으로 우선적으로 사용하거나 Control에서 LBN으로 전환해야 하지만 그 반대의 경우는 안 됩니다.
- 댐이 임신하면 교란을 최소화하십시오.
- E17에서(또는 플러그를 확인하지 않은 경우 암컷이 분명히 임신한 것처럼 보일 때마다) 암컷을 자체 표준 플렉시글라스 케이지에 분리하고 둥지를 짓기 위해 솜 둥지(5 x 5cm) 하나를 줍니다.
참고: 분리된 암컷을 주 군락실에서 멀리 떨어진 조용하고 작은 방으로 옮기는 것이 가장 좋으며, 12시간의 빛/어둠 주기가 있고 통제 및 LBN 설정을 위한 직원의 방해를 최소화합니다. - 생년월일(E19 경)을 기록합니다.
- P2에서 새끼를 세고 성별을 계산합니다. LBN 또는 제어 조건(댐의 첫 번째 깔짚인 경우)에 깔짚을 무작위로 할당합니다. 새끼와의 이러한 상호 작용은 조명이 켜진 후 1시간에서 4시간 사이에 완료되어야 합니다.
- 새끼를 새롭고 깨끗한 케이지에 조심스럽게 넣어 성별에 따라 분류합니다. 항문과 생식기 사이의 항문 생식기 거리는 여성보다 남성에서 더 크며 식별자로 사용할 수 있습니다.
- 수컷과 암컷을 그룹으로 분리하여 수를 세십시오.
- 8마리 이상의 새끼는 도태시키고 4마리 미만의 새끼는 버립니다. 최적의 새끼 크기는 4-8마리의 새끼이며, 이 범위를 벗어난 것은 연구 기간 동안 모성 보살핌의 분배를 방해할 수 있습니다.
참고: 새끼 크기로 인해 영향을 받을 수 있는 변수는 새끼 무게, 먹이를 먹는 기회, 어미-새끼 상호 작용이며, 이는 실험을 혼란스럽게 할 수 있습니다. 이상적으로, 생쥐는 쥐보다 생존 가능성이 적기 때문에 교차 육성되지 않습니다.
- 그림 1과 같이 Control 및 LBN 조건을 설정합니다.
- 제어: 표준 크기의 마우스 신발 상자 케이지(19.4cm x 13.0cm x 38.1cm)와 ~220g의 옥수수 속대 침구(케이지 크기에 따라 ~1cm 높이를 목표로 함) 및 표준 정사각형 면 둥지(5 x 5cm)를 사용합니다.
- 쥐가 이 낯선 환경에 적응할 수 있도록 하려면 이전 케이지의 배설물 펠릿 중 하나를 새 케이지의 각 모서리에 놓습니다. 또한 이전 케이지에서 사용한 면화 둥지를 소량(동전 크기)으로 새 둥지 위에 놓습니다.
- LBN: 이전에 준비한 메쉬 디바이더를 ~110g의 옥수수 속대 침구(~0.5cm 높이 목표)가 있는 표준 신발 상자 케이지에 넣습니다. 메쉬는 쥐와 옥수수 속대 침구 사이의 직접적인 접촉을 방지해야 합니다.
- 마지막으로 면화 네슬릿 사각형(2.5 x 5cm)의 절반을 추가합니다. 적응에 도움이 되도록 위의 모든 단계를 반복하십시오.
알림: 이 설정이 조용하고 LBN 케이지21에서 자란 새끼에게 저체온증을 유발하지 않는 것으로 나타났기 때문에 환기가 되지 않는 표준 랙에 신발 상자 케이지를 유지하는 것이 좋습니다. 그러나 이것은 환기가 잘되는 케이지에서 증가된 공기 흐름의 경우가 아닐 수 있습니다. 따라서 연구원은 환기가 잘되는 케이지를 사용하는 경우 시스템에서 소음 수준과 강아지 코어 온도를 측정해야 합니다.
- 마지막으로 면화 네슬릿 사각형(2.5 x 5cm)의 절반을 추가합니다. 적응에 도움이 되도록 위의 모든 단계를 반복하십시오.
- 제어: 표준 크기의 마우스 신발 상자 케이지(19.4cm x 13.0cm x 38.1cm)와 ~220g의 옥수수 속대 침구(케이지 크기에 따라 ~1cm 높이를 목표로 함) 및 표준 정사각형 면 둥지(5 x 5cm)를 사용합니다.
- 새끼를 지정된 새장에 넣고 둥지 위에 놓습니다. 다음으로, 새끼를 향하게 하는 케이지에 댐을 놓으면 새끼가 더 빨리 존재한다는 것을 알아차릴 수 있습니다. P8에서 실험이 끝날 때까지 케이지를 방해하지 않도록 최소 10일 동안 충분한 음식과 물이 포함되어 있는지 확인하십시오.
- 케이지 앞의 삼각대에 카메라를 놓으면 댐과 새끼를 선명하게 볼 수 있습니다. 선택적으로 모든 각도를 더 잘 포착할 수 있도록 케이지 주변에 거울을 배치합니다. 하루에 1시간 분량의 비디오 녹화만 분석하면 되지만, 실험 중에는 24/7 연중무휴로 연속으로 녹화하도록 카메라를 설정하여 교란을 모니터링할 수 있습니다.
참고: 생쥐를 직접 관찰할 수도 있으며, 모성의 행동을 손으로 점수를 매길 수 있지만, 실험자가 방에 있기 때문에 발생하는 혼란을 방지하기 위해 비디오 녹화가 더 좋습니다. 환기 랙을 사용하는 경우 여기에 설명된 것과 다른 절차를 사용하여 산모 관리 녹화를 위한 카메라를 배치해야 할 수도 있습니다. - P10 아침에 모든 동물을 표준 케이지 조건(이상적으로는 위의 대조 조건과 동일)으로 되돌리고 새끼의 무게를 잰다.
- 모든 새끼를 동일하게 취급하고 P21에서 젖을 떼고 2-5명의 동성 새끼 그룹으로 나뉩니다.
참고: 가능하면 동성 새끼를 함께 수용하는 것을 목표로 하되, 필요한 경우 동일한 조건에 있는 다른 새끼에서 태어난 동성 자손을 함께 수용하십시오. 하우징 컨트롤과 LBN 자손을 함께 피하는 것이 권장됩니다(행동표현형에 대한 케이지메이트 구성의 효과에 대해서는 Yang et al. 참조).

그림 1: 케이지 설정의 예. 이미지 왼쪽의 케이지는 전체 양의 침구와 전체 둥지가 포함된 표준 제어(CTL) 케이지를 보여줍니다. 오른쪽의 케이지는 침구 양의 절반, 둥지 절반, 침구에서 동물을 분리하기 위한 메쉬 칸막이로 구성된 제한된 침구 및 둥지(LBN) 설정을 보여줍니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
3. 모성 행동 점수 매기기
- 이 설정에서는 연속 기록이 수집되지만 P3에서 P6까지 1시간만 분석합니다. 조명이 바뀐 후 1시간 이내에 녹화된 비디오를 분석하여 습관화할 수 있도록 하고 매일 일관된 시간의 비디오를 분석하는 것이 좋습니다.
참고: P3에서 P6까지의 기간은 일반적으로 LBN으로 인해 산모 관리에서 가장 큰 차이를 포함합니다. 따라서 요즘은 분석만 하면 됩니다. 제안된 관찰/기록 시간을 통해 활성 주기에서 비활성 주기로 또는 그 반대로 전환한 후 활동을 캡처할 수 있습니다. 그러나 비활성 단계는 댐이 모성 보호에 참여할 가능성이 가장 높은 시기이며, 이전에는 모성 행동에서 가장 큰 집단 차이를 포함하는 것으로 나타났다3.
알림: 마우스가 케이지 변경에 익숙해지는 데 최소 1시간이 필요하기 때문에 다른 날보다 늦게 P2 기록을 캡처하십시오. 관심 있는 변수가 아닌 한 이 날을 분석에서 삭제합니다. - 표 1에 제시된 대로 모든 행동에 점수를 매깁니다. 일반적으로 동작은 데이터 수집 시간이 시작된 후 처음 50분 동안 점수가 매겨집니다.
참고: 이 작업은 Behavioral Observation Research Interactive Software(BORIS, 오픈 소스 소프트웨어) 또는 유사한 유형의 소프트웨어를 사용하여 수동으로 또는 전자적으로 수행할 수 있습니다. 아래 지침은 수동 채점을 위한 것이며 선택한 소프트웨어에 맞게 조정할 수 있습니다. - 인쇄된 표에는 약어, 시합 시작 시간 및 지속 시간, 설명 메모를 사용하여 관찰된 행동을 기록합니다. 예를 들어, 댐이 적극적으로 수유를 하고 나서 둥지를 떠났지만 새끼가 여전히 댐에 붙어 있는 경우 이를 AN으로 기록하고 그 뒤에 O를 붙입니다. 아직 붙어 있는 새끼에 대한 설명(및 얼마나 많은)은 나중에 필요할 경우를 대비하여 측면에 메모로 보관해야 합니다.
참고: 3초 미만의 동작은 분석되지 않습니다. 이 규칙은 환경 소음과 같은 외부 방해로 인한 일시적인 동작을 필터링하는 데 도움이 됩니다. 예외는 AN 시합에 눈에 띄는 중단(예: 큰 움직임이나 스트레칭)이 있을 때 발생하며, 이는 빠르게 재개됩니다. 이 경우, 표 1에 설명된 바와 같이 AN과 N-AN이 그 뒤를 잇는다. - 한 번에 여러 행동이 발생하는 경우 가장 활동적인 행동을 기록하십시오. 예를 들어, 댐의 수유량이 낮지만 나중에 핥고 그루밍을 시작하는 경우, 낮은 수유는 중지되는 것으로 표시되며, 다음 행동은 LN 중에 발생했다는 메모와 함께 LG로 표시되어야 합니다.
| 행동 유형 | 약어 | 묘사 | ||||
| 핥아 / 그루밍 | Lg 전자 | 댐은 새끼를 핥거나 손질하는 데 종사하고 있습니다. | ||||
| 적극적인 간호 | 안 | 댐은 등을 구부리고 서서 새끼를 돌보고 있습니다. | ||||
| 새로운 액티브 간호 | (주)엔-안 | 이 동작은 댐이 수유를 중단했지만 빠르게 재개할 때 특히 사용됩니다. 이것은 3s 규칙의 예외입니다. | ||||
| 낮은 수유 | 천연가스 | 댐은 새끼에게 적극적으로 젖을 먹이고 있지만 등은 낮거나 거의 평평합니다. 이 동작은 일반적으로 일정 기간 후에 AN을 따릅니다. | ||||
| 사이드 간호 | 에스엔에스 | 댐은 수유할 때 옆으로 누워 있습니다(수동 간호라고도 함). | ||||
| 둥지 끄기 | O | 댐은 둥지에 있지 않으며 그녀는 먹거나 마시지 않습니다. 이것은 그녀가 우리 주위를 걷거나 탐험하는 것에서 관찰 할 수 있습니다. | ||||
| 음식/마실 거리 | E | 댐은 둥지에서 벗어나 먹거나 마시고 있습니다. | ||||
| 셀프 그루밍 | SG (영문) | 댐은 스스로를 손질하고 있습니다. | ||||
| 새끼 데리고 다니기 | C | 댐은 일반적으로 새끼를 둥지로 다시 이주시키기 위해 새끼를 운반합니다. | ||||
| 둥지 건물 | 주의: | 댐은 둥지를 적극적으로 건설하거나 이전하고 있습니다. | ||||
| 둥지에서 이동 | M | 댐이 둥지 위에서 움직이고 있습니다. 이것은 댐이 LG 또는 새끼를 킁킁거리거나 기르거나 밟는 것과 같은 모든 유형의 간호와는 다른 방식으로 새끼와 상호 작용하는 것을 나타냅니다. | ||||
표 1: 모성 보호 행동에 대한 설명.
4. 모성 행동 데이터 분석
- 채점 결과를 스프레드시트로 컴파일합니다.
- 비디오를 전자적으로 분석한 경우 3단계에서 설명한 대로 시합이 3초 미만인 행동을 삭제합니다.
- 관찰 일마다 평균 시합 길이, 평균 빈도 및 총 핥기 및 그루밍 시간을 계산합니다.
참고: 점수가 매겨진 모든 행동에 대해 설명 통계를 수행할 수 있지만, 핥기 및 그루밍은 일반적으로 LBN에 의한 단편화(즉, 더 짧고 더 빈번한 시합) 측면에서 가장 명백한 방해를 나타냅니다. 이러한 변수는 P3-P6의 평균으로 분석하거나 관심이 있는 경우 시간 경과에 따른 변화를 찾기 위해 일별로 반복되는 측정으로 분석할 수 있습니다.
5. 엔트로피 계산
참고: 모성 보호 행동의 엔트로피 또는 예측 불가능성은 Vegetabile et al.23이 제안한 방법에 따라 계산됩니다. 이 방법은 모성 보호 행동이 행동 시퀀스의 엔트로피 속도를 추정하는 데 사용할 수 있는 마르코프 사슬로 작용한다는 가정을 기반으로 합니다. 각 댐의 일련의 거동은 경험적 전이 행렬 ij> i,j = 1... 한 행동 (i)에서 다른 행동 (j)으로 이동하는 조건부 확률 중 7 가지이며, 엔트로피 속도는 앞서 설명한 3,23과 같이 이로부터 계산되며 다음과 같습니다.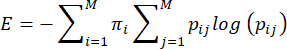
여기서 pij 는 댐이 행동 i를 수행하는 것이 관찰된 후 행동 j가 다음에 관찰될 조건부 확률이고,π i 는 행동 i가 관찰되는 빈도이며, M(=7)은 서로 다른 행동의 총 수입니다. 독자는 방정식의 이론적 토대에 대한 논의를 위해 Vegetabile et al.23 을 참조합니다. 여기서는 LBN 모델에 방법을 적용하는 방법에 초점을 맞춥니다.
- 이를 계산하려면 해석에 필요한 형식을 정렬합니다.
- AN, LN, SN 및 N-AN을 간호와 관련된 시간을 합산하여 N이라는 단일 변수로 결합합니다.
참고: 모성 보호 행동에 대한 설명은 표 1 을 참조하십시오. - 자기 주도 행동 또는 강아지 지향 행동(M 및 O)과 관련이 없는 행동을 O에 추가합니다.
- LG, E, SG, C, NB를 별도로 입력하면 총 7개의 동작이 생성됩니다.
- AN, LN, SN 및 N-AN을 간호와 관련된 시간을 합산하여 N이라는 단일 변수로 결합합니다.
- 마우스 ID, 쓰레기 ID, 쓰레기 #, 처리, 요일, 시간, 동작, 상태 순서에 따라 열이 있는 스프레드시트를 만듭니다.
- 마우스 ID에 댐의 마우스 계통/유전자형을 추가합니다.
- 쓰레기 ID에서 댐의 식별자와 쓰레기 번호를 차례로 사용합니다.
- 쓰레기 #에서 댐에 있는 쓰레기의 수를 나타냅니다.
- 동물이 배치된 조건에 따라 처리가 LBN 또는 대조군인지 확인하십시오.
- 분석된 해당 출생 후일로 날짜를 표시하십시오.
- 동작이 시작되고 종료된 비디오의 타임스탬프로 시간을 표시합니다(녹화 시작 기준).
- 앞에서 설명한 7가지(N, O, LG, E, SG, C 및 NB)에서 동작을 선택합니다(표 1).
- START와 STOP의 두 가지 유형의 상태를 표시합니다. 따라서 각 동작은 두 번 나타납니다. 첫 번째 표기법은 시작을 표시하고 두 번째 표기법은 중지를 표시합니다.
- 이 형식에 따라 분석된 모든 날짜의 정보를 포함합니다.
- R 환경에서 위와 같이 형식이 지정된 데이터 세트를 가져옵니다.
- https://github.com/bvegetabile/entropyRate 에서 사용할 수 있는 패키지를 설치합니다.
참고: 이 코드를 실행하면 LBN이라는 폴더가 생성됩니다. 조건에 관계없이 이 폴더에는 계산된 엔트로피가 들어 있습니다. 또한 각 날의 엔트로피는 P3-P6에 대한 피험자에 의해 평균화되고 조건 간에 비교될 수 있습니다.
결과
대표적인 결과는 LBN 케이지의 빈곤한 환경으로 인해 부과된 ELA가 댐에서의 모성 보호와 자손의 생리적 결과에 어떻게 영향을 미치는지를 보여줍니다. 모성 돌봄 행동의 일일 엔트로피는 P3-P6일에 걸쳐 LBN에서 더 높습니다(F1,58 = 7.21, p = 0.0094; 그림 2A), 이 기간 동안 각 댐의 평균 엔트로피(t15 = 3.03, p = 0.0085; 그림 2B). 주목할 ...
토론
이 기사에서는 마우스에 LBN 모델을 적용하기 위한 자세한 프로토콜을 제공합니다. 이 모델은 어린 시절의 만성 스트레스의 행동학적, 번역학적으로 관련된 형태가 어떻게 자손의 신경정신질환 발병에 기여하는지 이해하는 데 중요한 도구이다13. 또한 분자, 신경내분비 또는 회로 기반 관점에서 모성 행동과 댐 뇌의 변화를 연구하는 데 유용하다24. 이러한 유형?...
공개
저자는 이해 상충이 없습니다.
감사의 말
이 연구는 NIMH K99/R00 Pathway to Independence Award #MH120327, Whitehall Foundation Grant #2022-08-051, Brain & Behavior Research Foundation 및 The John and Polly Sparks Foundation의 NARSAD Young Investigator Grant #31308의 지원을 받았습니다. 저자들은 동물을 특별히 보살펴 준 조지아 주립 대학의 동물 자원학과와 비디오 관리 시스템을 설정하고 유지 관리하는 데 탁월한 기술 지원을 해준 Ryan Sleeth에게 감사의 뜻을 전합니다. Bolton 박사는 또한 박사 후 연구원 기간 동안 LBN 모델의 적절한 구현에 대한 훌륭한 교육을 제공한 Tallie Z. Baram 박사에게 감사를 표하고 싶습니다.
자료
| Name | Company | Catalog Number | Comments |
| 2-inch 4 MP 4x Zoom IR Mini PT Dome Network Camera | Hikvision | DS-2DE2A404IW-DE3(S6) | |
| Amazon Basics Aluminum Light Photography Tripod Stand with Case - Pack of 2, 2.8 - 6.7 Feet, 3.66 Pounds, Black | Amazon | From Amazon | |
| Blue Iris | Blue Iris Security | Optional video management software | |
| CAMVATE 1/4"-20 Mini Ball Head with Ceiling Mount for CCTV & Video Wall Monitors Mount - 1991 | Camvate | From Amazon | |
| Corn cob bedding | The Andersons | 4B | |
| Cotton nestlet | Ancare | NES3600 | |
| Mesh divider | McNICHOLS | 4700313244 | Standard, Aluminum, Alloy 3003-H14, 3/16" No. .032 Standard (Raised), 70% Open Area |
| Tendelux DI20 IR Illuminator | Tendelux | From Amazon |
참고문헌
- Warhaftig, G., Almeida, D., Turecki, G. Early life adversity across different cell- types in the brain. Neurosci Biobehav Rev. 148, 105113 (2023).
- Duffy, K. A., Mclaughlin, K. A., Green, P. A. Early life adversity and health-risk behaviors: Proposed psychological and neural mechanisms. Ann N Y AcadSci. 1428 (1), 151-169 (2018).
- Molet, J., et al. Fragmentation and high entropy of neonatal experience predict adolescent emotional outcome. Transl Psychiatry. 6 (1), e702 (2016).
- Garvin, M. M., Bolton, J. L. Sex-specific behavioral outcomes of early-life adversity and emerging microglia-dependent mechanisms. Front Behav Neurosci. 16, 1013865 (2022).
- Andersen, S. L. Neuroinflammation, early-life adversity, and brain development. Harv Rev Psychiatry. 30 (1), 24-39 (2022).
- Shrider, E. A., Creamer, J. . Poverty in the United States: 2022. , 60 (2023).
- Roos, L. L., Wall-Wieler, E., Lee, J. B. Poverty and early childhood outcomes. Pediatrics. 143 (6), e20183426 (2019).
- Ader, R., Tatum, R., Beels, C. C. Social factors affecting emotionality and resistance to disease in animals: I. Age of separation from the mother and susceptibility to gastric ulcers in the rat. J Comp Physiol Psychol. 53 (5), 446-454 (1960).
- Nishi, M. Effects of early-life stress on the brain and behaviors: Implications of early maternal separation in rodents. Int J Mol Sci. 21 (19), 7212 (2020).
- Trujillo, V., Durando, P. E., Suárez, M. M. Maternal separation in early life modifies anxious behavior and fos and glucocorticoid receptor expression in limbic neurons after chronic stress in rats: Effects of tianeptine. Stress. 19 (1), 91-103 (2016).
- Yu, S., et al. Early life stress enhances the susceptibility to depression and interferes with neuroplasticity in the hippocampus of adolescent mice via regulating miR-34c-5p/SYT1 axis. J Psychiatr Res. 170, 262-276 (2023).
- Walker, C. D., et al. Chronic early life stress induced by limited bedding and nesting (LBN) material in rodents: Critical considerations of methodology, outcomes and translational potential. Stress. 20 (5), 421-448 (2017).
- Rice, C. J., Sandman, C. A., Lenjavi, M. R., Baram, T. Z. A novel mouse model for acute and long-lasting consequences of early life stress. Endocrinology. 149 (10), 4892-4900 (2008).
- Glynn, L. M., Baram, T. Z. The influence of unpredictable, fragmented parental signals on the developing brain. Front Neuroendocrinol. 53, 100736 (2019).
- Karst, H., et al. Acceleration of GABA-switch after early life stress changes mouse prefrontal glutamatergic transmission. Neuropharmacology. 234, 109543 (2023).
- Demaestri, C., et al. Resource scarcity but not maternal separation provokes unpredictable maternal care sequences in mice and both upregulate CRH-associated gene expression in the amygdala. Neurobiol Stress. 20, 100484 (2022).
- Breton, J. M., et al. Early life adversity reduces affiliative behavior with a stressed cagemate and leads to sex-specific alterations in corticosterone responses in adult mice. Horm Behav. 158, 105464 (2023).
- Bath, K. G., Manzano-Nieves, G., Goodwill, H. Early life stress accelerates behavioral and neural maturation of the hippocampus in male mice. Horm Behav. 82, 64-71 (2016).
- Bolton, J. L., et al. Early stress-induced impaired microglial pruning of excitatory synapses on immature CRH-expressing neurons provokes aberrant adult stress responses. Cell Rep. 38 (13), 110600 (2022).
- Dahmen, B., et al. Effects of early-life adversity on hippocampal structures and associated HPA axis functions. Dev Neurosci. 40 (1), 13-22 (2018).
- Bolton, J. L., Short, A. K., Simeone, K. A., Daglian, J., Baram, T. Z. Programming of stress-sensitive neurons and circuits by early-life experiences. Front Behav Neurosci. 13, 30 (2019).
- Yang, M., Lewis, F., Foley, G., Crawley, J. N. In tribute to Bob Blanchard: Divergent behavioral phenotypes of 16p11.2 deletion mice reared in same-genotype versus mixed-genotype cages. Physiol Behav. 146, 16-27 (2015).
- Vegetabile, B. G., Stout-Oswald, S. A., Davis, E. P., Baram, T. Z., Stern, H. S. Estimating the entropy rate of finite Markov chains with application to behavior studies. J Educ Behav Stat. 44 (3), 282-308 (2019).
- Rincón-Cortés, M., Grace, A. A. Postpartum scarcity-adversity disrupts maternal behavior and induces a hypodopaminergic state in the rat dam and adult female offspring. Neuropsychopharmacology. 47 (2), 488-496 (2022).
- Gallo, M., et al. Limited bedding and nesting induces maternal behavior resembling both hypervigilance and abuse. Front behav neurosci. 13, 167 (2019).
- Manzano Nieves, G., Bravo, M., Baskoylu, S., Bath, K. G. Early life adversity decreases pre-adolescent fear expression by accelerating amygdala pv cell development. eLife. 9, e55263 (2020).
- Johnson, F. K., et al. Amygdala hyper-connectivity in a mouse model of unpredictable early life stress. Transl Psychiatry. 8 (1), 49 (2018).
- Demaestri, C., et al. Type of early life adversity confers differential, sex-dependent effects on early maturational milestones in mice. Horm Behav. 124, 104763 (2020).
- Reemst, K., et al. Molecular underpinnings of programming by early-life stress and the protective effects of early dietary ω6/ω3 ratio, basally and in response to LPS: Integrated mRNA-miRNAs approach. Brain Behav Immun. 117, 283-297 (2024).
- Reemst, K., et al. Early-life stress and dietary fatty acids impact the brain lipid/oxylipin profile into adulthood, basally and in response to LPS. Front Immunol. 13, 967437 (2022).
- Reemst, K., et al. Early-life stress lastingly impacts microglial transcriptome and function under basal and immune-challenged conditions. Transl Psychiatry. 12 (1), 507 (2022).
- Wang, T., et al. The nucleus accumbens CRH-CRHR1 system mediates early-life stress-induced sleep disturbance and dendritic atrophy in the adult mouse. Neurosci Bull. 39 (1), 41-56 (2023).
- Knop, J., Van, I. M. H., Bakermans-Kranenburg, M. J., Joëls, M., Van Der Veen, R. Maternal care of heterozygous dopamine receptor d4 knockout mice: Differential susceptibility to early-life rearing conditions. Genes Brain Behav. 19 (7), e12655 (2020).
- Bennett, S. N., Chang, A. B., Rogers, F. D., Jones, P., Peña, C. J. Thyroid hormones mediate the impact of early-life stress on ventral tegmental area gene expression and behavior. Horm Behav. 159, 105472 (2024).
- Parel, S. T., et al. Transcriptional signatures of early-life stress and antidepressant treatment efficacy. Proc Natl Acad Sci U S A. 120 (49), e2305776120 (2023).
- Julie-Anne, B., et al. Reactivation of early-life stress-sensitive neuronal ensembles contributes to lifelong stress hypersensitivity. J Neurosci. 43 (34), 5996 (2023).
- Bolton Jessica, L., et al. Maternal stress and effects of prenatal air pollution on offspring mental health outcomes in mice. Environ Health Perspect. 121 (9), 1075-1082 (2013).
- Block, C. L., et al. Prenatal environmental stressors impair postnatal microglia function and adult behavior in males. Cell Rep. 40 (5), 111161 (2022).
- Peña, C. J., et al. Early life stress alters transcriptomic patterning across reward circuitry in male and female mice. Nat Commun. 10 (1), 5098 (2019).
- Lapp, H. E., Salazar, M. G., Champagne, F. A. Automated maternal behavior during early life in rodents (amber) pipeline. Sci Rep. 13 (1), 18277 (2023).
- Madison, F. N., Palin, N., Whitaker, A., Glasper, E. R. Sex-specific effects of neonatal paternal deprivation on microglial cell density in adult California mouse (Peromyscus californicus) dentate gyrus. Brain, Behav. Immun. 106, 1-10 (2022).
- Walker, S. L., Sud, N., Beyene, R., Palin, N., Glasper, E. R. Paternal deprivation induces vigilance-avoidant behavior and accompanies sex-specific alterations in stress reactivity and central proinflammatory cytokine response in California mice (Peromyscus californicus). Psychopharmacology. 240 (11), 2317-2334 (2023).
- Molet, J., Maras, P. M., Avishai-Eliner, S., Baram, T. Z. Naturalistic rodent models of chronic early-life stress. Dev Psychobiol. 56 (8), 1675-1688 (2014).
- Tsuchimine, S., et al. Comparison of physiological and behavioral responses to chronic restraint stress between C57BL/6J and balb/c mice. Biochem Biophys Res Commun. 525 (1), 33-38 (2020).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유