Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
İnsan Kök Hücre Bakımı ve Bağırsak Organoid Üretimi için Bazal Membran Matrislerinin Karşılaştırmalı Çalışması
Bu Makalede
Özet
Organoidler, hastalık modellemesi için değerli araçlar haline geldi. Hücre dışı matris (ECM), organoid üretimi sırasında hücre kaderini yönlendirir ve doğal dokuya benzeyen bir sistem kullanmak model doğruluğunu artırabilir. Bu çalışma, hayvan kaynaklı ECM ve kseno içermeyen hidrojellerde indüklenmiş pluripotent kök hücrelerden türetilmiş insan bağırsak organoidlerinin üretimini karşılaştırmaktadır.
Özet
Hücre dışı matriks (ECM), hücre davranışı ve gelişiminde kritik bir rol oynar. İnsan kaynaklı pluripotent kök hücrelerden (hiPSC'ler) üretilen organoidler birçok araştırma alanının ilgi odağındadır. Bununla birlikte, klasik hücre kültürü materyallerinde fizyolojik ipuçlarının olmaması, verimli iPSC farklılaşmasını engellemektedir. Ticari olarak temin edilebilen ECM'nin kök hücre kültürüne dahil edilmesi, hücre bakımı için faydalı fiziksel ve kimyasal ipuçları sağlar. Hayvansal kaynaklı ticari olarak temin edilebilen bazal membran ürünleri, hücre bakımını destekleyen ECM proteinleri ve büyüme faktörlerinden oluşur. ECM, hücre kaderini modüle edebilen dokuya özgü özelliklere sahip olduğundan, klinik çalışmalara translasyonu sağlamak için kseno içermeyen matrisler kullanılır. Ticari olarak temin edilebilen matrisler hiPSC ve organoid çalışmalarında yaygın olarak kullanılırken, bu matrislerin eşdeğerliği henüz değerlendirilmemiştir. Burada, dört farklı matriste hiPSC idame ve insan bağırsak organoidleri (hIO) oluşumunun karşılaştırmalı bir çalışması yapılmıştır: Matrigel (Matris 1-AB), Geltrex (Matris 2-AB), Cultrex (Matris 3-AB) ve VitroGel (Matris 4-XF). Koloniler mükemmel yuvarlak bir şekle sahip olmasalar da, hücrelerin %85'inden fazlasının kök hücre markörü SSEA-4'ü eksprese etmesiyle minimal spontan farklılaşma vardı. Matrix 4-XF, 3D yuvarlak kümelerin oluşumuna yol açtı. Ayrıca, Matrix 4-XF hidrojel çözeltisini yapmak için kullanılan ortamdaki takviye ve büyüme faktörlerinin konsantrasyonunun arttırılması, SSEA-4'ün hiPSC ekspresyonunu 1.3 kat iyileştirdi. Matris 2-AB ile korunan hiPSC'nin farklılaşması, diğer hayvan türevli bazal membranlara kıyasla orta/arka bağırsak aşamasında daha az sferoid salınımına yol açtı. Diğerleriyle karşılaştırıldığında, kseno içermeyen organoid matris (Matris 4-O3) daha büyük ve daha olgun hIO'ya yol açar, bu da kseno içermeyen hidrojellerin fiziksel özelliklerinin organoid oluşumunu optimize etmek için kullanılabileceğini düşündürür. Toplamda, sonuçlar, farklı matrislerin bileşimindeki varyasyonların IO farklılaşmasının aşamalarını etkilediğini göstermektedir. Bu çalışma, ticari olarak temin edilebilen matrislerdeki farklılıklar hakkında farkındalık yaratır ve iPSC ve IO çalışmaları sırasında matris optimizasyonu için bir kılavuz sağlar.
Giriş
Hücre dışı matriks (ECM), hücre davranışını ve gelişimini düzenlemede merkezi bir rol oynayan dokuların dinamik ve çok işlevli bir bileşenidir. Karmaşık bir ağ olarak, yapısal destek, hücre yapışkan ligandları1 ve hücre sinyallemesini düzenleyen büyüme faktörlerinin ve sitokinlerin depolanmasını sağlar. Örneğin, yara iyileşmesi sırasında, ECM, göç eden hücreler için bir iskele görevi görür ve doku onarımında yer alan büyüme faktörlerinin bir rezervuarı olarak işlev görür2. Benzer şekilde, ECM'deki düzensizlik, fibroz ve kanser gibi çeşitli hastalıkların şiddetinde bir artışa yol açabilir 3,4. Embriyonik gelişim sırasında, ECM doku morfogenezine rehberlik eder. Örneğin, kalbin gelişiminde, ECM bileşenleri kalp dokusunun doğru mimarisini ve işlevini oluşturmada rol oynar5. On yıldan fazla bir süredir yapılan araştırmalar, mikro çevrenin sertliğinintek başına 6,7'nin kök hücre soy spesifikasyonunu kontrol edebileceğini göstermiştir. Bu nedenle, in vitro hücre farklılaşması sırasında ECM'nin farklılaşma için sinyaller sağlayarak kök hücre kaderini etkilemesi şaşırtıcı değildir.
Organoidler, indüklenmiş pluripotent kök hücrelerden (iPSC'ler) üretilebilir. Organoidleri başarılı bir şekilde oluşturmak için uygun şekilde karakterize edilmiş bir iPSC hattı ile başlamak gerekir. Bununla birlikte, klasik hücre kültürü materyallerinde fizyolojik ipuçlarının eksikliği, verimli iPSC farklılaşmasını ve organoid oluşumunu engeller. Ayrıca, son araştırmalar, organoid genişleme ve farklılaşma 12 bağlamında hücre dışı matrisin (ECM) bileşiminin, hücreler ve ECM8 arasındaki etkileşimlerin yanı sıra mekanik ve geometrik ipuçlarının 9,10,11 önemini vurgulamıştır. Tekrarlanabilirliği artırarak organoid teknolojisini ilerletmek, dokuya özgü fiziksel ve kimyasal ipuçlarının dahil edilmesini içerecektir.
Organoidler, doğal dokuyu fizyolojik olarak benzer bir mikro çevre içinde özetlemeyi amaçlar. Doğal doku ECM'sini yakından taklit eden bir ECM sistemi seçmek, hücre davranışı, işlevi ve uyaranlara yanıt ile ilgili fizyolojik alaka düzeyini elde etmek için çok önemlidir13. ECM bileşenlerinin seçimi, kök hücrelerin organoid içindeki belirli hücre tiplerine farklılaşmasını etkileyebilir. Farklı ECM proteinleri ve bunların kombinasyonları, hücre kaderini yönlendiren ipuçları sağlayabilir14. Örneğin, çalışmalar, spesifik ECM bileşenlerinin kullanılmasının, bağırsak kök hücrelerinin olgun bağırsak hücre tiplerine farklılaşmasını teşvik edebileceğini ve bunun fizyolojik olarak ilgili bağırsak organoidleri ile sonuçlanabileceğini göstermiştir15. Organoidler, hastalık modellemesi ve ilaç testi sırasında değerli bir araç olsa da, uygun bir ECM sisteminin seçilmesi bu uygulama için çok önemlidir. Uygun bir ECM sistemi, etkilenen dokuya benzeyen bir mikro çevre yaratarak hastalık modellemesinin doğruluğunu artırabilir16. Ayrıca, dokuya özgü ECM, hastalıkla ilişkili fenotipleri ve ilaç yanıtlarını daha iyi özetleyen organoidlerin üretilmesine yardımcı olabilir17. Organoid farklılaşmasında kullanılan ECM sisteminin optimize edilmesi, istenen farklılaşma sonuçlarının elde edilmesi için kritik öneme sahiptir.
Hayvansal ECM kaynaklarından (örneğin, Matrigel, Cultrex) ve kseno içermeyen hidrojelden (örneğin, VitroGel) türetilen ticari olarak temin edilebilen bazal membran sistemleri, iPSC ve organoid araştırmalarında yaygın olarak kullanılmaktadır. Bunları ticarileştiren şirketler ve bunları kullanan araştırmacılar, yıllar boyunca kendi özel ürünleri ve uygulamaları için birçok talimat ortaya koymuşlardır. Bu talimatların çoğu, bu protokolün oluşturulması için bir rehber görevi gördü. Ayrıca, içsel özellikleriyle ilişkili faydalar ve aksilikler birçok 18,19,20,21 tarafından ayrı ayrı belirtilmiştir. Bununla birlikte, iPSC ve organoid çalışmaları için en uygun sistemlerin seçimine rehberlik edecek sistematik bir iş akışı yoktur. Burada, iPSC ve organoid çalışmaları için çeşitli kaynaklardan ECM sistemlerinin eşdeğerliğini sistematik olarak değerlendirmek için bir iş akışı sağlanmaktadır. Bu, dört farklı matriste iki farklı insan iPSC hattının (hiPSC) ve insan bağırsak organoidlerinin (hIO) oluşumunun sürdürülmesinin karşılaştırmalı bir çalışmasıdır: Matrigel (Matris 1-AB), Geltrex (Matris 2-AB), Cultrex (Matris 3-AB) ve VitroGel (Matris 4-XF). Organoid kültür için, daha önce organoid kültür için optimize edilmiş kseno içermeyen matris VitroGel'in dört versiyonu kullanıldı: ORGANOID 1 (Matris 4-O1), ORGANOID 2 (Matris 4-O2), ORGANOID 3 (Matris 4-O3), ORGANOID 4 (Matris 4-O4). Ayrıca, organoidler için optimize edilmiş hayvan türevli matrisler kullanıldı: Matrigel Yüksek Konsantrasyon (Matris 1-ABO) ve Cultrex Tip 2 (Matris 3-ABO). Piyasada bulunan kök hücre kültür ortamı (mTeSR Plus) ve organoid farklılaşma kiti (STEMdiff intestinal organoid kit) kullanıldı. Bu protokol, okuyucuyu belirli iPSC ve organoid çalışmaları için ECM'nin başarılı bir şekilde optimizasyonuna yönlendirmek için ürün üreticilerinin bireysel talimatlarını laboratuvar deneyimleriyle birleştirir. Toplamda, bu protokol ve temsili sonuçlar, kök hücre çalışması ve organoid farklılaşması için en uygun mikro ortamın seçilmesinin önemini vurgulamaktadır.
Protokol
1. hiPSC bakımı
DİKKAT: Tüm çalışmalar, standart aseptik teknikler izlenerek bir Biyogüvenlik Kabininde (BSC) yapılır. Laboratuvar önlükleri, eldivenler ve gözlükler gibi kişisel koruyucu ekipmanların uygun kullanımı da dahil olmak üzere laboratuvarlar için OSHA güvenlik standartlarına uymalıdır.
- Matrislerin, alikotların ve hücre kültürü ortamlarının hazırlanması
- Ticari olarak temin edilebilen hayvan kaynaklı bazal membranlar (BM'ler; Matris 1-AB, Matris 2-AB, Matris 3-AB), Tablo 1'de özetlenen üreticinin tavsiyesine göre çalışma hacimlerinin alikotlarını hazırlayın ve uzun süreli depolama için -20 °C veya -80 °C'de saklayın. Kabarcık oluşumundan kaçının. Bazı kabarcıklar oluşursa, saklamadan önce, köpüğü yüzeye çıkmaya zorlamak için numuneleri 4 °C'de, <200 x g'da ~1-2 dakika santrifüjleyin.
NOT: Tek kullanımlık alikotlar yapmak, ECM mimarisini bozan tekrarlanan donma-çözülme döngülerinin önlenmesine yardımcı olur. BM konsantrasyonu lot numarasına göre değiştiğinden, tek kullanımlık alikotlar hazırlamak ve kaplama çözeltileri yapmak için üreticinin tavsiyesine uyduğunuzdan emin olun. Yüksek konsantrasyonlu BM'ler viskozdur ve pipetlenmesi zordur; daha önce -20 °C'de saklanmış soğuk uçları kullanın. - Üreticinin tavsiyesine göre kök hücre kültürü ortamını hazırlayın. Bu protokolde kullanılan ticari olarak temin edilebilen spesifik komple besiyerini hazırlamak için, 400 mL bazal besiyerine 100 mL 5x takviye kokteyli ekleyin. Daha sonra, bu ortamı iyice karıştırın ve 20 ° C'de saklanan 40 mL'lik hacimlere ayırın. Kullanım için, tam ortamın her bir alikotunu çözün, alıntılanan tam ortamı hemen kullanın veya 2 - 8 ° C'de 2 haftaya kadar saklayın. Tekrar dondurmayın.
- Matrix 4-XE Hidrojeli hazırlamak için takviye kokteylinin konsantrasyonunun 3 katını içeren kök hücre tam ortamının alikotlarını hazırlayın, yani 5x takviyeyi 3x'e seyreltin.
- Ticari olarak temin edilebilen hayvan kaynaklı bazal membranlar (BM'ler; Matris 1-AB, Matris 2-AB, Matris 3-AB), Tablo 1'de özetlenen üreticinin tavsiyesine göre çalışma hacimlerinin alikotlarını hazırlayın ve uzun süreli depolama için -20 °C veya -80 °C'de saklayın. Kabarcık oluşumundan kaçının. Bazı kabarcıklar oluşursa, saklamadan önce, köpüğü yüzeye çıkmaya zorlamak için numuneleri 4 °C'de, <200 x g'da ~1-2 dakika santrifüjleyin.
- Doku kültürü plastiğinin hayvansal kaynaklı BM'lerle kaplanması (Matrix 1-3AB)
- Başlamadan önce aşağıdakileri hazırlayın: Jelleşmelerini önlemek için matrisleri çözdürürken ve tutarken daima buzda tutun. Seyreltilmiş matrisleri hazırlamak için soğuk ortam kullanın. Başlamadan önce ve hiPSC farklılaşma sürecinin ve hIO organoid oluşumunun her aşamasında hücreleri test etmek için koşul başına yeterli sayıda çoğaltma kuyusu hazırlayın.
NOT: Burada, bu çalışma için 24 oyuklu plakalar kullanılmıştır. Diğer plaka boyutları için önerilen kaplama hacimleri için Tablo 2'ye bakın. - Her matris tipi için, 50 mL'lik konik bir tüpte 15 mM HEPES içeren 25 mL soğuk avans DMEM / F-12 hazırlayın. Bunları buz üzerinde tutun.
- Çözülmüş matrisleri ilgili soğuk avans DMEM / F-12'ye ekleyin ve iyice karıştırın. Karıştırma işlemi sırasında ortamı soğuk tutun. Topak olmadığından emin olarak homojen karışım olup olmadığını görsel olarak kontrol edin.
- Kullanım için seçilen her bir kuyuyu kaplamak için hemen seyreltilmiş matris çözeltilerini kullanın (24 oyuklu plaka kullanılıyorsa 250 μL/kuyu).
- Kaplama solüsyonunu yüzeye eşit şekilde yaymak için kültür kabını hafifçe eğin. Kullanmadan önce oda sıcaklığında (15 - 25 °C) en az 1 saat inkübe edin.
NOT: Hemen kullanılmazsa, plaka kaplamadan sonra 2 - 8 °C'de 1 haftaya kadar saklanabilir, ancak buharlaşmayı önlemek için şeffaf bir film ile kapatılmalıdır. Saklanan plakaları kullanırken, bir sonraki adıma geçmeden önce 30 dakika oda sıcaklığına (15 - 25 °C) ulaşmalarına izin verin. - Fazla çözeltiyi serolojik bir pipet kullanarak veya aspirasyonla nazikçe çıkarın. Kaplanmış yüzeyin çizilmediğinden emin olun.
- Hemen ılık tam kök hücre ortamını ekleyin (belirli bir kuyucuk için gereken toplam hacmin% 50'si, ör. 24 oyuklu bir plaka kullanılıyorsa 250 μL / kuyu).
- Başlamadan önce aşağıdakileri hazırlayın: Jelleşmelerini önlemek için matrisleri çözdürürken ve tutarken daima buzda tutun. Seyreltilmiş matrisleri hazırlamak için soğuk ortam kullanın. Başlamadan önce ve hiPSC farklılaşma sürecinin ve hIO organoid oluşumunun her aşamasında hücreleri test etmek için koşul başına yeterli sayıda çoğaltma kuyusu hazırlayın.
- Doku kültürü plastiğinin Matrix 4-XE hidrojel ile kaplanması
- Başlamadan önce aşağıdakileri hazırlayın: Matrix 4-XE hidrojeli buzdolabından çıkarın ve oda sıcaklığına (25 °C) ısınmaya bırakın. Başlamadan önce ve hiPSC farklılaşma sürecinin ve hIO organoid oluşumunun her aşamasında hücreleri test etmek için koşul başına yeterli sayıda çoğaltma kuyusu hazırlayın.
NOT: Burada, bu çalışma için 24 oyuklu plakalar kullanılmıştır. Diğer plaka boyutları için önerilen kaplama hacimleri için Tablo 3'e bakın. - Kök hücre kültürü için standart formülasyona (3x kök hücre ortamı) kıyasla 3x büyüme faktörü konsantrasyonu içeren eksiksiz bir kök hücre kültürü ortamı hazırlayın.
- Matrix 4-XE hidrojel ve 3x kök hücre ortamını 2:1 v/v karıştırma oranında karıştırın ve iyice karıştırmak için 5x-10x yukarı ve aşağı hafifçe pipetleyin.
- Hidrojel karışımını bir kuyu plakasına aktarın ve karışımı yüzeye eşit şekilde yaymak için kültür kabını dikkatlice eğin. 24 oyuklu bir plaka kullanıyorsanız 250 μL/kuyu kullanın. Önerilen hacimler için Tablo 3'e bakın.
- Yumuşak jel oluşumu için oda sıcaklığında 10-15 dakika bekleyin. Hidrojel oluşturma işlemi sırasında, plakayı eğerek veya sallayarak hidrojeli bozmayın.
- Başlamadan önce aşağıdakileri hazırlayın: Matrix 4-XE hidrojeli buzdolabından çıkarın ve oda sıcaklığına (25 °C) ısınmaya bırakın. Başlamadan önce ve hiPSC farklılaşma sürecinin ve hIO organoid oluşumunun her aşamasında hücreleri test etmek için koşul başına yeterli sayıda çoğaltma kuyusu hazırlayın.
- hiPSC enzim içermeyen küme geçişi ve tohumlama
- Başlamadan önce aşağıdakileri hazırlayın: geçmeden en az 1 saat önce, istenen plastik malzemeleri matrislerle kaplayın. Yeterli miktarda tam kök hücre besiyeri bulundurun ve oda sıcaklığına (15 - 25 °C) ısıtın. Tüm ortam için birden fazla ısıtma döngüsünden kaçının.
NOT: Aşağıdaki adımlar, halihazırda kurulmuş ve% >90 birleşik bir iPSC kültürünün 6 oyuklu bir plaka üzerinde geçişini ve bağırsak organoidlerinin farklılaşması için bunların 24 oyuklu plakalara tohumlanmasını açıklamaktadır. - Hücreleri 1 mL D-PBS (Ca++ ve Mg++ olmadan) ile durulayın ve aspire edin. 1 mL enzim içermeyen insan pluripotent kök hücre seçimi reaktifi ekleyin, eşit şekilde yaymak için dikkatlice döndürün ve 1 dakika içinde aspire edin. Kolonilerin sadece ince bir sıvı tabakasına maruz bırakılması gerekir.
- Koloniler daha az sıkıştırılmış görünmeye başlayana kadar 37 °C'de inkübe edin, bu ~ 3-8 dakika sürecektir.
NOT: Optimum inkübasyon süresi, kullanılan hücre hattına bağlı olarak değişebilir. En uygun inkübasyon süresi, her bir hücre hattını enzim içermeyen insan pluripotent kök hücre seçim reaktifi ile ilk kez geçirirken belirlenmelidir. - 1 mL tam kök hücre besiyeri ekleyin. Plakanın yan tarafına dikkatlice vurarak kolonileri ayırın. Plakayı diğer elinizle tuttuğunuzdan emin olun.
- 1 mL veya daha büyük bir pipetle, hücre kümeleri süspansiyonunu 15 mL'lik konik bir tüpe aktarın. Parlak alan mikroskobu kullanarak kümelerin boyutunu değerlendirin ve hücre kümesinin boyutunun 50-200 μm arasında olduğundan emin olun; Daha büyüklerse, parçalamak için konik boruyu hafifçe sallayın.
- Yığın sayımı için kullanılacak düz tabanlı 96 oyuklu bir plakanın her bir oyuğunun dibine bir xy ızgarası çizin ve kuyucukların her birine 50 μL D-PBS ekleyin. 3 kuyudan sayılan kümelerin ortalamasının alınması tavsiye edilir.
- Tüpü hafifçe sallayarak hücre kümelerinin eşit olarak dağıldığından emin olun ve ardından düz tabanlı 96 oyuklu plakanın her bir oyuğuna 5 μL küme süspansiyonu aktarın.
NOT: Kümeleri saymak için otomatik hücre sayacı kullanılması önerilmez. Manuel sayım önerilir. - Çapı 50 - 200 μm olan her kuyucuğun toplam küme sayısını sayın. Çoğu hücre kümesinin çapı > 200 μm ise (bkz. Şekil 1), 1.4.5 - 1.4.7 adımlarını tekrarlayın.
- 6.000 kümeyi tohumlamak için gereken yığın süspansiyonunun hacmini (μL cinsinden) aşağıdaki gibi hesaplayın:
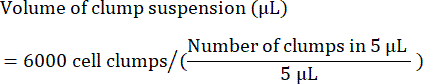
NOT: Optimum tohumlama yoğunluğu her hücre hattında optimize edilmelidir. Optimum tohumlama yoğunluğunu belirlemek için, bir dizi küme yoğunluğunda (örneğin, kuyu başına 4.000, 5.000 ve 6.000 küme) bir ilk tohumlama yapılması ve tohumlamadan 24-48 saat sonra %85-90 birleşmeye ulaşılıp ulaşılmadığını kontrol etmeniz önerilir. - Kalite kontrol olarak, kök hücre belirteçlerinin akış sitometrisi incelemesi için bir hücre örneğini ayırın. Yaygın işaretçilerin listesi için Tablo 4'e bakın.
- Farklı ECM ile kaplanmış kuyucuklarda tohumlamak için gerekli hacimde iPSC topak süspansiyonunu ayrı 15 mL'lik tüplere ayırın.
- Enzim içermeyen insan pluripotent kök hücre seçimi reaktifi içeren ortamı çıkarmak için iPSC topak çözeltisini içeren tüpü 200 x g'de 5 dakika santrifüjleyin. Santrifüjleme için beklerken, daha önce yapılmadıysa, her kuyuya her kuyu başına istenen hacmin% 50'sini ekleyin.
- Başlamadan önce aşağıdakileri hazırlayın: geçmeden en az 1 saat önce, istenen plastik malzemeleri matrislerle kaplayın. Yeterli miktarda tam kök hücre besiyeri bulundurun ve oda sıcaklığına (15 - 25 °C) ısıtın. Tüm ortam için birden fazla ısıtma döngüsünden kaçının.
- Hayvan kaynaklı matrisler içeren plakalarda iPSC kültürü
- İstenen yoğunluğu elde etmek için iPSC'lerin hesaplanan %50 tam kök hücre ortamı hacmindeki kümelerini nazikçe yeniden süspanse edin ve hücre agrega karışımını, hesaplanan tam kök hücre ortamının %50'sini içeren kaplanmış oyuklar üzerine yerleştirin.
NOT: ROCK-1 inhibitörü eklemek, bazı hücre hatları için veya kümeler 50 μm veya daha küçük olduğunda gerekli olabilir. Erken gastrulasyonu önlemek için <10 μm eklenmesi önerilir. - Matrislerin üzerine hücreli ortamı, 24 oyuklu bir plaka kullanılıyorsa 250 μL / kuyu dikkatlice ekleyin. Diğer boyuttaki kuyu plakaları için önerilen hücre ortamı hacmi için Tablo 2'ye bakın.
- Hücre kümelerini eşit olarak dağıtmak için plakayı birkaç kısa ileri geri ve yan yana hareketlerle eğin.
DİKKAT: Agregaların eşit olmayan dağılımı, insan iPSC'lerinin kendiliğinden farklılaşmasının artmasına neden olur. Kümelerin süspansiyonunun dairesel olarak yayılması, kuyuların sınırında kümelerin toplanmasına ve merkezde daha düşük yoğunluğa neden olur. - Plakayı 37 ° C'de inkübe edin ve her gün veya her gün tam kök hücre ortamı kullanarak orta değişiklikler yapın. Ortam değişiklikleri gerçekleştirirken, büyümeyi izlemek ve hücrelerin geçiş süresi gerektirip gerektirmediğini veya farklılaşmaya hazır olup olmadığını belirlemek için kültürleri görsel olarak değerlendirin. Art arda iki günlük beslemeyi atlamak için, tek bir gün için gereken ortamın hacminin 2 katını ekleyin.
- İstenen yoğunluğu elde etmek için iPSC'lerin hesaplanan %50 tam kök hücre ortamı hacmindeki kümelerini nazikçe yeniden süspanse edin ve hücre agrega karışımını, hesaplanan tam kök hücre ortamının %50'sini içeren kaplanmış oyuklar üzerine yerleştirin.
- Matrix 4-XE içeren plakalarda iPSC kültürü
- İstenen yoğunluğu elde etmek için iPSC'lerin kümelerini, hesaplanan toplam 3x kök kök hücre ortamı hacmine nazikçe yeniden süspanse edin.
- 24 oyuklu bir plaka kullanıyorsanız, hidrojel 250 μL/kuyu üzerine hücreli ortamı dikkatlice ekleyin. Diğer boyuttaki kuyu plakaları için önerilen hücre ortamı hacmi için Tablo 3'e bakın.
DİKKAT: Hidrojel şişecek ve taze yapılmış olandan daha büyük bir hacim kaplayacaktır. iPSC kolonileri, plakanın altındaki hidrojele kısmen gömülecektir, bu nedenle hidrojeli bozmadan üst ortamın %50-80'inin değiştirilmesi önerilir. - Hücre kümelerini eşit olarak dağıtmak için plakayı birkaç hızlı, kısa, ileri geri ve yan yana hareketlerle hareket ettirin.
- Plakayı %5 CO2 ve %95 nem oranına sahip 37 °C'lik bir inkübatöre yerleştirin. Tam kök hücre ortamını kullanarak hücre ortamını değiştirin. Her gün veya gün aşırı orta değişiklikler yapın; İkincisi için, ortamın hacminin 2 katı ekleyin.
- Farklılaşmaya uygun aşamaya ulaştıklarında büyümelerini takip etmek için kültürleri görsel olarak inceleyin.
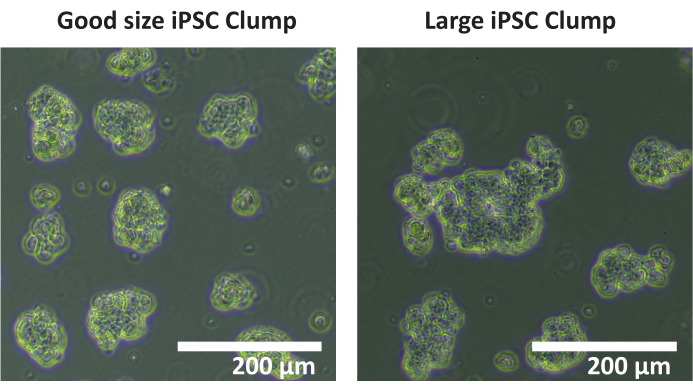
Şekil 1: Optimum yığın boyutu. Optimal küme boyutunun bir örneğini gösteren iPSC hücre hattı SCTi003A kümelerinin görüntüleri. Ölçek çubuğu = 200 μm. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
2. hiPSC farklılaşması ve bağırsak organoid oluşumu
DİKKAT: Tüm çalışmalar, standart aseptik teknikler izlenerek bir Biyogüvenlik Kabininde (BSC) yapılır. Laboratuvar önlükleri, eldivenler ve gözlükler gibi kişisel koruyucu ekipmanların uygun kullanımı da dahil olmak üzere laboratuvarlar için OSHA güvenlik standartlarına uymalıdır.
- Başlamadan önce aşağıdakileri hazırlayın: her aşama için gerekli olan farklılaşma ortamının alikotlarını hazırlayın. Alikotları çözdürdükten sonra hemen kullanın. Tekrar dondurmayın. 5 oyuklu bir plaka için gereken her aşama ortam türü ve hacimleri hakkında genel bir kılavuz için Tablo 24'i izleyin.
NOT: Her farklılaşma aşamasındaki en uygun zaman, hücre hattına göre değişebilir. Farklılaşma etkinliğini artırmak için her aşama hücre markörünün ifadesinin kontrol edilmesi önerilir. iPSCS kültürleri üzerindeki gen ekspresyonunun periyodik değerlendirmesi, düşük geçişlerde satıcı nitelikli partilerden yararlandığımız için bu araştırmaya dahil edilmemiştir, ancak sonraki farklılaşma adımları sırasında yeni/henüz kalifiye olmayan iPSC hatları için bir kalite kontrol adımı olarak önerilmektedir. - Aşama 1: Kesin endoderm (DE)
- Farklılaşmaya başlamaya hazır olup olmadığını değerlendirmek için aşağıdaki kriterleri kontrol edin.
- Bir mikroskop kullanarak, kök hücre kolonilerinin birleşmesini ve kültürdeki spontan farklılaşma miktarını değerlendirin. Sadece morfolojik değerlendirmeye güvenmeyin. Optimal birleşme %85-%90 arasında (~ 105 hücre /cm2'nin üzerinde) olmalı ve gözlenen minimum spontan farklılaşma %<5 farklılaşma olmalıdır.
- Bir sonraki adıma geçmeden önce hiPSC belirteçlerinin akış sitometrisi karakterizasyonu için kurban kuyusundan hücreleri toplayın. Temsili akış sitometrisi karakterizasyonu için bir ileri ve yan saçılma geçit stratejisi kullanıldı. Hücreler en uygun kriterleri karşılıyorsa, farklılaşmaya başlayın. Hücre geçirme kriteri, özellikle laboratuvarda yeni/henüz kalifiye olmayan iPSC hatları olması durumunda, ideal olarak 3 markörün >85% ifadesidir (Tablo 4).
NOT: Farklı matrisler üzerinde büyütülen iPSC kültürleri, yarı gömülü hücreleri rahatsız etmemek için daha yumuşak ortam değişiklikleri gerektiren, yalnızca Matrix 4-XE'de iPSC büyümesi ile aynı genel işleme tabi tutulur. Kesin endodermin indüksiyonu sırasında önemli hücre ölümü beklenir, çünkü hücreler bu aşamada özellikle hassastır. Hücrelerin 37 ° C inkübasyon ortamı dışında maruz kaldığı süreyi mümkün olduğunca en aza indirmeyi hedefleyerek ortam değişiklikleri sırasında dikkatli olun.
- Aşağıda tarif edildiği gibi hücre kolonilerinin farklılaşmasını başlatın.
- 0. Gün: DE besiyerine bir alikotu 37 °C'ye ısıtın. Ortamın ısınma-soğutma döngülerinden denatüre olmasını önlemek için, yalnızca Gün 0 (0.7 mL / kuyu) için gereken hacmi ısıttığınızdan emin olun.
- Medyayı hiPSC'lerden aspire edin. Kuyu kenarına kuyu başına dikkatlice 0.7 mL DE Medium ekleyin. Kolonileri ayırabilecek veya onlara zarar verebilecek sert pipetlemeden kaçının. Plakayı 37 °C'de, %5 CO2 ve %95 nem ile 24 saat inkübe edin.
- 1. Gün: Sadece 1. Gün için gereken hacmi (0.5 mL / kuyu) içeren bir DE ortamı alikotunu 37 ° C'ye ısıtın. DE ortamını hücrelerden aspire edin ve kuyu kenarına her kuyu başına dikkatlice 0.5 mL DE ortamı ekleyin. 37 °C'de %5 CO2 ve %95 nem ile 24 saat inkübe edin.
- 3. Gün: Hücreler kesin endoderm oluşumu için test edilmeye hazırdır. Önerilen işaretler için Tablo 4'e bakın. Bir sonraki aşamaya geçmeden önce, DE ile ilişkili spesifik belirteçlerin akış sitometrisi karakterizasyonunu gerçekleştirmek için bir kuyuyu feda edin. Temsili akış sitometrisi karakterizasyonu için bir ileri ve yan saçılma geçit stratejisi kullanıldı. Özellikle laboratuvarda yeni/henüz kalifiye olmayan iPSC hatları söz konusu olduğunda, 1'den fazla işaretleyicinin ifadesinin kontrol edilmesi önerilir.
- Farklılaşmaya başlamaya hazır olup olmadığını değerlendirmek için aşağıdaki kriterleri kontrol edin.
- Aşama 2: Midgut / Hindgut (MH)
- 3. Gün: Sadece 3. gün için gereken MH ortamının hacmini (0.5 mL / kuyu) 15 - 25 ° C'ye ısıtın. Hücrelerden DE besiyerini aspire edin ve 0.5 mL MH Besiyeri ile değiştirin. 37 °C'de %5 CO2 ve %95 nem ile 24 saat inkübe edin.
- 4 - 9. Günler: Günlük ortam değişikliklerinden önce, görünür 3D yapıları kontrol ederek sferoid oluşumunu değerlendirmek için mikroskobu 2x veya 4x büyütmede kullanın (4. günden itibaren olabilir); serbest yüzen sferoidler (5. günden itibaren ortaya çıkabilir).
- Sferoidler ayrılmaya başladığında, hücrelerden ayrılan sferoidlerin sayısını değerlendirmek için ortamı hücrelerden steril 15 mL'lik bir konik tüpe nazikçe aktarmak için 1 mL'lik bir pipetleyici kullanın.
NOT: 3B yapıları tek katmandan ayırabilecek herhangi bir kesme kuvvetinden kaçının; Hazır olduklarında, sferoidler kendi başlarına ayrılacaktır. - 50'den az sferoid ayrılırsa, 5 dakika boyunca 200 x g'da santrifüjleyin, eski ortamı çıkarın ve sferoidleri 0.5 mL / oyuklu ortamda yeniden süspanse edin ve yeterli sferoid olgunlaşana kadar ilgili kuyuya aktarın.
NOT: Orta bağırsak/arka bağırsak ortamına maruz kalma süresi, duodenum (daha kısa maruz kalma) veya ileum (daha uzun maruz kalma) gibi gelişmekte olan ince bağırsak organoidlerinin bölgesel kimliğini belirlemede çok önemli bir rol oynar. Aynı kimliğe sahip daha tek tip kültürler elde etmek için, orta bağırsak/arka bağırsak ortamına maruz kalan sferoidleri aynı anda toplamayı hedefleyin. - İnsan bağırsak organoid (hIO) kültürünü gömmek ve başlatmak için yeterli sferoid ayrılana kadar adım 2.3.3'ü tekrarlayın.
- Bir sonraki aşamaya geçmeden önce, bir sferoid örneğini ayırın ve Midgut / Hindgut (MH) ile ilişkili spesifik belirteçlerin bir akış sitometrisi karakterizasyonunu gerçekleştirin. Temsili akış sitometrisi karakterizasyonu için bir ileri ve yan saçılma geçit stratejisi kullanıldı. Yaygın olarak kullanılan işaretçilerin listesi için Tablo 4'e bakın. Özellikle laboratuvarda yeni/henüz kalifiye olmayan iPSC hatları söz konusu olduğunda, 1'den fazla işaretleyicinin ifadesinin kontrol edilmesi önerilir.
- Aşama 3: Küresel gömme
- Prosedüre başlamadan önce aşağıdakileri hazırlayın.
- Matris 1-ABO ve Matris 3-ABO'nun alikotlarını buz üzerinde çözün. Kubbe başına 30-40 μL matris gerekecekse, gereken toplam matris miktarını belirlemek için toplanan sferoid sayısını göz önünde bulundurun.
- 15 mM HEPES içeren 25 mL soğuk Advance DMEM / F-12 hazırlayın. Yüksek konsantrasyonlu ECM'ler viskozdur ve pipetlenmesi zordur. İşleme yardımcı olabilecek soğuk uçlar hazırlamak için -20 °C'de bir kutu steril 100 μL pipet ucu yerleştirin. 4 besleme gerektiren Bağırsak Organoid Büyüme Ortamının (OGM) alikotlarını hazırlayın (yem başına 0.5 mL / kuyu). Hazırlık için Tablo 5'e bakın.
- OGM takviyesinin bir kısmını buz üzerinde çözdürün. Alikotları çözdürdükten sonra hemen kullanın. Tekrar dondurmayın. Komple OGM'yi 2-8 °C'de 2 haftaya kadar saklayın.
- (3x OGM) için standart formülasyona kıyasla 3 kat takviye içeren OGM hazırlayın. Matrix 4-XFO1 thought Matrix 4-XFO4'ü buzdolabından çıkarın ve oda sıcaklığına (25 °C) ısınmaya bırakın.
- Hayvan kaynaklı sistem için aşağıda açıklanan adımları gerçekleştirin.
- Sferoidleri ve matrisleri hazırlarken 37 ° C'ye ısınması için inkübatöre steril bir 24 oyuklu doku kültürü plakası yerleştirin. Toplanan sferoidlerin 15 mL'lik konik bir tüpün dibine çökmesine izin verin. Süpernatanı dikkatlice aspire edin ve atın.
NOT: Matrislerin etkisinin daha doğru bir karşılaştırmasını yapmak için, hiPSC'den toplanan sferoidleri her matris üzerinde farklılaştırılmış ayrı tüplerde tuttuğunuzdan emin olun. - Sferoidlere 15 mM HEPES ile 1 mL DMEM / F-12 ekleyin. Oda sıcaklığında (15 - 25 ° C) 5 dakika boyunca 300 x g'da santrifüjleyin.
- Süpernatantın mümkün olduğunca çoğunu dikkatlice çıkarın. Çıkarmaya 1 mL'lik bir pipetleyici ile başlamanız ve sferoid peletini bozmadan mümkün olduğunca çıkarmak için 100 μL ve hatta 10 μL'lik pipetlere geçmeniz önerilir.
NOT: Kalan ortam hacmi ne kadar büyük olursa, matrisler o kadar seyreltilmiş olur. Seyreltilmiş matrisler jelleşme sorunlarına veya daha yumuşak kubbelere yol açabilir. Daha yumuşak kubbeler, minimum rahatsızlıkla daha yüksek çökme şansına yol açar. - Soğuk 100 μL pipet ucuna sahip bir pipetleyici kullanarak, ilgili tüplerine 40 μL/50 sferoid soğuk (2 - 8 °C) Matris 1-ABO veya Matris 3-ABO ekleyin. ~5x yukarı ve aşağı pipetleyerek sferoidleri matrise nazikçe dağıtın. Pipet ucunu tamamen boşaltmayın, bu kabarcıklara neden olabilir.
- Plakayı inkübatörden çıkarın ve soğuk bir pipet ucu kullanarak, Şekil 2'deki adımları izleyerek gömülü sferoidleri plakanın ortasına nazikçe aktarın. Matris 1-ABO ve Matris 3-ABO'yu kültür kabına çok hızlı bir şekilde dağıtmaktan kaçının, çünkü bu kubbeyi düzleştirecektir.
- Plakayı dikkatlice 37 °C'lik bir inkübatöre aktarın ve kubbe jelleşmesini sağlamak için 30 dakika inkübe edin. Taşıma sırasında ve kuvözde herhangi bir sallanma veya sert harekete karşı özellikle dikkatli olun.
- Kubbeyi jelleşme için inkübe ederken, kullanılacak kuyucuk sayısı için yeterli miktarda bağırsak OGM'sini (0,5 mL/kuyu) 37 °C'de ısıtın.
NOT: Yalnızca gereken hacmi ısıtın. Isınma-soğutma döngülerinden kaçının. Kubbeye eklemeden önce ortamın sıcak olduğundan emin olun; Soğuk ortam kubbenin çökmesine neden olabilir. - 30 dakika sonra, kubbeyi rahatsız etmemek için kuyunun yan tarafına dikkatlice 0,5 mL bağırsak OGM ekleyin. 37 °C'de %5 CO2 ve %95 nem ile inkübe edin. Ortamı çıkararak her 3-4 günde bir tam-orta değişikliği yapın ve ardından taze ortam ekleyin.
- Sferoidleri ve matrisleri hazırlarken 37 ° C'ye ısınması için inkübatöre steril bir 24 oyuklu doku kültürü plakası yerleştirin. Toplanan sferoidlerin 15 mL'lik konik bir tüpün dibine çökmesine izin verin. Süpernatanı dikkatlice aspire edin ve atın.
- Matrix 4-XF organoid sistemleri için açıklanan adımları izleyin.
NOT: Matrix 4-XF organoid sistemi dört farklı seçenek içerir (O1-O4); Her tipin formülasyonu, biyo-fonksiyonel ligandlar, sertlik ve bozunabilirlik açısından farklılık gösterir. Sonuç olarak, belirli bir uygulama için en uygun türü belirlemek için ilk deneylerin yapılması önerilir. Bu protokol, hiPSC'den türetilmiş bağırsak organoidleri için en uygun formülasyonu bulmak için dört seçeneğin kullanılmasını açıklar. Ek olarak, kullanılabilecek birden fazla kültür protokolü olsa da (örneğin, 3D kapsülleme, kubbe kapsülleme), bu protokol, hayvan kaynaklı bazal membran sistemleriyle çalışırken kullanılan yaygın yöntemlerle doğrudan karşılaştırmanın mümkün olacağı şekilde kubbe yönteminin kullanılmasını içerir.- Matrix 4-XFO4 sisteminde üretilen sferoidlere 16 mM HEPES içeren 1 mL/kuyu soğuk avans DMEM/F-12 ekleyin. Oda sıcaklığında (15 - 25 ° C) 5 dakika boyunca 300 x g'da santrifüjleyin.
NOT: Uygulama için en uygun formülasyonu bulmak için, santrifüjlemeden önce sferoidleri 4 ayrı tüpe dağıttığınızdan emin olun. Hayvan kaynaklı matrisler üzerinde üretilen sferoidler, bu sistem kullanılarak bağırsak organoidlerine de olgunlaştırılabilir. - 1 mL'lik bir pipetleyici kullanarak, sferoidleri rahatsız etmeden süpernatanı çıkarın. Sferoid peletine (~100 sferoid) 50 μL 3x OGM ekleyin. 50 μL'lik küresel süspansiyona seçilen Matrix 4-XFO'dan 100 μL ekleyin ve 5x-10x kez hafifçe karıştırın. Nihai konsantrasyon 1x'e sahip olmak için Matrix 4-XFO ila 3x OGM'yi 2:1 v/v karıştırma oranında tutun.
- 24 oyuklu bir doku kültürü plakasının merkezine 40 μL hidrojel-sferoid karışımı ekleyin. Plakaları dikkatlice 37 °C'lik bir inkübatöre aktarın ve 30 dakika inkübe edin.
NOT: Matrix 4-XFO, jelleşme için 37 °C inkübasyon gerektirmez; bununla birlikte, kubbelerin daha iyi jelleşmesi için 37 °C gerektiren Matrix 1-ABO ve Matrix 3-ABO sistemleriyle karşılaştırıldığında, organoidlerin benzer koşullara maruz kalması önerilir. - 30 dakika sonra, kubbeyi rahatsız etmemek için kuyu tarafına dikkatlice 0,5 mL bağırsak OGM ekleyin. 37 °C'de %5 CO2 ve %95 nem ile inkübe edin. Her 3-4 günde bir, ortamı çıkararak ve ardından yeni ortam ekleyerek tam orta bir değişiklik yapın.
- Matrix 4-XFO4 sisteminde üretilen sferoidlere 16 mM HEPES içeren 1 mL/kuyu soğuk avans DMEM/F-12 ekleyin. Oda sıcaklığında (15 - 25 ° C) 5 dakika boyunca 300 x g'da santrifüjleyin.
- Prosedüre başlamadan önce aşağıdakileri hazırlayın.
- hIO geçişi ve olgunlaşması
- Adım 2.4.1'de yapılanla aynı kimyasalları, çözeltileri ve reaktifleri hazırlayın.
- 15 mL'lik konik bir tüpe (koşul başına 1 adet) 1-2 mL yapışma önleyici durulama solüsyonu ekleyin ve tüpü kaplamak için döndürün.
- Yapışma önleyici solüsyonu çıkarın ve tüpleri 5 mL D-PBS (Ca++ ve Mg++ olmadan) ile durulayın. Tüm kaplanmış tüpleri kapatın ve ihtiyaç duyulana kadar oda sıcaklığında (15 - 25 °C) tutun.
- Ortamı kubbelerden aspire edin. 1 mL'lik bir pipet kullanarak, kubbeye doğrudan 1 mL soğuk DMEM/F-12 ekleyin. Amaç, kubbeleri plakadan ayırmaktır.
- Kuyuya 1 mL daha soğuk DMEM / F-12 ekleyin ve kalan organoidleri hasat etmek için yukarı ve aşağı pipetleyin. Kaplanmış 15 mL konik tüplere aktarın.
NOT: Kuyuyu mikroskop altında görsel olarak inceleyerek organoidlerin başarılı bir şekilde toplandığını doğrulayın. Herhangi bir kalıntı organoid gözlenirse, adım 2.5.5'i tekrarlayın. - 1 mL'lik bir pipetleyici ile, istenen organoid boyutunda (örn. 100 - 500 μm) düzgün bir parça süspansiyonu elde edilene kadar organoidleri parçalamak için süspansiyonun yukarı ve aşağı pipetlenmesini gerçekleştirin.
NOT: Organoidlerin önerilen boyuta uygun olduğunu doğrulamak için 200 μL'lik bir pipetleyici kullanın. 200 μL'lik pipetleyicinin kullanılması, gerektiğinde ek parçalanmayı kolaylaştırarak parçaların 200 μL'lik bir pipet ucundan sorunsuz bir şekilde geçmesini sağlar.
DİKKAT: Sert veya uzun süreli pipetleme ile parçaları tek hücrelere ayırmaktan kaçının. - Parçaları sayarak veya bölme oranını kullanarak istenen organoid yoğunluğunu oluşturun. Bir alikotu ayırın ve yığın sayımı için 1.4.6-1.4.9 adımlarındakiyle aynı prosedürü kullanarak sayma işlemini gerçekleştirin.
NOT: Optimum organoid yoğunluğu hat başına optimize edilmelidir; Genel olarak, kubbe başına 40 - 80 bağırsak organoidi yoğunluğu önerilir. - Organoid sayım işlemi sırasında tüpün buz üzerine yerleştirildiğinden emin olun. Yaklaşık 5 dakika sonra, organoid parçaları yerçekimi nedeniyle tüpün dibine çökmüş olacaktır.
NOT: Organoid çözeltinin hacmi ne kadar büyük olursa, dibe çökmesi o kadar uzun sürer. - Organoidlerin üzerinde oluşan süpernatan ve bulanık tabakayı nazikçe ortadan kaldırın. Organoidlerin olgunlaştığı erken pasajlarda, bu bulutlu faz bir matrisi ve tek tek hücreleri kapsar.
- Doğrudan peletin üzerine pipetleyerek 2 mL soğuk DMEM/F-12 ekleyin. Oda sıcaklığında (15 - 25 ° C) 5 dakika boyunca 200 x g'da santrifüjleyin.
- Hayvan kaynaklı sistem için, 2.4.2.4-2.4.2.9 adımlarında açıklanan adımların aynısını izleyerek süpernatanı dikkatlice çıkarın ve atın.
- Matrix 4-XFO sistemi için, 2.4.3.2-2.4.3.4 adımlarında açıklanan adımların aynısını izleyerek süpernatanı dikkatlice çıkarın ve atın.
NOT: Matrix 4-XFO sistemi ile çalışırken, hidrojel kalıntısının optimum şekilde uzaklaştırılması için kseno içermeyen bir hidrojel organoid geri kazanım solüsyonu kullanılması önerilir. Bu geri kazanım çözümü, herhangi bir ksenojenik materyalin ortadan kaldırılmasını sağlamak için hayvan bazlı sistemlerden kseno içermeyen hidrojel sistemlerine geçerken özellikle önerilir.
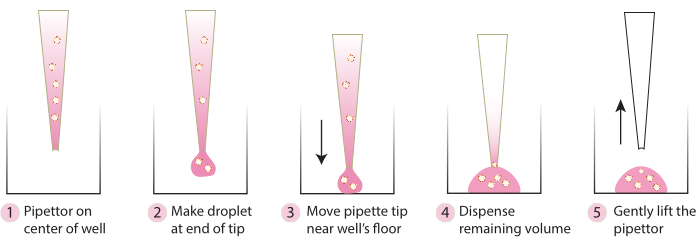
Şekil 2. Kubbe oluşumu için önerilen tekniğin şeması. Şematik, tüm sistemler için başarılı kubbe oluşumu için önerilen adım adım süreci açıklar. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
3. IO boyutu karakterizasyonu
NOT: Organoidlerin boyutu, 4x ve 10x'te çekilen parlak alan görüntüleri ile karakterize edildi. Görüntü işleme analizi MATLAB kullanılarak otomatikleştirildi. İşlemin genel adımları aşağıda açıklanmıştır ve kodun bir örneği Ek Dosya 1'e dahil edilmiştir.
- İmajları içeren dizini tanımlayın ve dizindeki tüm imaj dosyalarını listeleyin. Sonuçları depolamak için tabloyu başlatın. Bir dosyadaki parlak alan görüntülerini okuyun.
- Pikselden μm'ye dönüştürmeyi tanımlayın ve ölçeği ayarlayın. Görüntü bir ölçek çubuğu içermiyorsa, kullanıcıdan pikselden μm'ye dönüştürme faktörünü isteyin.
- Görüntüyü gri tonlamaya dönüştürün. Görüntüdeki paraziti azaltmak için bir Gauss filtresi uygulayın. Organoidleri arka plandan ayırmak için filtrelenmiş görüntüyü eşikleyin.
- İkili görüntüyü temizlemek için küçük delikleri doldurun ve küçük nesneleri çıkarın. Tek tek organoidleri tanımlamak ve alan, merkez, ana eksen uzunluğu ve küçük eksen uzunluğu gibi özelliklerini hesaplamak için bağlı bileşen analizi gerçekleştirin.
- Ana ve küçük eksen uzunluklarına göre organoid boyutunu hesaplayın. Segmentlere ayrılmış organoidleri orijinal görüntüde görüntüleyin ve boyutlarına göre etiketleyin. Organoid boyutlarını yazdırın ve sonuçları .cvs dosyasında saklayın.
NOT: İlk birkaç görüntü, Gauss filtresi standart sapması ve eşik değerine kadar olan alan için en uygun parametreleri belirlemek için manuel olarak analiz edilmiştir. Ek Dosya 1'deki kod, parlak alan görüntülerinden organoid boyut analizi için temel çerçevenin bir örneğini sağlar; Ancak, her görüntü türü ve kalitesi için özel gereksinimlere uymak için daha fazla iyileştirme gerekir. Aynı işlem, Image J'den FIJI gibi açık kaynaklı yazılımlar kullanılarak da yapılabilir. - FIJI yazılımını kullanmak için aşağıdaki adımları izleyin.
- Pikselden μm'ye dönüştürmeyi tanımlayın ve ölçeği ayarlayın. Görüntü bir ölçek çubuğu içermiyorsa, Analiz Et > Ölçeği Ayarla'yı tıklayarak kullanıcıdan pikselden μm'ye dönüştürme faktörünü isteyin.
- Görüntü > 8bit >yazına tıklayarak görüntüyü gri tonlamaya dönüştürün. İşlem'e tıklayarak görüntüdeki paraziti azaltmak için bir Gauss filtresi uygulayın > Filtre > Gauss tanıtım yazısı > Kullanılan Sigma (yarıçap): 2.
- Görüntü > Eşiği > MaxEntropy > Uygula'yı tıklatarak organoidleri arka plandan ayırmak için filtrelenmiş görüntünün eşiğini alın.
- İşle > Gürültü'ye tıklayarak ikili görüntüyü temizlemek için küçük delikleri doldurun > 20 pikselden > aykırı değerleri kaldırın.
- Analiz Et > Ölçümü Ayarla'ya tıklayarak tek tek organoidleri tanımlamak ve bunların alan, merkez, ana eksen uzunluğu ve küçük eksen uzunluğu gibi özelliklerini hesaplamak için bağlı bileşen analizi gerçekleştirin >Alan, Çevre ve Çap'ın dahil edildiğinden emin olun > Parçacıkları Analiz Et > Analiz Et > Ana Hatları Göster'.
- İstatistiksel analiz
- JMP (SAS) yazılımını kullanarak Saphiro-Wilk testi aracılığıyla normallik için veri dağılımını değerlendirin. Gruplar arasındaki istatistiksel farklılıkları incelemek için iki yönlü ANOVA gerçekleştirin ve JMP (SAS) yazılımında parametrik olmayan Wilcoxon yöntemini kullanarak post-hoc test yapın. Anlamlılık, p ≤ 0.05 alfa düzeyinde kurulmuştur.
Sonuçlar
Bu protokolü takiben, hiPSC hücrelerini yetiştirmek ve bunları hIO'ya farklılaştırmak için ticari olarak temin edilebilen bazal membranlar ve kseno içermeyen bir hidrojel sistemi başarıyla kullanıldı. Bu deneylerin temel amacı, hiPSC ve hIO çalışmaları için çeşitli kaynaklardan alınan matrislerin eşdeğerliğini sistematik olarak değerlendirmekti. Bu protokolün ilk bölümü, verimli bir bağırsak organoid üretimi sağlayan sağlıklı bir iPSC kültürünün sürdürülmesi ve karakterizasyonu...
Tartışmalar
Kök hücre ve organoid çalışmaları için en uygun mikro ortamın seçilmesi, bu platformları çok çeşitli uygulamalar için kullanırken çok önemli bir erken adımdır. Temsili sonuçlarımız, Matrix 4-XFO3'ün daha yüksek konsantrasyonda büyüme faktörleri ile kombinasyon halinde daha büyük organoidlere yol açtığını göstermektedir, bu da kseno içermeyen hidrojellerin fiziksel özelliklerinin bu sistemler kullanılarak organoid üretimini optimize etmek için kullanılabileceğini düşündürmekte...
Açıklamalar
Dr. John Huang, TheWell Bioscience'ın kurucusu ve CEO'sudur.
Teşekkürler
Yazarlar, Dr. Christina Pacak, Silveli Susuki-Hatano ve Russell D'Souza'dan hiPSC ve organoid çalışmalarına başlama ile ilgili önceki eğitimleri ve genel önerileri kabul etmektedir. İn vitro hücre kültürü çalışmaları için hidrojel sistemlerini kullanma konusundaki rehberliği için Dr. Chelsey Simmons'a teşekkür ederler. Ayrıca yazarlar, STEMCELL Technologies'den Dr. Christine Rodriguez ve Thomas Allison'a hiPSC kültürü konusundaki rehberlikleri için teşekkür eder. Yazarlar ayrıca yayın maliyetlerini karşıladığı için TheWell Bioscience'a teşekkür eder.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 24-Well Plate (Culture treated, sterile) | Falcon | 353504 | |
| 37 °C water bath | VWR | ||
| 96-well plate | Fisher Scientific | FB012931 | |
| Advanced DMEM/F12 | Life Technologies | 12634 | |
| Anti-adherence Rinsing Solutio | STEMCELL Technologies | 7010 | |
| Biological safety cabinet (BSC) | Labconco | Logic | |
| Brightfield Microscope | Echo Rebel | REB-01-E2 | |
| BXS0116 | ATCC | ACS-1030 | |
| Centrifuge with temperature control (4 °C capabilities) | ThermoScientific | 75002441 | |
| Conical tubes, 15 mL, sterile | Thermo Fisher Scientific | 339650 | |
| Conical tubes, 50 mL, sterile | Thermo Fisher Scientific | 339652 | |
| Cultrex RGF BME, Type 2 | Bio-techne | 3533-005-02 | |
| Cultrex Stem Cell Qualified RGF BME | Bio-techne | 3434-010-02 | |
| D-PBS (Without Ca++ and Mg++) | Thermo Fisher Scientific | 14190144 | |
| GeltrexLDEV-Free, hESC-Qualified Reduce Growth Factor | Gibco | A14133-02 | |
| GlutaMAX Supplement | Thermo Fischer Scientific | 35050-061 | |
| Guava Muse Cell Analyzer or another flow cytometry equipment (optional) | Luminex | 0500-3115 | |
| HEPES buffer solution | Thermo Fischer Scientific | 15630-056 | |
| Heralcell Vios Cell culture incubator (37 °C, 5% CO2) | Thermo Scientific | 51033775 | |
| JMP Software | SAS Institute | JMP 16 | |
| MATLAB | MathWorks, Inc | R2022b | |
| Matrigel Growth Factor Reduced (GFR) Basement Membrane Matrix LDEV free | Corning | 356231 | |
| Matrigel Matrix High Concentration (HC), Growth Factor Reduced (GFR) LDEV-free | Corning | 354263 | |
| mTeSR Plus Medium | STEMCELL Technologies | 100-0276 | |
| Nunclon Delta surface treated 24-well plate | Thermo Scientific | 144530 | |
| PE Mouse Anti-human CD326 (EpCAM) | BD Pharmingen | 566841 | |
| PE Mouse Anti-human CDX2 | BD Pharmingen | 563428 | |
| PE Mouse Anti-human FOXA2 | BD Pharmingen | 561589 | |
| PerCP-Cy 5.5 Mouse Anti-human SSEA4 | BD Pharmingen | 561565 | |
| ReLeSR | STEMCELL | 5872 | |
| SCTi003-A | STEMCELL Technologies | 200-0510 | |
| Serological pipettes (10 mL) | Fisher Scientific | 13-678-11E | |
| Serological pipettes (5 mL) | Fisher Scientific | 13-678-11D | |
| STEMdiff Intestinal Organoid Growth Medium | STEMCELL Technologies | 5145 | |
| STEMdiff Intestinal Organoid Kit | STEMCELL Technologies | 5140 | |
| Vitrogel Hydrogel Matrix | TheWell Bioscience | VHM01 | |
| VitroGel ORGANOID Discovery Kit | TheWell Bioscience | VHM04-K |
Referanslar
- Hynes, R. O. Integrins: Bidirectional, allosteric signaling machines. Cell. 110 (6), 673-687 (2002).
- Frantz, C., Stewart, K. M., Weaver, V. M. The extracellular matrix at a glance. J Cell Sci. 123, 4195-4200 (2010).
- Hinz, B., Gabbiani, G. Fibrosis: Recent advances in myofibroblast biology and new therapeutic perspectives. F1000 Biol Rep. 2, 78 (2010).
- Pickup, M. W., Mouw, J. K., Weaver, V. M. The extracellular matrix modulates the hallmarks of cancer. EMBO Rep. 15 (12), 1243-1253 (2014).
- Rozario, T., DeSimone, D. W. The extracellular matrix in development and morphogenesis: A dynamic view. Dev Biol. 341 (1), 126-140 (2010).
- Even-Ram, S., Artym, V., Yamada, K. M. Matrix control of stem cell fate. Cell. 126 (4), 645-647 (2006).
- Engler, A. J., Sen, S., Sweeney, H. L., Discher, D. E. Matrix elasticity directs stem cell lineage specification. Cell. 126 (4), 677-689 (2006).
- Tran, O. N., et al. Organ-specific extracellular matrix directs trans-differentiation of mesenchymal stem cells and formation of salivary gland-like organoids in vivo. Stem Cell Res Ther. 13 (1), 306 (2022).
- Nikolaev, M., et al. Homeostatic mini-intestines through scaffold-guided organoid morphogenesis. Nature. 585 (7826), 574-578 (2020).
- Gjorevski, N., et al. Designer matrices for intestinal stem cell and organoid culture. Nature. 539 (7630), 560-564 (2016).
- Gjorevski, N., et al. Tissue geometry drives deterministic organoid patterning. Science. 375 (6576), (2022).
- Heo, J. H., Kang, D., Seo, S. J., Jin, Y. Engineering the extracellular matrix for organoid culture. Int J Stem Cells. 15 (1), 60-69 (2022).
- Shamir, E. R., Ewald, A. J. Three-dimensional organotypic culture: experimental models of mammalian biology and disease. Nat Rev Mol Cell Biol. 15 (10), 647-664 (2014).
- Clevers, H. Modeling development and disease with organoids. Cell. 165 (7), 1586-1597 (2016).
- Jung, P., et al. Isolation and in vitro expansion of human colonic stem cells. Nat Med. 17 (10), 1225-1227 (2011).
- Lancaster, M. A., Knoblich, J. A. Organogenesis in a dish: Modeling development and disease using organoid technologies. Science. 345 (6194), 1247125 (2014).
- Huch, M., et al. In vitro expansion of single Lgr5+ liver stem cells induced by Wnt-driven regeneration. Nature. 494 (7436), 247-250 (2013).
- Greenlee, A. R., Kronenwetter-Koepel, T. A., Kaiser, S. J., Liu, K. Comparison of Matrigel and gelatin substrata for feeder-free culture of undifferentiated mouse embryonic stem cells for toxicity testing. Toxicol In Vitro. 19 (3), 389-397 (2005).
- Geltrex LDEV-Free, HESC-Qualified, Reduced Growth Factor Basement Membrane Matrix User Guide (Pub.No. MAN0007336 3.0. Fisher Scientific Available from: https://www.thermofisher.com/document-connect/document-connect.html?url=https://assets.thermofisher.cn/TFS-Assets%2FLSG%2Fmanuals%2FGeltrex_LDEV_Free_hESC_qualified_PI.pdf (2024)
- biotechne R&D Systems. Cultrex Stem Cell Qualified Reduced Growth Factor. biotechne R&D Systems. , (2024).
- VitroGel Organoid Protocol. TheWell Bioscience Available from: https://www.thewellbio.com/video-protocols (2024)
- Spence, J. R., et al. Directed differentiation of human pluripotent stem cells into intestinal tissue in vitro. Nature. 470 (7332), 105-110 (2011).
- Henderson, J. K., et al. Preimplantation human embryos and embryonic stem cells show comparable expression of stage-specific embryonic antigens. Stem Cells. 20 (4), 329-337 (2002).
- Haruna, N. F., Huang, J. Investigating the dynamic biophysical properties of a tunable hydrogel for 3D cell culture. J Cytol Tissue Biol. 7, 30 (2020).
- Cherne, M. D., et al. A synthetic hydrogel, VitroGel ORGANOID-3, improves immune cell-epithelial interactions in a tissue chip co-culture model of human gastric organoids and dendritic cells. Front Pharmacol. 12, 707891 (2021).
- Stewart, D. C., et al. Quantitative assessment of intestinal stiffness and associations with fibrosis in human inflammatory bowel disease. PLoS One. 13, e0200377 (2018).
- Hernandez-Gordillo, V., et al. Fully synthetic matrices for in vitro culture of primary human intestinal enteroids and endometrial organoids. Biomaterials. 254, 120125 (2020).
- Broguiere, N., et al. Growth of epithelial organoids in a defined hydrogel. Adv Mater. 30, 1801621 (2018).
- Barthes, J., et al. Cell microenvironment engineering and monitoring for tissue engineering and regenerative medicine: The recent advances. BioMed Res Int. 2014, 921905 (2014).
- Engler, A. J., Sen, S., Sweeney, H. L., Discher, D. E. Matrix elasticity directs stem cell lineage specification. Cell. 126 (4), 677-689 (2006).
- Aisenbrey, E. A., Murphy, W. L. Synthetic alternatives to Matrigel. Nat Rev Mater. 5 (7), 539-551 (2020).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır