È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Metodi basati su immagini per studiare eventi di traffico di membrana in cellule di lignaggio stomatico
In questo articolo
Riepilogo
Diversi metodi comunemente usati sono introdotti qui per studiare gli eventi di traffico di membrana di una chinasi del recettore della membrana plasmatica. Questo manoscritto descrive protocolli dettagliati tra cui la preparazione del materiale vegetale, il trattamento farmacologico e la configurazione dell'imaging confocale.
Abstract
Nelle cellule eucariotiche, i componenti della membrana, comprese le proteine e i lipidi, vengono trasportati spaziotemporalmente a destinazione all'interno del sistema endomembrana. Ciò include il trasporto secretorio di proteine di nuova sintesi sulla superficie cellulare o all'esterno della cellula, il trasporto endocitico di carichi extracellulari o componenti della membrana plasmatica nella cellula e il riciclaggio o il trasporto di carichi tra gli organelli subcellulari, ecc. Gli eventi di traffico di membrana sono cruciali per lo sviluppo, la crescita e l'adattamento ambientale di tutte le cellule eucariotiche e, quindi, sono sottoposti a una regolamentazione rigorosa. Le chinasi recettoriali della superficie cellulare, che percepiscono i segnali del ligando dallo spazio extracellulare, subiscono sia il trasporto secretorio che quello endocitico. Gli approcci comunemente usati per studiare gli eventi di traffico di membrana utilizzando una chinasi recettoriale ricca di ripetizione leucina localizzata nella membrana plasmatica, ERL1, sono descritti qui. Gli approcci includono la preparazione del materiale vegetale, il trattamento farmacologico e la configurazione dell'imaging confocale. Per monitorare la regolazione spaziotemporale di ERL1, questo studio descrive l'analisi di co-localizzazione tra ERL1 e una proteina marcatrice del corpo multi-vescicolare, RFP-Ara7, l'analisi delle serie temporali di queste due proteine e l'analisi z-stack di ERL1-YFP trattata con gli inibitori del traffico di membrana brefeldina A e wortmannin.
Introduzione
Il traffico di membrana è un processo cellulare conservato che distribuisce componenti di membrana (noti anche come carichi), tra cui proteine, lipidi e altri prodotti biologici, tra diversi organelli all'interno di una cellula eucariotica o attraverso la membrana plasmatica da e verso lo spazio extracellulare1. Questo processo è facilitato da un insieme di membrane e organelli chiamati sistema endomembrana, che consiste nella membrana nucleare, nel reticolo endoplasmatico, nell'apparato di Golgi, nel vacuolo / lisosomi, nella membrana plasmatica e negli endosomi multipli1. Il sistema endomembrana consente la modifica, il confezionamento e il trasporto dei componenti della membrana utilizzando vescicole dinamiche che fanno la spola tra questi organelli. Gli eventi di traffico di membrane sono cruciali per lo sviluppo, la crescita e l'adattamento ambientale delle cellule e, pertanto, sono soggetti a una regolamentazione rigorosa e complessa2. Attualmente, molteplici approcci in biologia molecolare, biologia chimica, microscopia e spettrometria di massa sono stati sviluppati e applicati al campo del traffico di membrana e hanno notevolmente migliorato la comprensione della regolazione spaziotemporale del sistema endomembrana 3,4. La biologia molecolare viene utilizzata per le classiche manipolazioni genetiche dei presunti attori coinvolti nel traffico di membrana, come alterare l'espressione genica della proteina di interesse o etichettare la proteina di interesse con determinati tag. Gli strumenti di biologia chimica includono l'uso di molecole che interferiscono specificamente con il traffico di determinate rotte 4,5. La spettrometria di massa è potente per identificare i componenti in un organello che è stato isolato meccanicamente con approcci biochimici 3,4. Tuttavia, il traffico di membrana è un processo biologico dinamico, diversificato e complesso1. Per visualizzare il processo di traffico di membrana in cellule vive in varie condizioni, la microscopia ottica è uno strumento essenziale. Sono stati fatti continui progressi nelle tecniche avanzate di microscopio per superare le sfide nella misurazione dell'efficienza, della cinetica e della diversità degli eventi4. Qui, questo studio si concentra sulle metodologie ampiamente adottate in biologia chimica / farmacologica, biologia molecolare e microscopia per studiare gli eventi di traffico di membrana in un sistema naturalmente semplificato e sperimentalmente accessibile, il processo di sviluppo stomatico.
Gli stomi sono micropori sulle superfici aeree delle piante che si aprono e si chiudono per facilitare lo scambio di gas tra le cellule interne e l'ambiente 6,7,8. Quindi, gli stomi sono essenziali per la fotosintesi e la traspirazione, due eventi cruciali per la sopravvivenza e la crescita delle piante. Lo sviluppo stomatico viene regolato dinamicamente da segnali ambientali per ottimizzare l'adattamento della pianta all'ambiente circostante9. Risalente a studi nel 2002, l'identificazione della proteina recettore Too Many Mouths (TMM) ha aperto le porte a una nuova era di studio dei meccanismi molecolari dello sviluppo stomatico nella pianta modello Arabidopsis thaliana10. Dopo pochi decenni, è stata identificata una via di segnalazione classica. Da monte a valle, questa via include un gruppo di ligandi peptidici secretori nella famiglia dei fattori di pattern epidermico (EFP), diverse chinasi del recettore LRR (leucine-rich-repeat) della superficie cellulare nella famiglia EREECTA (ER), la proteina del recettore LRR TMM, una cascata MAPK e diversi fattori di trascrizione bHLH tra cui SPEECHLESS (SPCH), MUTE, FAMA e SCREAM (SCRM)11,12,13,14, 15,16,17,18,19,20,21,22,23,24,25,26. Lavori precedenti indicano che una delle chinasi recettoriali, ER-LIKE 1 (ERL1), dimostra comportamenti subcellulari attivi sulla percezione di EPF20. ERL2 traffica anche dinamicamente tra la membrana plasmatica e alcuni organelli intracellulari27. Il blocco delle fasi di traffico della membrana provoca un pattern stomatico anomalo, con conseguente ammasso stomatico sulla superficie fogliare28. Questi risultati suggeriscono che il traffico di membrana svolge un ruolo essenziale nello sviluppo stomatico. Questo studio descrive un protocollo per studiare spaziotemporalmente le dinamiche ERL1 utilizzando l'analisi di co-localizzazione subcellulare proteina-proteina combinata con un trattamento farmacologico utilizzando alcuni inibitori del traffico di membrana.
Protocollo
1. Preparazione delle soluzioni
- Preparare la soluzione di sterilizzazione dei semi mescolando 15 ml di candeggina con 35 ml di acqua distillata e 50 μL di Triton X-100.
- Preparare la soluzione di brefeldina A (BFA) sciogliendo la polvere di BFA in etanolo fino a una concentrazione finale di 10 mM (stock). Preparare la soluzione di wortmannin (Wm) sciogliendo la polvere di Wm in DMSO ad una concentrazione finale di 10 mM (stock).
2. Semina i semi
- Aliquote 10-50 semi da ciascuna delle piante transgeniche necessarie in provette da microcentrifuga da 1,5 ml. Aggiungere 1 mL di soluzione di sterilizzazione dei semi in ogni tubo e mescolare accuratamente capovolgendo delicatamente il tubo per 10 minuti su uno shaker.
- Scartare la soluzione di sterilizzazione dei semi e lavare i semi con 1 ml di acqua distillata autoclavata cinque volte.
- Aggiungere 300 μL di acqua distillata autoclavata in ciascuna provetta e seminare i semi su terreni MS a metà forza contenenti 1% (p/v) di saccarosio e 0,75% (p/v) di agar. Integrare il mezzo con gli antibiotici corrispondenti, se necessario.
- Tenere la piastra capovolta a 4 °C al buio per 2 giorni per sincronizzare la germinazione.
- Dopo 2 giorni, trasferire la piastra in una camera di crescita con un ciclo di luce di 16 ore / buio di 8 ore (80 μmol/m2/s1) a 22 °C. Questo è considerato il primo giorno dopo la germinazione (1 dpg).
- Trapiantare le piantine nel terreno a 10 dpg per un'ulteriore crescita.
3. Preparazione di piante transgeniche F1 bicolore
- Coltivare piante transgeniche omozigoti portatrici di ERL1-YFP (pianta A) e piante transgeniche omozigoti portatrici di una proteina marcatrice RFP-Ara7 (pianta B)20 marcata con RFP fianco a fianco fino alla fioritura in una stanza di crescita con un ciclo di luce di 16 ore / 8 ore di buio (80 μmol / m2 / s1) a 22 ° C.
- Scegli una giovane infiorescenza dalla pianta A. Tieni un fiore che sta per aprirsi sull'infiorescenza per le croci genetiche. Rimuovere tutti i fiori e le siliques più vecchi. Inoltre, rimuovere con cura i fiori più giovani e i meristemi floreali per evitare confusione futura.
- Sezionare delicatamente il fiore non aperto rimuovendo i sepali, i petali e lo stame usando un paio di pinzette affilate. Lascia solo il pistillo sull'infiorescenza.
- Prendi uno stame maturo da un fiore aperto sulla pianta B e deposita i grani di polline sullo stigma del pistillo sezionato sulla pianta A.
- Etichetta questo fiore incrociato manualmente indicando suo padre, sua madre e la data dell'incrocio genetico. Lascia maturare il fiore e raccogli i semi F1 quando la silique diventa gialla / marrone (~ 20 giorni dopo la croce). Verifica la presenza di un impianto F1 di successo con segnali YFP e RFP.
4. Trattamento farmacologico
- Per il trattamento BFA, rimuovere i cotiledoni delle piantine di 7 giorni, immergere il resto delle piantine in una soluzione fittizia (etanolo allo 0,3%) o in una soluzione di BFA da 30 μM, applicare il vuoto per 1 minuto e mantenere il campione immerso per 30 minuti prima dell'imaging.
- Per il trattamento con wortmannin, rimuovere i cotiledoni delle piantine di 7 giorni, immergere il resto delle piantine in una soluzione DMSO allo 0,25% o in una mostomannina da 25 mM, applicare il vuoto per 1 minuto e mantenere il campione immerso per 30 minuti prima dell'imaging.
- Per il trattamento sottovuoto dei campioni, in una provetta da microcentrifuga da 1,5 ml, aggiungere 500 μL della soluzione farmacologica corrispondente e immergere le piantine sezionate nella soluzione. Collegare saldamente una siringa da 10 mL alla provetta della microcentrifuga e applicare il vuoto per 1 minuto (Figura 1). Rimuovere la siringa e conservare il campione nella soluzione per il tempo richiesto. Estrarre delicatamente le piantine per la preparazione dell'imaging.

Figura 1: Dispositivo di vuoto semplice. Una siringa da 10 ml è collegata a una provetta da microcentrifuga da 1,5 ml per il trattamento sotto vuoto. Fare clic qui per visualizzare una versione ingrandita di questa figura.
5. Preparazione del campione per l'imaging
- Sezionare la vera foglia dal campione trattato usando una lama di rasoio affilata. Metti delicatamente la foglia vera in una goccia d'acqua su un vetrino e mantieni il lato abassiale verso l'alto. Coprire lentamente la foglia vera con un coprivetrino evitando di intrappolare eventuali bolle.
6. Imaging confocale
NOTA: Un microscopio confocale a scansione invertita Leica SP8 è stato utilizzato per visualizzare il segnale di fluorescenza dei campioni in questo lavoro.
- Impostazione del percorso del fascio
- Selezionare un laser a 514 nm per l'eccitazione YFP. Utilizzare un'elevata potenza laser per aumentare l'intensità del segnale e, quindi, ottenere un'elevata qualità dell'immagine. Tuttavia, potenze laser superiori al 5% corrono il rischio di fotosbiancamento e la salute del campione può essere influenzata. Se il segnale del campione non è troppo debole, iniziare a bassa intensità laser.
- Attivare PMT/HyD per il rilevamento e definire le soglie della banda di emissione superiore e inferiore in base allo spettro per il fluoroforo YFP. Impostare una finestra di rilevamento di 530-570 nm per raccogliere il segnale YFP.
- Imaging sequenziale per il secondo colore: fai clic sul pulsante Seq e aggiungi un nuovo canale. Per impostazione predefinita, il percorso del fascio YFP progettato in precedenza sarà Seq 1. In Seq 2, selezionare un laser a 561 nm per l'eccitazione RFP e impostare una finestra di rilevamento di 570-630 nm per raccogliere il segnale RFP.
- Impostazione delle condizioni di scansione (Figura 2)
- Per visualizzare l'attività del traffico della membrana subcellulare all'interno delle cellule precursori stomatiche, scegliere una lente Corr 63x/1,2 W sul sistema per l'imaging.
- Il formato si riferisce alla dimensione dell'immagine in pixel. Inizia con 1.024 pixel x 1.024 pixel, quindi ottimizza questo in base al fattore di zoom e alle impostazioni dell'obiettivo per una buona risoluzione della qualità di pubblicazione.
- La velocità si riferisce alla velocità della testina di scansione mentre il laser passa su ciascun pixel. Sebbene le basse velocità di scansione spesso comportino un migliore rapporto segnale-rumore, potrebbero non catturare in modo efficiente gli eventi di traffico di membrane in rapida evoluzione. Inizia con una velocità di 400 Hz e ottimizzala in base alla situazione specifica dei campioni.
- Il fattore di zoom viene utilizzato per ingrandire una regione di interesse senza modificare l'obiettivo dell'obiettivo. Inizia con un fattore di zoom pari a 1 e ottimizzalo in base alle esigenze specifiche dell'esperimento.
- La media della linea si riferisce al numero di volte in cui ogni linea X verrà scansionata per ottenere un risultato medio. Una media di linea maggiore riduce il rumore nell'immagine risultante, ma aumenta anche il tempo di scansione e il tempo di esposizione alla luce laser. Per visualizzare gli eventi di traffico di membrana, non utilizzare una linea media alta. Inizia con una media di 2 righe e ottimizza secondo necessità.
- Raccolta di una serie temporale
NOTA: Quando si studiano gli eventi di traffico di membrana, è spesso necessaria una serie temporale per registrare il rapido movimento degli endosomi subcellulari.- Nella modalità di acquisizione, selezionare la modalità di scansione xyt per abilitare l'utilità Time Series.
- Decidi un periodo di attesa tra i punti temporali in Intervallo di tempo. In alternativa, fai clic su Riduci a icona per scattare immediatamente le immagini una dopo l'altra. Un intervallo di tempo di 7 s è stato utilizzato nel seguente esperimento di serie temporali.
- Seleziona Durata e immetti il tempo totale di esecuzione dell'esperimento. In alternativa, definite il numero di fotogrammi da raccogliere selezionando Fotogrammi (Figura 3).
- Per raccogliere le informazioni tridimensionali relative all'evento di traffico di membrana all'interno dell'intera cella, utilizzare la modalità di scansione Z-stack. La proiezione di massima intensità delle immagini Z-stack viene spesso utilizzata per l'analisi.
- Selezionare la modalità di scansione xyz nella modalità di acquisizione, quindi l'utilità Z-Stack diventerà accessibile.
- Selezionare l'opzione Z-wide . In modalità di scansione, definire l'immagine superiore e l'immagine inferiore dello stack Z utilizzando i pulsanti Inizio e Fine .
- Definite lo spessore dello z-step facendo clic su z-step size. In alternativa, definire quante immagini scattare per coprire l'intera gamma dello Z-stack. Per garantire la coerenza tra i campioni, definire la dimensione z-step (Figura 4).
- Elaborazione di immagini
- La proiezione di massima intensità delle immagini z-stack è generata dal software confocale (http://www.leica-microsystems.com). Nella scheda Processo principale, scegli innanzitutto il file z-stack interessato nella scheda Apri progetti all'estrema sinistra. Quindi, passare alla scheda centrale denominata Strumenti di processo, selezionare la funzione Proiezione , scegliere Massimo nel pannello a discesa di Metodo e fare clic sul pulsante Applica . Un'immagine di proiezione z-stack verrà generata nella scheda Apri progetti.
- Il video delle immagini della serie temporale è generato da Fiji (https://imagej.net/Fiji). Nella scheda File , utilizzare la funzione Apri per aprire tutte le immagini delle serie temporali nell'ordine corretto. Nella scheda Immagine , trova la funzione Stack e scegli Immagini da impilare per generare un video. Salvate il file nel formato .avi con la frequenza fotogrammi desiderata (5 fotogrammi/s per Video 1).
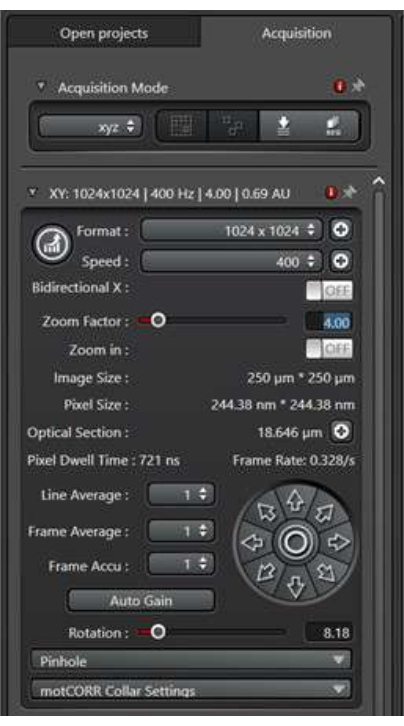
Figura 2: Il pannello della modalità di scansione della dimensione XY. Il pannello della modalità di scansione viene utilizzato per impostare le condizioni di scansione dell'immagine. Fare clic qui per visualizzare una versione ingrandita di questa figura.
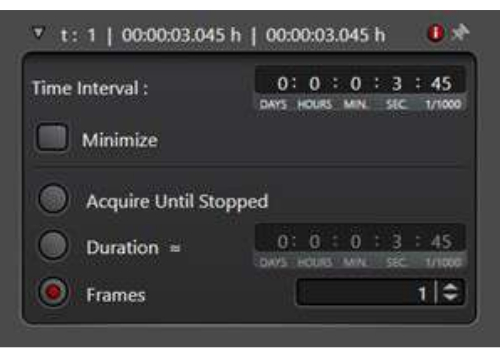
Figura 3: L'utilità Time Series in modalità di scansione xyt. L'utilità Time Series viene utilizzata per impostare le condizioni di imaging per raccogliere consecutivamente una serie di immagini. Fare clic qui per visualizzare una versione ingrandita di questa figura.
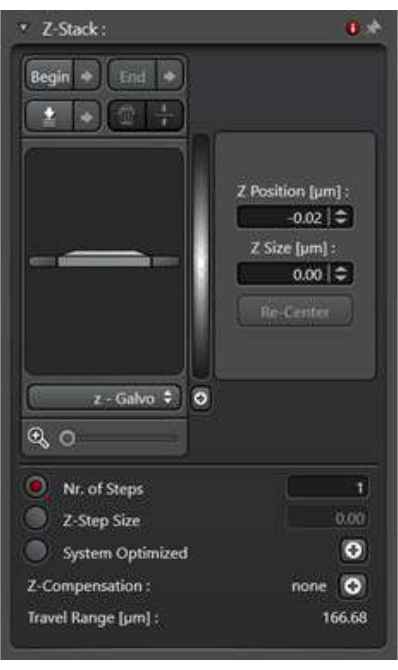
Figura 4: L'utilità z-stack in modalità di scansione xyz. L'utilità z-stack viene utilizzata per impostare le condizioni di imaging per raccogliere una serie di immagini sull'asse z. Fare clic qui per visualizzare una versione ingrandita di questa figura.
Risultati
Uno studio precedente ha indicato che ERL1 è una chinasi recettore attiva che subisce eventi di traffico dinamico di membrana20. ERL1 è una chinasi transmembrana del recettore LRR sulla membrana plasmatica. L'ERL1 appena sintetizzato nel reticolo endoplasmatico viene elaborato nei corpi del Golgi e ulteriormente trasportato alla membrana plasmatica. Le molecole ERL1 sulla membrana plasmatica possono percepire i ligandi EPF usando il loro dominio LRR extracellulare18. Dopo...
Discussione
Il sistema endomembrana separa il citoplasma di una cellula eucariotica in diversi compartimenti, che consente la funzione biologica specializzata di questi organelli. Per consegnare le proteine cargo e le macromolecole alla loro destinazione finale al momento giusto, numerose vescicole sono guidate per fare la spola tra questi organelli. Gli eventi di traffico di membrana altamente regolamentati svolgono un ruolo fondamentale nella vitalità, nello sviluppo e nella crescita delle cellule. Il meccanismo che regola questo...
Divulgazioni
Gli autori non dichiarano conflitti di interesse.
Riconoscimenti
Questo lavoro è stato supportato dalla National Science Foundation (IOS-2217757) (X.Q.) e dal Bronson Foundation Award (H.Z.) dell'Università dell'Arkansas per le scienze mediche (UAMS).
Materiali
| Name | Company | Catalog Number | Comments |
| 10 mL syringes | VWR | BD309695 | Vacuum samples |
| Brefeldin A (BFA) | Sigma | B7651 | membrane trafficking drug |
| Confocal Microscope | Leica | Lecia SP8 TCS with LAS-X software package | Imaging |
| Dissecting Forceps | VWR | 82027-402 | Genetic cross |
| Fiji | NIH | https://imagej.net/Fiji | Image processing |
| Leica LAS AF software | Leica | http://www.leica-microsystems.com | Image processing |
| transgenic seeds of ERL1-YFP | Qi, X. et al. The manifold actions of signaling peptides on subcellular dynamics of a receptor specify stomatal cell fate. Elife. 9, doi:10.7554/eLife.58097, (2020). | ||
| transgenic seeds of RFP-Ara7 | Ebine, K. et al. A membrane trafficking pathway regulated by the plant-specific RAB GTPase ARA6. Nat Cell Biol. 13 (7), 853-859, doi:10.1038/ncb2270, (2011). | ||
| Wortmannin (Wm) | Sigma | W1628 | membrane trafficking drug |
Riferimenti
- Aniento, F., Sanchez de Medina Hernandez, V., Dagdas, Y., Rojas-Pierce, M., Russinova, E. Molecular mechanisms of endomembrane trafficking in plants. Plant Cell. 34 (1), 146-173 (2022).
- Sigismund, S., et al. Endocytosis and signaling: Cell logistics shape the eukaryotic cell plan. Physiological Reviews. 92 (1), 273-366 (2012).
- Lyu, Z., Genereux, J. C. Methodologies for measuring protein trafficking across cellular membranes. ChemPlusChem. 86 (10), 1397-1415 (2021).
- Rodriguez-Furlan, C., Raikhel, N. V., Hicks, G. R. Merging roads: Chemical tools and cell biology to study unconventional protein secretion. Journal of Experimental Botany. 69 (1), 39-46 (2017).
- Foissner, I., Sommer, A., Hoeftberger, M., Hoepflinger, M. C., Absolonova, M. Is wortmannin-induced reorganization of the trans-Golgi network the key to explain charasome formation. Frontiers in Plant Science. 7, 756 (2016).
- Qi, X., Torii, K. U. Hormonal and environmental signals guiding stomatal development. BMC Biology. 16 (1), 21 (2018).
- Han, S. K., Kwak, J. M., Qi, X. Stomatal lineage control by developmental program and environmental cues. Frontiers in Plant Science. 12, 751852 (2021).
- Bharath, P., Gahir, S., Raghavendra, A. S. Abscisic acid-induced stomatal closure: An important component of plant defense against abiotic and biotic stress. Frontiers in Plant Science. 12, 615114 (2021).
- Becklin, K. M., Ward, J. K., Way, D. A. . Photosynthesis, Respiration, and Climate Change., 1st edition. , (2021).
- Yang, M., Sack, F. D. The too many mouths and four lips mutations affect stomatal production in Arabidopsis. Plant Cell. 7 (12), 2227-2239 (1995).
- Hara, K., Kajita, R., Torii, K. U., Bergmann, D. C., Kakimoto, T. The secretory peptide gene EPF1 enforces the stomatal one-cell-spacing rule. Genes & Development. 21 (14), 1720-1725 (2007).
- Hara, K., et al. Epidermal cell density is autoregulated via a secretory peptide, EPIDERMAL PATTERNING FACTOR 2 in Arabidopsis leaves. Plant & Cell Physiology. 50 (6), 1019-1031 (2009).
- Hunt, L., Gray, J. E. The signaling peptide EPF2 controls asymmetric cell divisions during stomatal development. Current Biology. 19 (10), 864-869 (2009).
- Sugano, S. S., et al. Stomagen positively regulates stomatal density in Arabidopsis. Nature. 463 (7278), 241-244 (2010).
- Kondo, T., et al. Stomatal density is controlled by a mesophyll-derived signaling molecule. Plant & Cell Physiology. 51 (1), 1-8 (2010).
- Hunt, L., Bailey, K. J., Gray, J. E. The signalling peptide EPFL9 is a positive regulator of stomatal development. New Phytologist. 186 (3), 609-614 (2010).
- Shpak, E. D., McAbee, J. M., Pillitteri, L. J., Torii, K. U. Stomatal patterning and differentiation by synergistic interactions of receptor kinases. Science. 309 (5732), 290-293 (2005).
- Lin, G., et al. A receptor-like protein acts as a specificity switch for the regulation of stomatal development. Genes & Development. 31 (9), 927-938 (2017).
- Lee, J. S., et al. Direct interaction of ligand-receptor pairs specifying stomatal patterning. Genes & Development. 26 (2), 126-136 (2012).
- Qi, X., et al. The manifold actions of signaling peptides on subcellular dynamics of a receptor specify stomatal cell fate. Elife. 9, e58097 (2020).
- MacAlister, C. A., Ohashi-Ito, K., Bergmann, D. C. Transcription factor control of asymmetric cell divisions that establish the stomatal lineage. Nature. 445 (7127), 537-540 (2007).
- Pillitteri, L. J., Sloan, D. B., Bogenschutz, N. L., Torii, K. U. Termination of asymmetric cell division and differentiation of stomata. Nature. 445 (7127), 501-505 (2007).
- Ohashi-Ito, K., Bergmann, D. C. Arabidopsis FAMA controls the final proliferation/differentiation switch during stomatal development. Plant Cell. 18 (10), 2493-2505 (2006).
- Kanaoka, M. M., et al. SCREAM/ICE1 and SCREAM2 specify three cell-state transitional steps leading to Arabidopsis stomatal differentiation. Plant Cell. 20 (7), 1775-1785 (2008).
- Bergmann, D. C., Lukowitz, W., Somerville, C. R. Stomatal development and pattern controlled by a MAPKK kinase. Science. 304 (5676), 1494-1497 (2004).
- Wang, H., Ngwenyama, N., Liu, Y., Walker, J. C., Zhang, S. Stomatal development and patterning are regulated by environmentally responsive mitogen-activated protein kinases in Arabidopsis. Plant Cell. 19 (1), 63-73 (2007).
- Ho, C. M., Paciorek, T., Abrash, E., Bergmann, D. C. Modulators of stomatal lineage signal transduction alter membrane contact sites and reveal specialization among ERECTA kinases. Developmental Cell. 38 (4), 345-357 (2016).
- Le, J., et al. Auxin transport and activity regulate stomatal patterning and development. Nature Communications. 5, 3090 (2014).
- Geldner, N., et al. The Arabidopsis GNOM ARF-GEF mediates endosomal recycling, auxin transport, and auxin-dependent plant growth. Cell. 112 (2), 219-230 (2003).
- Qi, X., et al. Autocrine regulation of stomatal differentiation potential by EPF1 and ERECTA-LIKE1 ligand-receptor signaling. Elife. 6, 24102 (2017).
- Heilemann, M., et al. Subdiffraction-resolution fluorescence imaging with conventional fluorescent probes. Angewandte Chemie. 47 (33), 6172-6176 (2008).
- Leighton, R. E., Alperstein, A. M., Frontiera, R. R. Label-free super-resolution imaging techniques. Annual Review of Analytical Chemistry. 15 (1), 37-55 (2022).
- Oreopoulos, J., Berman, R., Browne, M. Spinning-disk confocal microscopy: Present technology and future trends. Methods in Cell Biology. 123, 153-175 (2014).
- Gao, R., et al. Cortical column and whole-brain imaging with molecular contrast and nanoscale resolution. Science. 363 (6424), (2019).
- Nwaneshiudu, A., et al. Introduction to confocal microscopy. Journal of Investigative Dermatology. 132 (12), (2012).
- Sanderson, J. Multi-photon microscopy. Current Protocols. 3 (1), 634 (2023).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon