このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
肺体幹バンディングによる圧力過負荷誘発右心室肥大と失敗のマウスモデル
要約
肺体幹バンディングによって誘発される右心室圧過負荷のマウスモデルについて説明します。この論文には、挿管、手術、および心エコー検査による表現型の詳細なプロトコルが含まれています。挿管や手術にはカスタムメイドの器具が使用されるため、モデルを迅速かつ安価に再現することができます。
要約
圧力過負荷によって引き起こされる右心室(RV)不全は、多くの心血管疾患および肺疾患の罹患率および死亡率と強く関連しています。RV不全の病因は複雑で、まだ十分に理解されていません。RV不全の治療のための新しい治療戦略を特定するには、堅牢で再現性のある動物モデルが不可欠です。肺動脈幹バンディング (PTB) のモデルは、RV 機能が肺血管系の変化とは無関係に評価できるため、人気を博しています。
この論文では、5週齢のマウスでPTBによって誘発されるRV圧力過負荷のマウスモデルを紹介します。このモデルは、軽度のRV肥大から非代償性RVの故障まで、さまざまな程度のRVの病状を誘発するために使用できます。挿管、PTB手術、および心エコー検査による表現型の詳細なプロトコルが論文に含まれています。さらに、挿管やPTB手術のための器具のカスタマイズ手順も用意されており、PTBモデルを迅速かつ安価に再現することができます。
チタン製の結紮クリップを使用して肺動脈幹を収縮させ、再現性が高く、オペレーターに依存しない程度の肺動脈幹収縮を確保しました。PTB の重症度は、異なるインナーライゲーションクリップ径 (軽度: 450 μm および重度: 250 μm) を使用して等級付けしました。これにより、RV機能が保持された肥大から、心拍出量の減少と心臓外症状を伴う非代償性RV障害まで、RVの病状が生じました。RV機能は、手術後1週間と3週間後に心エコー検査によって評価されました。心エコー画像と結果の例を以下に示します。さらに、右心カテーテル法と心臓組織の組織学的分析の結果が示されています。
概要
右心室(RV)不全は、心不全の症状とRV機能障害に起因する全身鬱血の徴候を伴う臨床症候群です1。RV機能障害は、多くの心血管疾患および肺疾患2の罹患率および死亡率と強く関連しています。RV機能障害の病因は複雑であり、その根底にあるシグナル伝達経路と制御は十分に解明されていません。
現在の治療法からの観察によると、RV機能の改善は後負荷の減少と密接に関連しており、肺血管系が主要な治療目標であることが示唆されています3。このことは、現在の治療法がRV機能に直接的な影響を与えるのは最小限であり、肺血管抵抗の改善後も悪化する可能性があることを示しています3。そのため、後負荷低減とは無関係にRV機能を向上させるためのさらなる研究が大いに求められています。
堅牢で再現性のある動物モデルは、新しい治療薬の探索に不可欠です。慢性RV不全のほとんどのモデルでは、根本的な原因は肺血管系の構造変化によって引き起こされる肺高血圧症です4,5,6。十分に特徴付けられたモデルには、慢性低酸素モデル7,8、Sugen-hypoxiaモデル9,10,11、およびモノクロタリンモデル12,13が含まれます。これらのモデルでは、RVの失敗は肺高血圧症に続発するため、肺血管系への介入の影響をRV6への直接的な影響と区別することは不可能です。
肺血管系から独立してRVを研究するために、肺体幹バンディング(PTB)モデルが人気を博し、マウス、ラット、ウサギ、イヌ、ヒツジ、ブタを含むいくつかの動物種で記載されています6,14,15,16,17,18,19,20,21,22,23、24、25、26、27。PTBモデルでは、肺幹の狭窄は外科的に達成され、RV圧力6の増加を引き起こします。PTBの適用には、結紮糸または金属結紮クリップ18,28による血管の収縮を含む、さまざまなアプローチが存在する。結紮糸を使用するモデルでは、肺動脈幹が針に結び付けられ、針が引っ込められ、結紮糸が所定の位置に残ります。これにより、針のサイズと結び目18,29の張力に依存する血管の収縮が生じます。金属製の結紮クリップを採用しているモデルでは、肺体幹の収縮の程度がより再現性が高い場合があります。変更されたライゲーションクリップアプライヤーは、ライゲーションクリップを事前定義された一定の直径に閉じるために使用されます。これにより、この分析法はオペレーターに依存せず、疾患の表現型15,27,28におけるPTB関連の変動性が減少します。
マウスPTBモデルは、RV肥大と故障を誘発することが示されています18,28。PTBモデルを使用する際の大きな課題の1つは、RVの病理の望ましい程度を達成するために適切なPTB直径を選択することです。これは、非補償型RVの故障をモデル化しようとする場合に特に困難です。このためには、収縮は、急性RV不全や手術直後の死亡につながることなく、慢性RV不全を誘発するのに十分なほどきつくなければなりません6。この課題を解決するための1つのアプローチは、離乳期または幼体を使用することです6,15。PTBモデルは、Wistarラット離乳子15,30を使用してRV故障のさまざまな段階を研究するために成功裏に使用されています。これを達成するために、成長可能性が残っている幼若ラットは、チタンライゲーティングクリップを適用してPTB手術を受けました。ラットが成長すると、肺狭窄は徐々に重症化し、PTB15,30の重症度に応じてRV肥大または慢性RV不全を引き起こしました。このモデルに触発されて、私たちは、幼若マウスを使用したマウスPTBモデルでRV病理のさまざまな段階を生成できるという仮説を立てました。軽度から重篤な疾患までの幅広いRV病理を研究することは、疾患の進行とRV肥大からRV不全への移行についての理解を解明するのに役立つ可能性があります。
ここでは、PTBによって誘発されるRVの圧力過負荷のマウスモデルを若年マウスで紹介します。このモデルでは、RV肥大から非代償性RV障害まで、さまざまな程度のRV病理を生成することができます。この研究には、挿管、PTB 手術、および心エコー検査による表現型に関する詳細なプロトコルが含まれています。
プロトコル
本試験は、デンマーク動物実験検査局(承認番号:2021-15-0201-00928)によって承認され、国家実験動物法に従って実施されました。この研究では、5週齢の雄C57BL/6Nマウスを使用しました。
1. 挿管・手術用器具のカスタマイズ(図1)
注:このセクションでは、挿管およびPTB手術用のカスタムメイド器具を安価で容易に入手できる材料から準備する際の最も重要な手順について詳しく説明します。
- 気管内チューブを準備します(図1A)。
一般的な静脈内(IV)カテーテルは、マウスの挿管と換気に使用できます。- マウスのサイズに対応する適切なサイズの血管内カテーテルを選択してください。5週齢のマウスには22Gカテーテル(17-20g)、大型マウスには23Gカテーテル(>20g)が推奨されます。
- 針を引き出し、ロック機構を取り外します。針をカテーテルに戻し、針の先端をカテーテルの先端から約2mmのところに45°の角度で切断します。
- マウスの声帯の損傷を防ぐために、サンドペーパーを使用して先端を鈍くします。
- 挿管中の視界を良くするために、カテーテルの片方の翼を切り取ります。
- 胸部リトラクターを準備します(図1B)。
- ニードルホルダーを使用して、中央にある約10cmの柔軟な金属線を30°の角度で曲げます。
- ニードルホルダーを使用して、ワイヤーの両端に幅5mmの非外傷性フックを慎重に作成します。
- 挿管スタンドを準備します(図1C)。
注:挿管スタンドを使用すると、挿管中に鼻管を介して麻酔を連続的に送達できます。これにより、目視による指導の下での制御された安全な挿管が可能になり、声帯や気管の損傷のリスク、食道へのチューブの誤配置のリスクが軽減されます。挿管スタンドのフレームとして、金属製またはプラスチック製のフレームを使用することができます。この研究では、わずかに曲がったキッチンロールホルダーを使用しました。- マウスの鼻にフィットする3cmのゴムチューブをカットし、IVカテーテルバルブに接続します。吸入麻酔は、挿管前にバルブを介して接続することができます。
- チューブの開口部から約5mmのところに1-0編組縫合糸を使用してループを作ります。これは、マウスの鼻をチューブに固定するために使用されます。
- 柔軟なプラスチックシートの上部近くに穴を開け、その穴にチューブを置きます。このシートは、挿管スタンドでマウスを支えるために使用されます。
- 図 1C に示すように、テープを使用して個々のパーツを一緒に保持します。
- ガイダンスカニューレを準備します(図1D、E)。
- 6-0モノフィラメント縫合糸を鈍い27Gカニューレに通し、縫合糸に結び目を作ります。この結び目は、後でPTB手術中に縫合糸をつかむために使用します。
- ニードルホルダーを使用して、カニューレの先端を80°の角度に曲げます。
- ライゲーティングクリップアプライヤーを準備します。
注意: 角度のある顎を備えた結紮クリップアプライヤーは、調整可能な停止機構(図1F)で変更され、顎が互いに正確に所定の距離にあるときに結紮クリップの圧縮が停止します。改質された結紮クリップアプライヤーは、肺動脈幹にチタン製の結紮クリップを適用するために使用されます。- カスタムカットした真ちゅう製の部品を、2本のネジでライゲーティングクリップアプライヤーのハンドルに固定します。中央に調整可能なネジ(図1F、白い矢印)を取り付けて、ライゲーティングクリップアプライヤーの圧縮ハンドル間の正確な距離を決定します。これはジョー間の正確な距離に対応します。

図1:挿管およびPTB手術用の器具 (A)IVカテーテルから作られた気管内チューブ。(B)胸部リトラクター。(C)挿管スタンドと挿管スタンドに置かれたマウスが鼻管で麻酔を受けます。(D)PTB手術に使用される手術器具および改造された結紮クリップアプライヤー。(E)ガイダンスカニューレ。(F)カスタムメイドの調整可能なストップメカニズム。 この図の拡大版を表示するには、ここをクリックしてください。
2.ライゲーションクリップアプライヤーの調整
- ライゲーションクリップの内径は、RVの故障の望ましい重大度に基づいて選択します。5週齢の雄C57BL/6Nマウス(17-20g)の場合、重度の場合は250μm、軽度のRV圧力過負荷の場合は450μmのクリップ径を使用します。中間のクリップ直径を使用して、適度な圧力過負荷を誘発します。
- 金属線または針を使用して、ライゲーションクリップアプライヤーを調整します。ワイヤの直径が目的のクリップ直径に対応していることを確認します。
- クリップアプライヤーにライゲーティングクリップをロードし、調整ワイヤーをライゲーティングクリップの中央に配置します。クリップアプライヤーを圧縮しながら、クリップのジョーがワイヤーの周りにしっかりと収まるまでネジを回します。クリップアプライヤーを離したら、クリップが調整ワイヤーの所定の位置に留まっていることを確認します。
- クリップアプライヤを調整した状態で、調整ワイヤに別のライゲーションクリップを配置して、設定された直径を確認します。
3. 手術の準備
- 0.6 L/分 100% 酸素中に 7% セボフルランを使用して、導入チャンバーで麻酔を誘発します。挿管前につま先をつまんで十分な麻酔を確認してください。
注:イソフルランも使用できます。異なる濃度を使用する必要があることに注意してください。 - マウスに22G IVカテーテルを挿管します。手術用顕微鏡と挿管スタンドを使用して目視による指導の下で挿管を行い、声帯の視覚化と鼻管への吸入麻酔薬の継続的な送達のための適切な位置合わせを可能にします(図1C)。
- マウスを175ストローク/分、一回換気量300μL/ストロークで換気します。
注:8〜10μL / gの潮汐量も推奨され、理想的な一回換気量は、換気システムの漏れやデッドスペースの可能性によって異なります。 - 挿管したマウスをカバー付きの加熱パッド(37°C)に置き、マウスの目に保湿軟 ?? を塗ります。.
- 麻酔を維持し(0.6 L / min 100%酸素中に3.5%セボフルラン)、周術期鎮痛のために0.1 mg / kgブプレノルフィンと5 mg / kgカルプロフェンを皮下投与します。.脱毛クリームを使用して胸部からすべての髪を取り除き、消毒用ワイプで皮膚を消毒します。
4. PTB手術
- 胸骨角から左前腋窩線まで、第2肋間腔の上の皮膚に10mmの切開を行います。鈍的解剖により、大胸筋と小胸筋を分割します。
- 第2肋間腔の肋間筋を切断し、胸腺を鈍く解剖して心臓、肺幹、大動脈を露出させます。胸部リトラクターを肋間腔に配置して、手術野にアクセスできるようにします。
注:肋間筋を切断するときは、左内乳動脈が胸骨の横方向にわずか1〜2 mm走っているため、細心の注意を払う必要があります。この動脈が損傷すると、重大な失血を引き起こす可能性があります。 - 顕微鏡の鉗子を使用して血管間の結合組織を鈍く取り除くことにより、上行大動脈から肺幹を分離します。マウスの下半身を回転させることにより、肺幹の露出をさらに改善します(左脚を右脚の上に)。
- 誘導カニューレを肺幹の後方の横心膜洞に通します。鉗子を使用してガイダンスカニューレの先端にある結び目をつかみ、ガイダンスカニューレを通して縫合糸を引っ張ります。縫合糸が肺幹の周りの所定の位置に留まった状態で、ガイダンスカニューレを慎重に取り外します。
- 結紮クリップアプライヤをロードし、縫合糸を使用して肺幹を結紮クリップの顎に導き、クリップを圧縮します。クリップを装着した直後に縫合糸を放し、肺動脈幹の充填を観察します。
注:徐脈は、結紮クリップの適用後最初の数秒で観察される場合があります。. - 6-0モノフィラメント吸収性縫合糸を第2肋骨と第3肋骨の周囲に配置し、肋間腔を閉じます。縫合糸を引き締めながら胸部に穏やかな圧力をかけることにより、胸腔からできるだけ多くの空気を排出します。
- 最後に、6-0モノフィラメント吸収性縫合糸で皮膚を縫合します。
- 偽手術中に、ライゲーティングクリップの配置(ステップ4.5)を除いて、同じ手順を実行します。
5. 心エコー検査
- 導入室で麻酔を導入した後(1〜2分、100%酸素中6%セボフルラン)、鼻管(100%酸素中3.5%セボフルラン)を使用して麻酔を維持します。脱毛クリームを使用して胸と腹部からすべての髪を取り除き、マウスを加熱パッドの上に置きます。保湿軟膏を目に、超音波ジェルをマウスの胸部に塗布します。
注意: 2Dゲイン、フォーカス深度、および画像の深度を調整して、すべての心エコー測定で画質を向上させます。 - 超音波プローブを調整して、胸骨傍長軸(PLAX)ビューを見つけます(図2)。PLAX で、肺幹の肺幹内径と肺幹の速度時間積分 (VTI) を測定します。
- Bモードを選択し、加熱パッドをX軸、Y軸、Z軸に慎重に動かして、画像の中央にある肺幹を特定します。色を使用して、最大の肺幹の直径を特定します。シネストアを使用して、肺幹の直径を測定するためのシーケンスをキャプチャします。
- カラーとパルス波(PW)ドップラーを選択し、カーソルを肺幹の中央に置きます。点線が血管内の血流と平行になるまでPW角度を調整します。
- シネストアを押してVTIを測定します。カーソルを肺幹の両壁の近くに置き、シネストアを再度押して、血管壁の近くの流れを取得します。
注:右心室(RV)の内径とRVフリー壁の厚さもPLAXビューで評価できます。
- 胸骨傍短軸(PSAX)ビュー(図3)を見つけて、左心室(LV)の内径を測定し、中隔の膨らみ(D構成)を評価するために使用できます。
- Bモードを選択し、プローブを反時計回りに90°回します。胸骨によるRVの影を避けるためにプローブを横方向に20〜30度傾け、左心室ができるだけ丸くなるまでプローブを頭蓋方向に20〜30度傾けます。次に、プローブを頭蓋尾方向にスライドさせて、心室直径が最大の乳頭筋のレベルを特定し、シネストアを押します。
注:中乳頭レベルのPSAXは、RVフラクショナルエリアの変化を評価するためにも使用できます。大動脈弁のレベルでPSAXはRVのフラクショナル短縮またはRVの自由な壁厚さを測定するのに使用することができます。
- Bモードを選択し、プローブを反時計回りに90°回します。胸骨によるRVの影を避けるためにプローブを横方向に20〜30度傾け、左心室ができるだけ丸くなるまでプローブを頭蓋方向に20〜30度傾けます。次に、プローブを頭蓋尾方向にスライドさせて、心室直径が最大の乳頭筋のレベルを特定し、シネストアを押します。
- 頂端 4 チャンバー (A4CH) ビュー (図 4) を使用して、三尖弁環状平面収縮期エクスカーション (TAPSE) を測定し、三尖弁逆流を評価します。
- 図4に示すようにプローブを配置します。心臓が特定されたら、手首と指だけを使用してプローブを微調整し、心臓と三尖弁の4つの心室すべてを特定します。
- 良好なA4CHビューを特定して維持することは困難です。安定性のために、プローブを操作する手を加熱パッドに置きます。適切な画像が見つかるまで、プローブをスライドさせ、傾け、少し回します。
- プローブは一度に1次元だけ動かします:たとえば、頭蓋尾筋をスライドさせて心臓を見つけ、次にプローブを傾けて4つのチャンバーすべてを特定し、最後に4つのチャンバーと三尖弁がすべてフレームに入るまでプローブを回転させます。必要に応じて、3つの手順すべてを数回繰り返してから、理想的な画像を取得します。
- 三尖弁が特定されたら、 Mモード を選択し、自由壁の三尖弁輪に点線を配置します。 cine store を押して、測定値を保存します。
- 三尖弁の逆流を評価する ための色 を選択します。逆流が存在する場合、収縮期にはRVから右心房(RA)への逆行性の流れのジェットが見られます(図5)。
注:A4CHビューでは、RVフリーウォールの組織ドップラーとRV流入速度も測定できます。
- 図4に示すようにプローブを配置します。心臓が特定されたら、手首と指だけを使用してプローブを微調整し、心臓と三尖弁の4つの心室すべてを特定します。
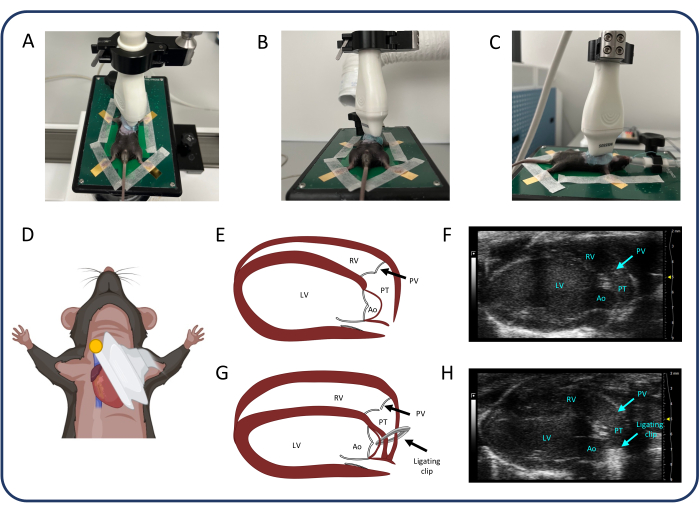
図2:傍胸骨長軸図(PLAX)(A-D)超音波プローブの位置。(E, F) PLAXの正常なマウスの心臓。(G、H)PTB後のRV拡張と肥大。略語:LV:左心室、RV:右心室、PV:肺動脈弁、PT:肺幹、Ao:大動脈。この図の拡大版を表示するには、ここをクリックしてください。
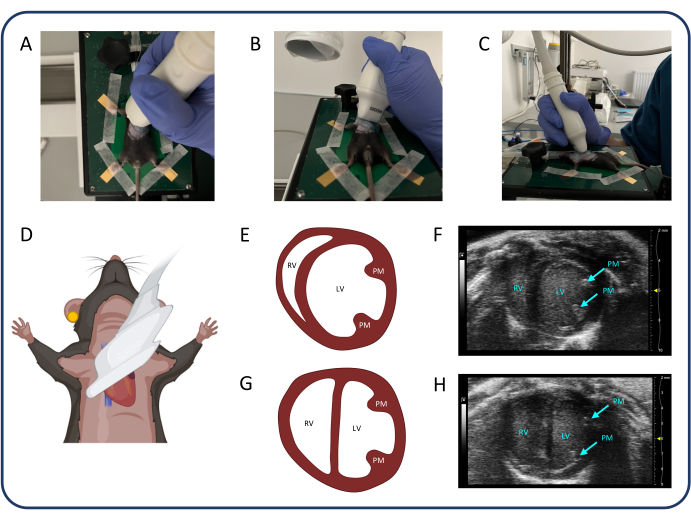
図3:胸骨傍短軸図(PSAX)(A-D)超音波プローブの位置。(E、F)PSAXの正常なマウスの心臓。(G、H)PTB後のPSAX。略語:LV:左心室、RV:右心室、PM:乳頭筋。この図の拡大版を表示するには、ここをクリックしてください。
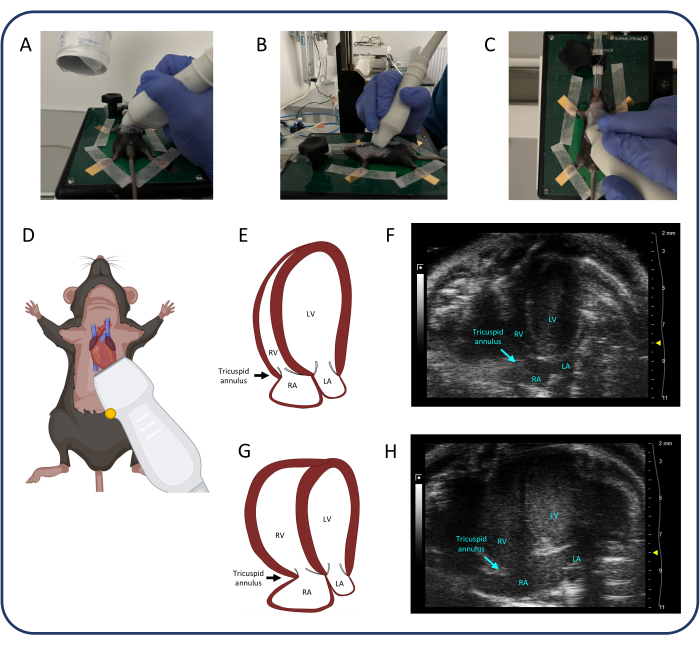
図4:頂端4チャンバービュー(A4CH)(A-D)超音波プローブの位置。(E, F) A4CHビューの正常なマウスの心臓。(G、H)PTB 後の RV および RA 拡張。略語:LV:左心室、RV:右心室、RA:右心房、LA:左心房。この図の拡大版を表示するには、ここをクリックしてください。
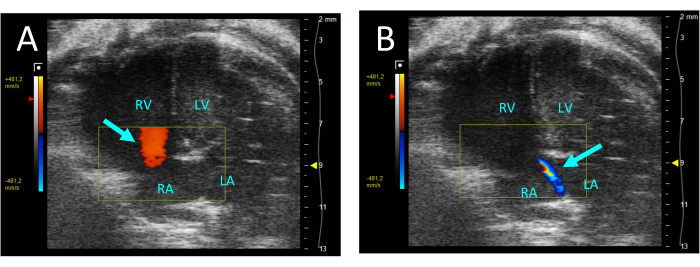
図5:A4CHビューのカラードップラーで可視化された三尖弁逆流 (A)拡張期では、RAからRVへの流れが観察されます(矢印)。(B)収縮期には、RVからRAへの細い流れが見えます(矢印)。略語:LV:左心室、RV:右心室、RA:右心房、LA:左心房。 この図の拡大版を表示するには、ここをクリックしてください。
6. データ分析
- PLAX で 3 つの心周期で肺幹の直径を測定し、平均肺の体幹の直径をさらなるデータ分析に使用します。PLAX で 3 つの心周期の VTI を、保存された 3 つのシネ ループ (肺幹の中心と血管壁の近く) のそれぞれで測定します。すべてのVTI測定値の平均VTIを使用して、さらに分析します。次の式を使用して CO を計算します。
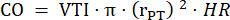
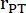 :肺動脈幹の半径、HR:心拍数
:肺動脈幹の半径、HR:心拍数 - PSAXのLVEIを中乳頭レベルで測定します。測定ツールを使用して、中隔から自由壁までの最大のLV内径(LVid1)を測定します。次に、最初の測定値(LVid2)に直交するLV内径を測定します。これらの測定を 3 回の心周期で繰り返し、平均 LV 内径と次の式を使用して LVEI を計算します。
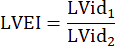
- A4CHビューで3つの心周期でTAPSEを測定し、さらなるデータ分析に平均TAPSEを使用します。
7. 右心カテーテル法
- PTB手術の3週間後に1.4Fマイクロチップカテーテルを使用した右心臓カテーテル法により、右心室(RV)の圧力と体積を測定します。
- ステップ3.1〜3.4で説明されているように、マウスに麻酔をかけ、挿管します。マウスをカバー付きの加熱パッド(37°C)に置き、麻酔を維持します(0.6 L / min、100%酸素中3.5%セボフルラン)。
- 2000 IUのヘパリン(筋肉内[i.m.])と0.5 mLのNaCl(皮下[s.c.])を投与します。.
- 外科用ハサミを使用して、剣状突起のすぐ尾側に腹壁を切断し、胸壁の切開部に沿って横隔膜を慎重に切断することにより、胸腔にアクセスします。心臓への十分なアクセスが得られるまで、横隔膜と肋骨を切断します。.
- 下大静脈の周りに結紮糸を置きます。これを使用して容器を閉塞し、プロトコルの後半で圧力体積測定を記録するための予圧を軽減します。
- 26Gの針を使用して、RVに小さな穴を慎重に突き刺し、これができるだけ頂点に近く、針が心室を完全に貫通するのではなく、コンダクタンスカテーテルを挿入するためのガイドとして機能することを確認します。出血が発生した場合は、出血を最小限に抑えるために、小さな綿棒で穏やかな圧力をかけます。
- 心室壁の小さな穴を特定し、組織を貫通してカテーテルを挿入します。
注意: カテーテルを挿入するときは、心室内壁を傷つけないように注意してください。 - 右心室圧(RVP)の変化は、カテーテル挿入後数分間観察されることがよくあります。RVPが安定するまで待ってから、代表的な定常状態の測定値を取得します。
- 圧力-体積ループを取得するには、以前に下大静脈の周りに配置した結紮糸を使用します。結紮糸を慎重に引っ張って血管を閉塞し、予圧を徐々に減らします。
- 代表的な圧力-体積ループが記録されたら、カテーテルを抜出し、心臓を切除してマウスを安楽死させます。このとき、さらなる分析のために血液と組織のサンプルを採取します。
結果
C57BL/6Nマウス(雄、5週齢、17-20g)を重症PTB(sPTB、250μm、n=12)、軽度PTB(mPTB、450μm、n=9)、偽手術(sham、n=15)のいずれかに無作為に割り付けた。心機能の評価は、手術の1週間後と3週間後に心エコー検査によって行われました。右心カテーテル法とその後の安楽死は、術後3週間で行われました。臓器の重量を量り、組織学的分析のために心臓組織を調製しました。
手術の1週間後の...
ディスカッション
この論文では、圧力過負荷によるRV肥大と故障のマウスモデルを紹介します。(i) 幼若マウスの PTB は、軽度の RV 肥大から、代償不全の心臓外徴候を伴う RV 障害や組織学的に確認された RV 線維症まで、さまざまな程度の RV 病理を誘発する可能性があります。(ii) RV 機能障害の兆候は、PTB 手術の 1 週間後と 3 週間後に心エコー検査によって観察および定量化できます。(iii)RV肥大の程度は、PTBの...
開示事項
著者は何も開示していません。
謝辞
この研究は、Snedkermester Sophus Jacobsen og Hustru Astrid Jacobsens Fond、Helge Peetz og Verner Peetz og hustru Vilma Peetz Legat、Grosserer A.V. Lykfeldt og Hustrus Legatの支援を受けました。さらに、著者らは、オーフス大学臨床医学科の動物施設のスタッフが実験作業の実行中にサポートしてくれたことに感謝したいと思います。
資料
| Name | Company | Catalog Number | Comments |
| Biosyn 6-0, monofilament, absorbable suture | Covidien | UM-986 | |
| Blunt cannula, 27G 0.4x0.25, | Sterican | 292832 | |
| Bupaq Multidose vet 0,3 mg/ml (Buprenorphinum) | Salfarm Danmark | VNR 472318 | |
| C57BL/6NTac mice | Taconic Biosciences | C57BL/6NTac | |
| Dagrofil 1, braided, non-absorbable suture | B Braun | C0842273 | |
| Depilatory cream | Veet | 3132000 | |
| Disinfection Swabs (82% Ethanol + 0.5% Chlorhexidine) | Mediq | 3340122 | |
| Disposable scalpels, size 11 | Swann-Morton | 11708353 | |
| Dräger Vapor 2000 Sevoflurane | Dräger | M35054 | |
| Eye oinment neutral, "Ophta" | Actavis | MTnr.: 07586 Vnr: 53 96 68 | |
| Horizon ligating clips | Teleflex Medical | 5200 (IPN914931) | |
| Horizon Open Ligating Clips applier, curved, 6" (15 cm) | Teleflex Medical | 537061 | |
| Kitchen roll holder | n.a. | n.a. | |
| Metal wire of different thickness | n.a. | n.a. | |
| Microsurgical instruments set | Thompson | n.a. | |
| MiniVent Ventilator | Hugo Sachs | Type 845 | |
| MS505S transducer | Visual sonics | n.a. | |
| Rimadyl Bovis vet. 50 mg/ml (Carprofen) | Zoetis | MTnr: 34547, Vnr: 10 27 99, | |
| Sevoflurane Baxter 100 % | Baxter Medical | MTnr: 35015 | |
| Silicone tubing | n.a. | n.a. | |
| Soft plastic sheet | n.a. | n.a. | |
| Stereomicroscope, "Opmi Pico" | Carl Zeiss Surgicals GmbH | n.a. | |
| Ultrasonic probe holder/rail | Visual Sonics | 11277 | |
| Varming plate | Visual sonics | 11437 | |
| Venflon ProSafety, 22G, 0,9 x 25mm | Becton Dickinson | 393222 |
参考文献
- Voelkel, N. F., et al. Right ventricular function and failure: Report of a national heart, lung, and blood institute working group on cellular and molecular mechanisms of right heart failure. Circulation. 114 (17), 1883-1891 (2006).
- Haddad, F., Doyle, R., Murphy, D. J., Hunt, S. A. Right ventricular function in cardiovascular disease, part ii: Pathophysiology, clinical importance, and management of right ventricular failure. Circulation. 117 (13), 1717-1731 (2008).
- Van De Veerdonk, M. C., et al. Progressive right ventricular dysfunction in patients with pulmonary arterial hypertension responding to therapy. J Am Coll Cardiol. 58 (24), 2511-2519 (2011).
- Gomez-Arroyo, J., et al. A brief overview of mouse models of pulmonary arterial hypertension: Problems and prospects. Am J Physiol Lung Cell Mol Physiol. 302 (10), L977-L991 (2012).
- Maarman, G., Lecour, S., Butrous, G., Thienemann, F., Sliwa, K. A comprehensive review: The evolution of animal models in pulmonary hypertension research; are we there yet. Pulm Circ. 3 (4), 739-756 (2013).
- Andersen, A., et al. Animal models of right heart failure. Cardiovasc Diagn Ther. 10 (5), 1561-1579 (2020).
- Voelkel, N. F., Tuder, R. M. Hypoxia-induced pulmonary vascular remodeling: A model for what human disease. J Clin Invest. 106 (6), 733-738 (2000).
- Rabinovitch, M., Gamble, W., Nadas, A. S., Miettinen, O. S., Reid, L. Rat pulmonary circulation after chronic hypoxia: Hemodynamic and structural features. Am J Physiol. 236 (6), H818-H827 (1979).
- Taraseviciene-Stewart, L., et al. Inhibition of the VEGF receptor 2 combined with chronic hypoxia causes cell death-dependent pulmonary endothelial cell proliferation and severe pulmonary hypertension. Faseb j. 15 (2), 427-438 (2001).
- Ciuclan, L., et al. A novel murine model of severe pulmonary arterial hypertension. Am J Respir Crit Care Med. 184 (10), 1171-1182 (2011).
- Nicolls, M. R., et al. New models of pulmonary hypertension based on VEGF receptor blockade-induced endothelial cell apoptosis. Pulm Circ. 2 (4), 434-442 (2012).
- Hessel, M. H., Steendijk, P., Den Adel, B., Schutte, C. I., Van Der Laarse, A. Characterization of right ventricular function after monocrotaline-induced pulmonary hypertension in the intact rat. Am J Physiol Heart Circ Physiol. 291 (5), H2424-H2430 (2006).
- Gomez-Arroyo, J. G., et al. The monocrotaline model of pulmonary hypertension in perspective. Am J Physiol Lung Cell Mol Physiol. 302 (4), L363-L369 (2012).
- Janssen, W., et al. 5-ht2b receptor antagonists inhibit fibrosis and protect from RV heart failure. Biomed Res Int. 2015, 438403 (2015).
- Andersen, S., et al. A pulmonary trunk banding model of pressure overload induced right ventricular hypertrophy and failure. J Vis Exp. (141), e58050 (2018).
- Axelsen, J. B., et al. Effects of 6-mercaptopurine in pressure overload induced right heart failure. PLoS One. 14 (11), e0225122 (2019).
- Egemnazarov, B., et al. Pressure overload creates right ventricular diastolic dysfunction in a mouse model: Assessment by echocardiography. J Am Soc Echocardiogr. 28 (7), 828-843 (2015).
- Wang, Q., et al. Induction of right ventricular failure by pulmonary artery constriction and evaluation of right ventricular function in mice. J Vis Exp. (147), e59431 (2019).
- Kojonazarov, B., et al. The peroxisome proliferator-activated receptor β/δ agonist gw0742 has direct protective effects on right heart hypertrophy. Pulm Circ. 3 (4), 926-935 (2013).
- Kojonazarov, B., et al. P38 MAPK inhibition improves heart function in pressure-loaded right ventricular hypertrophy. Am J Respir Cell Mol Biol. 57 (5), 603-614 (2017).
- Rai, N., et al. Effect of Riociguat and Sildenafil on right heart remodeling and function in pressure overload induced model of pulmonary arterial banding. Biomed Res Int. 2018, 3293584 (2018).
- Sydykov, A., et al. Genetic deficiency and pharmacological stabilization of mast cells ameliorate pressure overload-induced maladaptive right ventricular remodeling in mice. Int J Mol Sci. 21 (23), 9099 (2020).
- Andersen, S., et al. Effects of combined angiotensin ii receptor antagonism and neprilysin inhibition in experimental pulmonary hypertension and right ventricular failure. Int J Cardiol. 293, 203-210 (2019).
- Andersen, S., et al. Pressure overload induced right ventricular remodeling is not attenuated by the anti-fibrotic agent pirfenidone. Pulm Circ. 9 (2), 2045894019848659 (2019).
- Labazi, H., et al. Sex-dependent changes in right ventricular gene expression in response to pressure overload in a rat model of pulmonary trunk banding. Biomedicines. 8 (10), 430 (2020).
- Sun, X. Q., et al. Increased mao-a activity promotes progression of pulmonary arterial hypertension. Am J Respir Cell Mol Biol. 64 (3), 331-343 (2021).
- Axelsen, J. S., et al. Effects of Empagliflozin on right ventricular adaptation to pressure overload. Front Cardiovasc Med. 10, 1302265 (2023).
- Mamazhakypov, A., Veith, C., Schermuly, R. T., Sydykov, A. Surgical protocol for pulmonary artery banding in mice to generate a model of pressure-overload-induced right ventricular failure. STAR Protoc. 4 (4), 102660 (2023).
- Boehm, M., et al. Delineating the molecular and histological events that govern right ventricular recovery using a novel mouse model of pulmonary artery de-banding. Cardiovasc Res. 116 (10), 1700-1709 (2020).
- Andersen, S., et al. Effects of bisoprolol and losartan treatment in the hypertrophic and failing right heart. J Card Fail. 20 (11), 864-873 (2014).
- Hirata, M., et al. Novel model of pulmonary artery banding leading to right heart failure in rats. Biomed Res Int. 2015, 753210 (2015).
- Vildbrad, M. D., et al. Limitations and pitfalls in measurements of right ventricular stroke volume in an animal model of right heart failure. Physiol Meas. 36 (5), 925-937 (2015).
- Boehm, M., et al. Maintained right ventricular pressure overload induces ventricular-arterial decoupling in mice. Exp Physiol. 102 (2), 180-189 (2017).
- Cheng, H. W., et al. Assessment of right ventricular structure and function in mouse model of pulmonary artery constriction by transthoracic echocardiography. J Vis Exp. (84), e51041 (2014).
- Luitel, H., et al. Pressure overload leads to an increased accumulation and activity of mast cells in the right ventricle. Physiol Rep. 5 (6), e13146 (2017).
- Mamazhakypov, A., et al. Novel therapeutic targets for the treatment of right ventricular remodeling: Insights from the pulmonary artery banding model. Int J Environ Res Public Health. 18 (16), 8297 (2021).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved