JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
산화아연 나노입자의 제조 및 항균 효과 평가
* 이 저자들은 동등하게 기여했습니다
요약
이 연구에서는 산화아연 나노입자를 침전방법을 사용하여 합성하였다. 합성된 입자의 항균 효과는 다제내성 메티실린 내성 황색포도상구균 (MRSA) 및 녹농 균 균주에 대해 테스트되었습니다.
초록
병원내 세균 감염은 항생제에 대한 내재적 내성으로 인해 점점 더 어려워지고 있습니다. 병원에서 다제내성 세균주의 출현은 항생제의 광범위하고 다양한 사용에 기인하며, 이는 항생제 내성 문제를 더욱 악화시키고 있습니다. 금속 나노 물질은 항생제 내성 박테리아 세포를 근절하기 위한 대체 솔루션으로 널리 연구되어 왔습니다. 금속 나노 입자는 항균 이온의 방출, 활성 산소 종의 생성 또는 박테리아가 저항력을 발달시킬 수 없는 물리적 파괴와 같은 다양한 메커니즘을 통해 박테리아 세포를 공격합니다. 활발히 연구되고 있는 항균 금속 나노입자 중 FDA 승인을 받은 산화아연 나노입자는 생체 적합성 및 항균 특성으로 알려져 있습니다. 본 연구에서는 산화아연 나노입자를 합성하기 위한 침전 방법을 성공적으로 개발하고, 이러한 나노입자의 특성을 분석하고, 항균 시험을 수행하는 데 중점을 두었습니다. 산화아연 나노입자는 투과 전자 현미경(TEM), 동적 광 산란(DLS), 자외선/가시광선 분광법 및 X선 회절(XRD)을 사용하여 특성화되었습니다. 항균 검사는 메티실린 내성 황색포도상구균 (MRSA) 및 녹농균(Pseudomonas aeruginosa)의 다제내성 균주를 대상으로 육수 미세희석 검사를 사용하여 수행되었습니다. 이 연구는 항생제 내성 박테리아의 증식을 억제하는 산화아연 나노입자의 잠재력을 입증했습니다.
서문
다제내성(MDR) 세균 감염은 전 세계적으로 인간의 건강에 심각한 위협이 되고 있습니다1. 이러한 감염은 기저 질환이 있는 환자에게 치명적일 수 있기 때문에 이 문제를 해결하기 위한 연구가 활발히 진행되고 있습니다2. 박테리아는 다양한 약물의 작용을 회피하도록 진화해 왔습니다. 전 세계적으로 수백만 명의 생명을 구한 것으로 널리 알려지고 인정받는 페니실린은 박테리아 세포벽의 합성을 억제하는 β락탐 항생제이다3. 그러나 박테리아는 유출 펌프, 트랜스펩티다아제 변형 또는 투과성 감소와 같은 다양한 메커니즘을 통해 약물의 효능을 중화하도록 진화해 왔다4. 또한, 세균세포는 이러한 저항성 유전자를 다음 세대로 전달할 수 있어 다음 세대의 생존율을 높이고 저항성 균주의 문제를 강화할 수 있다5.
항생제 내성 세균의 증가는 일반적으로 여러 항생제에 내성을 보이는 MDR 세균의 출현으로 이어졌습니다. MDR 균주는 여러 박테리아 균주가 다양한 항생제에 노출되어 결과적으로 다양한 항생제에 대한 내성이 생기는 병원 환경에서 가장 빈번하게 발생한다6. 황색포도상구균, 특히 메티실린 내성 황색포도상구균(MRSA)은 인간의 약 30%의 피부에 군집을 형성하는 그람 양성 공생 박테리아입니다 7,8. 1960년대에 처음 발견된 MRSA는 β-락탐 항생제에 대한 민감성이 감소하여 1990년대 이후 감염률이 급격히 증가하고 있다9. 그람 음성 박테리아 중 녹농균(P. aeruginosa)은 병원에서 획득하는 가장 흔한 균주 중 하나입니다. 이 종은 통성 막대 모양의 박테리아로 인간에게 기회 감염을 일으킨다10. 특히, 인체 건강에 직접적인 영향을 미치는 MDR 균주는 의료 관련 감염의 50% 이상을 차지한다11. 이 연구에서는 병원에서 가장 흔하게 발견되는 다제내성 균주인 MRSA와 녹농균(P. aeruginosa)을 활용했습니다.
항생제 내성 문제를 해결하기 위해 항균 목적으로 나노 입자(NP)를 사용하는 것이 광범위하게 조사되었습니다. 특히 금속 NP는 다양한 메커니즘을 통해 박테리아 세포 사멸을 유도하여 약물 내성 문제에 대한 잠재적인 해결책을 제공합니다. 금속 NP는 항균 이온의 방출, 활성산소종(ROS)의 생성, 세포의 물리적 파괴 등 여러 메커니즘을 통해 항균 활성을 발휘합니다12. 은, 구리, 산화아연(ZnO) 및 산화티타늄으로 구성된 NP는 높은 항균 효능을 가지고 있어 활발히 연구되고 있습니다13.
ZnO NP는 미국 식품의약국(FDA)의 인체 사용 승인을 받았습니다. 반대로, 높은 항균 효능에도 불구하고 인체에 대한 은 및 구리 NP의 사용은 높은 세포 독성으로 인해 제한됩니다. 그러나, ZnO NPs는 일상 생활에서 흔히 발견되며, 널리 사용되는 자외선 차단제 제제에도 존재한다14. 주목할 점은, ZnO NP에서 방출되는 Zn2+ 이온은 세균 처리에 매우 효과적이며, ROS 및 기타 물리적 손상 메커니즘의 생성을 통해 세균 세포 사멸을 유도한다15.
이 연구는 침전 방법을 사용하여 ZnO 나노 입자(NP)를 합성하기 위한 프로토콜을 간략하게 설명하고 MRSA 및 녹농균의 임상 샘플과 함께 미세 브로스 희석 방법을 사용하는 항균 테스트 접근 방식을 소개합니다. ZnO NP의 침전 방법은 아연 아세테이트 또는 질산 아연16과 같은 용해성 전구체를 사용하여 pH와 온도를 조정하여 불용성 고체 ZnO NP를 합성하는 것을 포함합니다. 상대적으로 쉽고 신속한 생산과 함께 이 방법은 합성의 반복성을 보장하고 입자 크기 및 형태에 대한 제어를 용이하게 합니다17. 이 합성 프로토콜에서는 가장 일반적으로 사용되는 침전제 중 하나인 수산화나트륨(NaOH)을 사용하여 아연 아세테이트를 침전시켰고, 소량의 헥사데실트리메틸암모늄 브로마이드(CTAB)를 사용하여 나노입자18의 제어되지 않은 합성을 억제했습니다. 다양한 항균 시험 중 ZnO 나노 입자의 항균 활성은 금속 산화물 나노 입자의 광학 간섭을 피하고 MIC19를 결정하기 위한 직접 콜로니 측정을 가능하게 하는 미세 브로스 희석 방법을 사용하여 평가되었습니다.
Access restricted. Please log in or start a trial to view this content.
프로토콜
이 연구에 사용된 시약 및 장비는 재료 표에 나열되어 있습니다.
1. 산화 아연 나노 입자의 제조
- 200mL의 절대 에틸 알코올을 측정하여 둥근 바닥 플라스크에 붓습니다.
- 둥근 바닥 플라스크를 가열 맨틀에 놓고 25-40 °C에서 교반을 유지합니다.
- 50mL 바이알에서 500mg의 CTAB를 측정하고 플라스크의 에틸 알코올에 추가합니다. CTAB가 완전히 녹을 때까지 저어줍니다.
- 용액에 아연 아세테이트 1.4g을 넣고 완전히 녹을 때까지 저어줍니다.
- 가열 맨틀 온도를 70 °C로 설정하여 용액의 온도를 높입니다.
- 혼합물에 25mL의 0.5M NaOH 용액을 넣고 투명 용액이 흰색이 될 때까지 1시간 동안 반응시킵니다.
- 용액을 50mL 코니컬 튜브에 분취하고 실온에서 15분 동안 15000× g 으로 원심분리한 다음 상층액을 버립니다.
- 원뿔형 튜브 중 하나에 증류수 10mL를 추가하고 용액을 초음파 처리하여 나노 입자를 재현탁시킵니다. 현탁액을 ZnO 펠릿이 들어있는 다른 원추형 튜브로 옮기고 모든 ZnO 용액이 하나의 원뿔형 튜브에 수집될 때까지 반복합니다.
- 15000× g 에서 원심분리를 통해 나노입자를 15분(실온) 동안 세척하고 상층액을 제거하고 증류수에 재현탁시킵니다. pH 시험지를 사용하여 상층액 용액의 pH를 확인하고 용액의 pH가 중성이 될 때까지 반복합니다.
알림: 상층액 용액의 pH가 중성(pH = 7)이 되면 상층액 용액을 버리고 증류수로 재현탁하지 마십시오. - 샘플 팔레트를 60°C에서 24시간 동안 진공 건조하고 ZnO NP 분말을 얻습니다.
2. MRSA와 녹농균을 이용한 항균 시험
- 세균 배양
참고: 임상 MDR 박테리아 균주는 한국 서울의 중앙대학교병원에서 획득했습니다.- TSB(Tryptic Soy Broth)에 비축된 MRSA 및 녹농균 박테리아 균주를 급속 냉동고에서 꺼냅니다.
- 박테리아 용액을 해동한 후 일회용 접종 루프를 사용하여 TSA(Tryptic Soy Agar) 플레이트에 용액을 줄무늬 줄무늬를 만듭니다. 줄무늬가 있는 한천 플레이트를 인큐베이터에 넣고 24시간 동안 배양합니다.
참고: TSA 플레이트에서 채취한 단일 콜로니를 박테리아 접종 루프를 사용하여 50mL 원추형 튜브에 있는 10mL의 TSB 배지에 첨가했습니다. 박테리아를 24시간 동안 배양하였다. 박테리아는 37°C의 호기성 배양 조건에서 배양하였다. - 박테리아 용액의 농도를 측정하려면 증류수를 사용하여 10배 연속 희석을 사용하여 배양 용액을 10-6 으로 희석합니다. 그런 다음 희석된 용액 50μL를 TSA 플레이트에 놓고 L자형 스프레더를 사용하여 용액을 펴 바릅니다.
- 인큐베이터에서 플레이트를 24시간 동안 배양합니다.
참고: 콜로니는 광학적으로 계수되었으며, 배양된 용액의 농도는 희석 인자에 계수된 콜로니의 수를 곱하여 계산되었습니다.
- 세균 샘플링
- 광범위한 ZnO 농도를 테스트하려면 Dulbecco의 DPBS(Phosphate-Buffered Saline)를 사용하여 2mg/mL ZnO NP 용액을 준비하고 2배 연속 희석을 수행하여 다른 농도를 만듭니다.
참고: 1000 μg/mL, 500 μg/mL, 250 μg/mL, 125 μg/mL 및 62.5 μg/mL를 테스트했습니다. - 테스트된 ZnO NP 농도 각각에 대해 100μL를 96웰 플레이트에 추가합니다.
참고: 웰의 각 샘플은 100μL의 박테리아 배양액을 추가하여 희석되므로 최종 원하는 ZnO NP 농도의 두 배(2x)를 사용합니다. 2% 항생제-항진균제(A/A) 용액을 양성 대조군으로 사용하고 DPBS를 음성 대조군으로 사용합니다. A/A는 페니실린과 스트렙토마이신 항생제 복합체로 각각 그람 양성 및 그람 음성 박테리아에 효과적입니다. - TSB 배지를 사용하여 박테리아 배양액을 1 × 106 CFU/mL로 희석하고 서로 다른 농도의 ZnO NP를 포함하는 각 웰에 100μL를 추가합니다.
참고: 초기 MRSA 및 녹농균 배양 용액 농도는 3 x 109 CFU/mL였습니다. 박테리아 배양 농도 1 x 106 CFU/mL는 배양 용액을 1/20 및 1/150 희석하여 만들었습니다. 100 μL의 ZnO NP와 혼합 한 후 박테리아의 최종 농도는 5 × 105 CFU / mL가됩니다. - 96웰 플레이트를 37°C 인큐베이터에 넣고 24시간 동안 배양합니다.
- 광범위한 ZnO 농도를 테스트하려면 Dulbecco의 DPBS(Phosphate-Buffered Saline)를 사용하여 2mg/mL ZnO NP 용액을 준비하고 2배 연속 희석을 수행하여 다른 농도를 만듭니다.
- 세균 확산
- 각 웰에서 100μL를 피펫팅하고 10-6까지 다양한 10배 연속 희석액을 준비합니다.
알림: 박테리아 용액이 포함된 ZnO NP 100μL를 멸균 증류수 900μL에 넣고 6회 반복합니다. - 4개의 희석된 용액에서 50μL를 피펫팅하고 TSA 배지 플레이트에 추가합니다. L자형 세포 스프레더를 사용하여 박테리아 현탁액을 한천 플레이트에 펴 바릅니다.
참고: 100, 10-2, 10-4 및 10-6 희석액을 사용합니다. 모든 실험을 삼중으로 수행하십시오. 모든 박테리아 용액이 한천 플레이트에 흡수될 때까지 펴 바릅니다. - 한천 플레이트를 37°C 인큐베이터에 넣고 24시간 동안 배양합니다.
- 각 웰에서 100μL를 피펫팅하고 10-6까지 다양한 10배 연속 희석액을 준비합니다.
- 세균 CFU 계수
- 각 그룹에 대해 계산할 수 있는 희석 계수를 선택합니다. 계산 가능한 희석 플레이트에 모든 콜로니를 표시하고 농도가 CFU/mL의 #이 되도록 다시 계산합니다.
알림: 계산 가능한 희석 계수는 개별 플레이트에 20-100 CFU가 있는 플레이트를 나타냅니다. 초기에 계수된 농도 결과 # 계수 CFU/50 μL. 희석되지 않은 박테리아 용액과 함께 스프레드 플레이트를 사용하여 잠재적인 최소 살균 농도를 결정합니다. - 얻은 데이터를 사용하여 음성 대조군에 있는 박테리아에 대한 살아있는 박테리아의 비율을 나타냅니다.
참고: 살아있는 박테리아의 비율(%) =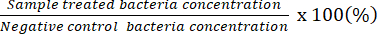
- 각 그룹에 대해 계산할 수 있는 희석 계수를 선택합니다. 계산 가능한 희석 플레이트에 모든 콜로니를 표시하고 농도가 CFU/mL의 #이 되도록 다시 계산합니다.
Access restricted. Please log in or start a trial to view this content.
결과
ZnO NP의 성공적인 합성은 그림 1A와 같이 투과 전자 현미경(TEM)을 사용하여 확인되었습니다. 얻어진 ZnO NP는 평균 입자 크기가 35.35nm이고 표준 편차가 6.81nm인 둥근 모양으로 관찰되었습니다. 이러한 나노 입자의 침전은 아연 아세테이트에 NaOH 용액을 첨가하여 이중 변위 반응을 통해 관찰되었으며, 여기서 Zn2 + 이온은 가수 분해를 거쳤습니다.<...
Access restricted. Please log in or start a trial to view this content.
토론
침전을 통한 ZnO NP의 합성은 비교적 간단하고 간단합니다. 이 방법을 사용하여 ZnO NP를 성공적으로 합성하려면 전구체(아연 아세테이트)가 용매에 완전히 용해되도록 교반하는 것이 중요합니다. 또한 온도를 높이면 성공적인 이중 변위 반응을 유도하는 데 도움이 됩니다. ZnO NP의 합성에는 침전제, 침전제의 농도 및 계면활성제를 포함하여 크기와 모양을 결정하는 ?...
Access restricted. Please log in or start a trial to view this content.
공개
최종훈 박사는 CEO/설립자이며, 최용현 박사는 Nanomedicine Corporation의 파인만 공과대학(Feynman Institute of Technology)의 CTO입니다.
감사의 말
본 연구는 2022년 중앙대학교 대학원 연구장학금(Ms. Gahyun Lee)의 지원을 받아 수행되었다. 또한, 한국연구재단(National Research Foundation of Korea, NRF)의 국비지원금(과기정통부)(제2020R1A5A1018052호)과 중소벤처기업부(MSS, Korea)의 기술개발사업(RS202300261938)의 지원을 받았다.
Access restricted. Please log in or start a trial to view this content.
자료
| Name | Company | Catalog Number | Comments |
| DLS | Zetasizer Pro | ||
| Ethyl alcohol, absolute | DAEJUNG | 4023-2304 | |
| Microplate reader | BioTeck | ||
| Sodium Hydroxide | Sigma-Aldrich | 221465 | |
| TEM | JEOL JEM-F200 | ||
| TSA | DB difco | 236950 | |
| TSB | DB difco | 211825 | |
| XRD | NEW D8-Advance | ||
| Zinc acetate | Sigma-Aldrich | 383317 |
참고문헌
- Catalano, A., et al. Multidrug resistance (MDR): A widespread phenomenon in pharmacological therapies. Molecules. 27 (3), 616(2022).
- Bazaid, A. S., et al. Bacterial infections among patients with chronic diseases at a tertiary care hospital in Saudi Arabia. Microorganisms. 10 (10), 1907(2022).
- Miller, E. L. The penicillins: A review and update. J Midwifery Women's Health. 47 (6), 426-434 (2002).
- Martínez-Trejo, A., et al. Evasion of antimicrobial activity in acinetobacter baumannii by target site modifications: An effective resistance mechanism. Int J Mol Sci. 23 (12), 6582(2022).
- Jiang, J. -H., et al. Antibiotic resistance and host immune evasion in staphylococcus aureus mediated by a metabolic adaptation. Proc Natl Acad Sci U S A. 116 (9), 3722-3727 (2019).
- Lee, H. N., et al. A lateral flow assay for nucleic acid detection based on rolling circle amplification using capture ligand-modified oligonucleotides. BioChip J. 16 (4), 441-450 (2022).
- Craft, K. M., Nguyen, J. M., Berg, L. J., Townsend, S. D. Methicillin-resistant staphylococcus aureus (MRSA): Antibiotic-resistance and the biofilm phenotype. Med Chem Comm. 10 (8), 1231-1241 (2019).
- Tieu, M. -V., Pham, D. T., Le, H. T. N., Hoang, T. X., Cho, S. Rapid and ultrasensitive detection of Staphylococcus aureus using a gold-interdigitated single-wave-shaped electrode (AU-ISWE) electrochemical biosensor. BioChip J. 17, 1-10 (2023).
- Turner, N. A., et al. Methicillin-resistant Staphylococcus aureus: An overview of basic and clinical research. Nat Rev Microbiol. 17 (4), 203-218 (2019).
- Tuon, F. F., Dantas, L. R., Suss, P. H., Tasca Ribeiro, V. S. Pathogenesis of the Pseudomonas aeruginosa biofilm: A review. Pathogens. 11 (3), 300(2022).
- Sarabhai, S., Sharma, P., Capalash, N. Ellagic acid derivatives from terminalia chebula retz. Downregulate the expression of quorum sensing genes to attenuate pseudomonas aeruginosa pao1 virulence. PLoS One. 8 (1), e53441(2013).
- Dizaj, S. M., Lotfipour, F., Barzegar-Jalali, M., Zarrintan, M. H., Adibkia, K. Antimicrobial activity of the metals and metal oxide nanoparticles. Mat Sci Eng: C. 44, 278-284 (2014).
- Ribeiro, A. I., Dias, A. M., Zille, A. Synergistic effects between metal nanoparticles and commercial antimicrobial agents: A review. ACS App Nano Mater. 5 (3), 3030-3064 (2022).
- Newman, M. D., Stotland, M., Ellis, J. I. The safety of nanosized particles in titanium dioxide-and zinc oxide-based sunscreens. J Am Acad Dermatol. 61 (4), 685-692 (2009).
- Sivakumar, P., Lee, M., Kim, Y. -S., Shim, M. S. Photo-triggered antibacterial and anticancer activities of zinc oxide nanoparticles. J Mater Chem B. 6 (30), 4852-4871 (2018).
- Kołodziejczak-Radzimska, A., Jesionowski, T. Zinc oxide-from synthesis to application: A review. Materials. 7 (4), 2833-2881 (2014).
- Raoufi, D. Synthesis and microstructural properties of ZnO nanoparticles prepared by precipitation method. Renew Energy. 50, 932-937 (2013).
- Wang, Y. -X., Sun, J., Fan, X., Yu, X. A CTAB-assisted hydrothermal and solvothermal synthesis of ZnO nanopowders. Ceram Int. 37 (8), 3431-3436 (2011).
- Balouiri, M., Sadiki, M., Ibnsouda, S. K. Methods for in vitro evaluating antimicrobial activity: A review. J Pharm Anal. 6 (2), 71-79 (2016).
- Clogston, J. D., Patri, A. K. Zeta potential measurement. Characterization of nanoparticles intended for drug delivery. Methods Mol Biol. McNeil, S. , 63-70 (2011).
- Abdelbaky, A. S., Mohamed, A. M., Sharaky, M., Mohamed, N. A., Diab, Y. M. Green approach for the synthesis of ZnO nanoparticles using Cymbopogon citratus aqueous leaf extract: Characterization and evaluation of their biological activities. Chem Biol Technol Agric. 10 (1), 63(2023).
- Ankamwar, B. G., Kamble, V. B., Annsi, J. I., Sarma, L. S., Mahajan, C. M. Solar photocatalytic degradation of methylene blue by ZnO nanoparticles. J Nanosci Nanotechnol. 17 (2), 1185-1192 (2017).
- Babayevska, N., et al. Zno size and shape effect on antibacterial activity and cytotoxicity profile. Scientific Rep. 12 (1), 8148(2022).
- Hamidian, K., Sarani, M., Behjati, S., Mahjoub, M., Zafarnia, N. Cytotoxic performance of synthesized mn-doped ZnO nanorods in mcf-7 cells. ChemistrySelect. 8 (19), e202300292(2023).
- Gharpure, S., et al. Non-antibacterial and antibacterial ZnO nanoparticles composed of different surfactants. J Nanosci Nanotechnol. 21 (12), 5945-5959 (2021).
- Dhoke, S. K. Synthesis of nano-ZnO by chemical method and its characterization. Results Chem. 5, 100771(2023).
- Choi, K. -C., et al. Modifying hydrogen bonding interaction in solvent and dispersion of ZnO nanoparticles: Impact on the photovoltaic performance of inverted organic solar cells. RSC Adv. 4 (14), 7160-7166 (2014).
- Lee, W., et al. High colloidal stability ZnO nanoparticles independent on solvent polarity and their application in polymer solar cells. Scientific Rep. 10 (1), 18055(2020).
- Cozzoli, P. D., Kornowski, A., Weller, H. Colloidal synthesis of organic-capped ZnO nanocrystals via a sequential reduction-oxidation reaction. J Phy Chem B. 109 (7), 2638-2644 (2005).
- Roh, S., Jang, Y., Yoo, J., Seong, H. Surface modification strategies for biomedical applications: Enhancing cell-biomaterial interfaces and biochip performances. BioChip J. 17, 1-18 (2023).
- Chen, D., Jiao, X., Cheng, G. Hydrothermal synthesis of zinc oxide powders with different morphologies. Solid State Commun. 113 (6), 363-366 (1999).
- Hu, X. -L., Zhu, Y. -J., Wang, S. -W. Sonochemical and microwave-assisted synthesis of linked single-crystalline ZnO rods. Mater Chem Phys. 88 (2-3), 421-426 (2004).
- Ahamad Khan, M., et al. Phytogenically synthesized zinc oxide nanoparticles (ZnO-NPs) potentially inhibit the bacterial pathogens: In vitro studies. Toxics. 11 (5), 452(2023).
- Xie, J., et al. Recent advances in ZnO nanomaterial-mediated biological applications and action mechanisms. Nanomaterials. 13 (9), 1500(2023).
- Chawla, U., et al. A review on ZnO-based targeted drug delivery system. Lett Drug Des Discov. 21 (3), 397-420 (2024).
- Alavi, M., Nokhodchi, A. An overview on antimicrobial and wound healing properties of ZnO nanobiofilms, hydrogels, and bionanocomposites based on cellulose, chitosan, and alginate polymers. Carbohydr Polym. 227, 115349(2020).
Access restricted. Please log in or start a trial to view this content.
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유