É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Prostatectomia Radical Assistida por Robô Poupadora de Retzius
Neste Artigo
Resumo
A prostatectomia radical poupadora de Retzius assistida por robô é uma técnica que permite preservar a continência urinária ou facilita a recuperação da continência urinária na maioria dos pacientes. Os pacientes devem ser informados sobre o risco de uma margem cirúrgica positiva.
Resumo
A técnica de prostatectomia radical assistida por robô poupador de Retzius (RS-RARP) e a experiência inicial com ela em um único centro são fornecidas. A técnica é descrita passo a passo e ilustrada por um vídeo para melhorar a reprodutibilidade. Os primeiros resultados oncológicos e funcionais foram avaliados. No total, 77 pacientes foram incluídos com um seguimento mediano de 11 meses (variação: 3-21 meses). Cinquenta e um por cento dos pacientes tinham câncer de próstata local de alto risco ou localmente avançado. Não houve complicações intraoperatórias, e todas as complicações de alto grau (2,6%) estavam relacionadas à dissecção linfonodal pélvica realizada concomitantemente com RS-RARP. O tempo mediano de operação foi de 160 min (intervalo: 122-265 min) e a mediana de permanência hospitalar foi de 3 (intervalo: 3-8) dias. Uma margem cirúrgica positiva foi relatada em 42,9%. A sobrevida livre de recidiva bioquímica em um ano foi de 90,1%. Após 6 meses, todos os pacientes eram socialmente continentes e após 1 ano, 94,3% eram totalmente continentes. Dos pacientes sexualmente ativos que foram submetidos a pelo menos preservação unilateral de nervos, 43,3% foram capazes de ter relações sexuais. Esta série destaca a segurança cirúrgica da realização de RS-RARP por uma técnica padronizada e confirma o efeito benéfico no retorno precoce da continência. O paciente precisa ser informado sobre o risco de uma margem cirúrgica positiva.
Introdução
Para curar casos localizados e selecionados de câncer de próstata localmente avançado, a prostatectomia radical é uma das opções de tratamento recomendadas1. Técnicas minimamente invasivas (laparoscopia convencional e laparoscopia assistida por robô) têm a vantagem de diminuir a perda de sangue, a dor pós-operatória e o tempo de internação em comparação com a prostatectomia radical aberta 2,3. Entre as técnicas minimamente invasivas, a cirurgia assistida por robô combina as vantagens da cirurgia minimamente invasiva com maior destreza e liberdade de movimento dos instrumentos cirúrgicos e com visão perioperatória tridimensional. Em países com bons recursos, a prostatectomia radical assistida por robô (RARP) tornou-se o modo predominante para a realização da prostatectomia radical4.
A incontinência urinária, temporária ou definitiva, é um efeito colateral comum da prostatectomia radical, independentemente do modo pela qual tenha sido realizada5. Com RARP ANTERIOR ABERTA (ABDOMINAL), LAPAROSCÓPICA E "PADRÃO" (SA-RARP), a prostatectomia radical é realizada por uma abordagem anterior na qual o espaço retropúbico (de Retzius) é aberto6. Graças ao aumento da destreza associada à RARP, é possível uma abordagem anatômica alternativa na qual a próstata é ressecada através da bolsa retovesical ou da bolsa de Douglas, conforme descrito pela primeira vez por Galfano et al.7. Esta abordagem posterior deixa intacto o espaço de Retzius ("Retzius-sparing RARP"; RS-RARP). A principal vantagem da RS-RARP parece ser uma recuperação maior e mais rápida da continência urinária8. Este estudo tem como objetivo descrever em detalhes (como sugerido pelo painel de consenso de Pasadena9) as etapas do RS-RARP apoiado por material audiovisual e relatar os primeiros resultados funcionais e oncológicos dos primeiros casos em um único centro.
Protocolo
Este estudo foi submetido ao comitê de ética local do Hospital Universitário de Ghent e a aprovação institucional foi concedida (EC UZG 2019/1506). O estudo foi registado no registo de estudos belga sob a referência B670201941650. Todos os pacientes assinaram o termo de consentimento livre e esclarecido.
1. Preparação e posicionamento do paciente
- Preparação
- Seguir as diretrizes contemporâneas internacionalmente aceitas para diagnosticar o câncer de próstata e definir a indicação para a prostatectomia radical1. Use a ressonância nuclear magnética (RNM) multiparamétrica para estadiamento local, pois isso fornece informações importantes sobre o volume da próstata, o aumento concomitante da próstata e o lobo mediano, além da localização e extensão do tumor. Isso ajudará na decisão de realizar a preservação dos nervos e/ou a preservação da bexigano pescoço 10. Certifique-se de que esta imagem está disponível no momento da operação.
- Oferecer RS-RARP a pacientes com câncer de próstata local ou localmente avançado e uma expectativa de vida >10 anos. Discuta opções alternativas de tratamento, como vigilância ativa, outras modalidades de prostatectomia radical e irradiação, sempre que aplicável. Não ofereça RS-RARP a pacientes com câncer de próstata metastático.
- Descartar condições médicas que sejam uma contraindicação para cirurgia robótica em posição íngreme de Trendelenburg por exame anestesiológico pré-operatório. Se essas condições médicas estiverem presentes, trate-as primeiro (se possível) ou discuta o tratamento alternativo com o paciente. Inclua o tipo e a triagem do sangue do paciente na avaliação pré-operatória no caso raro de uma transfusão de sangue ser necessária.
- Administrar natriumlaurylsulfoacetate-sorbitol-natriumcitratedihydrate clysma 4-8 h antes da operação para limpar o reto. Permitir a ingestão de alimentos e a ingestão de líquidos límpidos até 6 h e 4 h antes da indução, respectivamente.
- Realizar anestesia geral com intubação endotraqueal. Administrar um tiro profilático de dose única de cefazolina 2g na indução.
- Insira uma linha intravenosa periférica de grande calibre e uma linha arterial para garantir o acesso e o monitoramento do sistema circulatório. Use pulsoximetria e monitoramento cardíaco de 4 derivações durante todo o procedimento.
- Posicionamento
- Coloque o paciente na posição supina. Coloque e prenda os braços ao longo do corpo do paciente e prenda as pernas por uma alça ao nível dos joelhos. Proteja todos os pontos de compressão com almofadas de gel.
NOTA: O paciente usa meias dissuasivas de tromboembolia. - Aplique apoios de ombro para evitar mudanças devido à posição íngreme de Trendelenburg. Prenda o tórax do paciente à mesa com fita adesiva (7,5 cm de largura) para evitar novos deslocamentos. Cubra o paciente com um dispositivo de cobertura de aquecimento torácico.
- Desinfetar o campo cirúrgico por solução alcoólica de iodopovidona ou, alternativamente, por clorexidina em caso de alergia ao iodo. Inclua o abdômen anterior, virilhas e genitália no campo cirúrgico. Anexe cortinas estéreis nas bordas do campo após a desinfecção.
- Coloque um cateter transuretral de látex revestido com hidrogel 16 F para garantir a drenagem urinária e o esvaziamento da bexiga no momento da inserção do trocarte. Certifique-se de ter fácil acesso ao cateter transuretral, pois ele ajudará na identificação da uretra mais tarde durante o procedimento.
- Coloque o paciente na posição supina. Coloque e prenda os braços ao longo do corpo do paciente e prenda as pernas por uma alça ao nível dos joelhos. Proteja todos os pontos de compressão com almofadas de gel.
2. Acoplamento do sistema robótico
- Cubra os braços robóticos do carrinho do paciente com cortinas estéreis, pois eles estarão mais tarde em contato com o campo cirúrgico. Use uma câmera de 30°.
NOTA: O sistema Da Vinci Xi é usado para essa operação (Figura 1). Este sistema consiste em três partes básicas: um console do cirurgião que é colocado a uma distância da mesa de operação; um carrinho de paciente com quatro braços robóticos que serão acoplados aos trocartes e um carrinho de visão com o monitor para enfermeiro e assistente de esfoliação, sistema de eletrocautério e insuflador de CO2 colocado ao lado do paciente. - Trocar inserção
- Inserção de trocarte de câmera
- Faça uma incisão na pele longitudinalmente sobre 2-2,5 cm cerca de 1 cm acima do umbigo. Dissecar o tecido adiposo subcutâneo sem rodeios até que a fáscia do reto seja identificada.
- Incidir longitudinalmente a fáscia do reto e colocar suturas absorvíveis de poliglactina 1 na fáscia de ambos os lados.
- Abra o peritônio com uma tesoura. Garantir por palpação digital com o dedo indicador que não há contato do intestino com essa abertura.
- Insira um trocarte robótico de câmera de 8 mm com cone de Hasson na cavidade peritoneal. Prenda os grampos dos cones às suturas de permanência na fáscia.
- Ligue o trocarte da câmara ao insuflador de CO2 e insufle até à pressão de 12-15 mmHg. Traga o paciente na posição de Trendelenburg de 30-35° para libertar a pelve menor do intestino delgado. Certifique-se de que não haja deslocamento do corpo durante o posicionamento íngreme de Trendelenburg.
- Coloque no nível horizontal do trocador da câmera, dois e um trocars de 8 mm para os instrumentos robóticos, respectivamente, nos lados esquerdo e direito do trocarte da câmera com distância de 6-8 cm entre qualquer trocar robótico. Coloque todos os trocartes sob visão direta com a câmera. Use o obturador de ponta contundente para colocar os trocartes.
- Coloque um trocarte assistente de 5 mm e 5 cm cranialmente à linha média entre o trocarte da câmera e o trocador robótico direito. Coloque um trocarte assistente de 12 mm 3 cm acima da espinha ilíaca direita anterior superior.
NOTA: O assistente está no lado direito do paciente, enquanto a enfermeira de esfoliação está no lado esquerdo do paciente. - Desconecte o cabo de insuflação no trocarte da câmera e conecte-se ao trocador assistente de 12 mm.
- Inserção de trocarte de câmera
- Acoplamento do carrinho do paciente e inserção de instrumentos robóticos
- Mova o carrinho do paciente para o lado direito do paciente até que o terceiro braço possa ser conectado ao trocador da câmera. Otimize ainda mais o posicionamento do carrinho do paciente usando a aplicação automática do sistema. Conecte os outros três trocartes de 8 mm com pelo menos 10 cm de distância entre os braços para evitar a colisão durante os movimentos operacionais.
- Use como instrumentos robóticos, uma tesoura curva monopolar, uma pinça bipolar fenestrada, uma pinça Cadiere e um grande driver de agulha. No início da operação, coloque a tesoura monopolar no trocador robótico direito, a pinça fenestrada bipolar no trocador robótico medial esquerdo e a pinça Cadiere no trocador robótico lateral esquerdo.
- Controle a inserção de instrumentos robóticos por uma visão direta para evitar a perfuração de vísceras, aderências omentais ou estruturas vasculares.
- Como instrumentos assistentes, use um dispositivo laparoscópico de sucção-irrigação colocado no trocarte assistente de 5 mm e um agarrador laparoscópico colocado no trocador assistente de 12 mm. Ocorra no console do cirurgião para iniciar a parte assistida por robô da operação.
NOTA: Estes instrumentos laparoscópicos são manuseados pelo assistente e não estão ligados a braços robóticos.
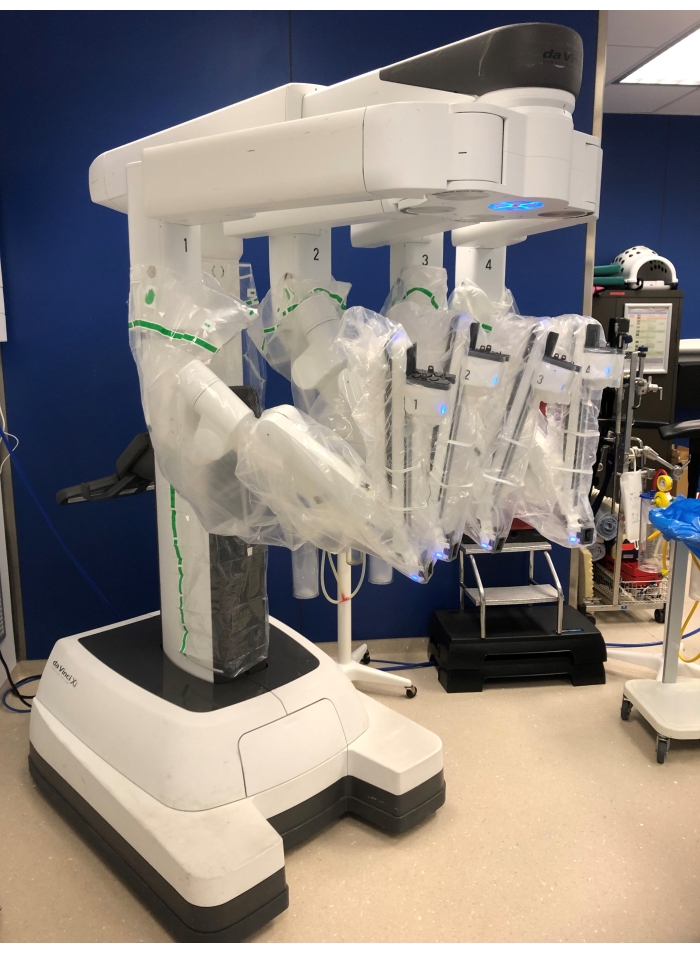
Figura 1: O carrinho do paciente com 4 braços robóticos. Clique aqui para ver uma versão maior desta figura.
3. Dissecção das vesículas seminais
- Acesso à pelve menor
- Realize a aderência liberando quaisquer aderências que dificultem o fácil acesso à pelve menor e à bolsa retovesical. Realize essa aderência com a lente virada 30° para baixo.
- Facilite o acesso à bolsa retovesical (ou de Douglas) empurrando a bexiga para cima com a pinça Cadiere e empurrando o reto para baixo com o dispositivo de sucção-irrigação.
- Acesso às vesículas seminais
- Incida o peritônio sobre o ducto deferente em ambos os lados e continue medialmente até que essas incisões se alcancem.
NOTA: O ducto deferente é mais facilmente identificado quando atravessa os vasos ilíacos externos, especialmente em homens obesos. - Na borda lateral da incisão, disseque o ducto deferente de forma circunferencial e transecte-o. Dissecar o ducto deferente medialmente até que a ponta da vesical seminal seja atingida.
- Incida o peritônio sobre o ducto deferente em ambos os lados e continue medialmente até que essas incisões se alcancem.
- Dissecção das vesículas seminais
- Descasque a fáscia de Denonvilliers medialmente do ducto deferente caso não haja evidência de invasão seminal da vesícula. Se houver suspeita de invasão da vesícula seminal, incite a fáscia de Denonvilliers 1-2 mm abaixo da borda inferior da vesícula seminal para garantir uma margem cirúrgica segura.
- Fixar os vasos onde eles entram na ponta e superfície lateral da vesícula seminal por hemostasia bipolar ou com clipes metálicos de 5 mm e transectá-los. Continue esta dissecção até que a base da próstata tenha sido atingida. Execute o mesmo procedimento no lado oposto.
NOTA: Os nervos eréteis estão próximos à ponta e à superfície lateral das vesículas seminais e a coagulação monopolar deve ser evitada no caso de se tentar poupar nervos.
4. Dissecção pós-erolateral da próstata
- Dissecção lateral da próstata
- Retraia a vesícula seminal medialmente pela pinça de Cadiere para o lado direito e pelo agarrador laparoscópico assistente para o lado esquerdo. Isso permite a visualização do tecido adiposo em um triângulo entre a base da vesícula seminal e a região lateral à base da próstata.
NOTA: Este triângulo está logo acima dos nervos eréteis e pedículo prostático. - Realize dissecção contundente neste tecido adiposo ao longo da superfície lateral da próstata até que o reflexo da fáscia endopélvica seja encontrado. Realizar hemostasia pela pinça bipolar, pois a corrente monopolar pode danificar os nervos eréteis.
- Retraia a vesícula seminal medialmente pela pinça de Cadiere para o lado direito e pelo agarrador laparoscópico assistente para o lado esquerdo. Isso permite a visualização do tecido adiposo em um triângulo entre a base da vesícula seminal e a região lateral à base da próstata.
- Suspensão do peritônio
- Facilitar o acesso à próstata e colo da bexiga por duas suturas de suspensão através da parte superior da incisão peritoneal.
- Insira o driver de agulha grande no braço robótico direito. Coloque uma agulha reta com uma sutura não reabsorvível através da parede abdominal 2-3 cm acima do osso púbico apenas medialmente do ligamento umbilical medial.
- Perfure a parte superior da incisão peritoneal e o tecido adiposo subjacente com a agulha reta. Traga a agulha de volta para fora do corpo, perto do trato de inserção. Mantenha este ponto de suspensão sob tensão usando um grampo de mosquito fora do abdômen. Faça o mesmo no lado contralateral.
- Dissecção posterior da próstata
- Remova o driver da agulha e traga de volta a tesoura curva no braço robótico direito. Retraia as vesículas seminais para cima e ligeiramente laterais com a pinça de Cadiere e o agarrador laparoscópico assistente para os lados esquerdo e direito, respectivamente, para colocar a fáscia de Denonvilliers sob tensão.
- Manipulação de nervos eréteis.
- Abordagem bilateral poupadora de nervos: Desenvolver um plano por dissecção contundente entre a fáscia prostática e a fáscia de Denonvilliers até o ápice da próstata e lateralmente até que os vasos prosstáticos sejam encontrados.
- Abordagem não poupadora de nervos: Incise a fáscia de Denonvilliers 1-2 mm abaixo da base da próstata. Dissecar a superfície anterior do reto e mais lateralmente no tecido adiposo perirretal.
- Abordagem poupadora unilateral de nervos: Execute a etapa 4.3.2.1 no local da preservação do nervo e a etapa 4.3.2.2 no local da preservação não nervosa. Incise a fáscia de Denonvilliers na linha média sobre a parede retal.
- Hemostasia do pedículo prostático e dissecção do feixe neurovascular
- Acesso ao lado direito: Segure a base da próstata com a pinça de Cadiere logo abaixo da fixação da vesícula seminal ipsilateral. Retraia a base da próstata medialmente e ligeiramente para cima para trazer o pedículo prostático sob tensão.
- Faça uma janela com a tesoura monopolar no pedículo prostático e prenda esta parte do pedículo usando um grande clipe de bloqueio de polímero que é aplicado através dos trocartes assistentes de 12 mm. Transecte esta parte do pedículo no lado prostático do clipe.
- Repita 4.4.2 (geralmente 2-3 vezes) até que todo o pedículo prostático esteja fixado. Mantenha a tensão no pedículo prostático após cada vez que uma parte do pedículo é transectada.
- Repita o passo 4.4.2 até atingir o ápice da próstata. Mantenha uma distância segura da superfície prostática cada vez que uma janela é feita.
NOTA: Isso sacrificará o feixe neurovascular contendo os nervos eréteis. - Descascar o feixe neurovascular da fáscia prostática por dissecção contundente e mantendo o feixe sob leve tensão usando uma retração medial e ascendente progressiva com a pinça Cadière.
- Prenda pequenos vasos presos à próstata por clipes metálicos de 5 mm e transecte-os com uma tesoura. Prossiga até que o ápice da próstata seja atingido. Garanta a sucção e irrigação pelo assistente através do trocarte de 5 mm sempre que necessário.
- Acesso ao lado esquerdo: Mude a pinça Cadiere para o trocarte medial do lado esquerdo e a pinça bipolar fenestrada para o trocador lateral esquerdo. Retraia a base da próstata medialmente e para cima. Use o endopulso do instrumento para criar um ângulo de 90° para baixo, sob o qual o assistente tenha fácil acesso para colocar os clipes. Repita o procedimento no lado esquerdo, conforme descrito acima (etapas 4.4.2 até 4.4.6).
5. Dissecção do colo da bexiga
- Segure as vesículas seminais pela pinça de Cadiere e recrai-as para baixo para criar tensão entre o colo da bexiga e a base da próstata.
- Desenvolva o plano entre o colo da bexiga e a base da próstata usando uma combinação de incisões monopolares com a tesoura e a dissecção contundente. Preserve as fibras musculares circulares do colo da bexiga em caso de preservação do colo da bexiga. Mova as vesículas seminais mais lateralmente para facilitar a dissecção lateral do colo da bexiga.
- Abertura do colo da bexiga
- Incidir a mucosa na face posterior do colo vesical com mais de 1 cm. Visualize o cateter uretral.
- Coloque uma sutura de poliglactina 3-0 absorvível na face posterior do colo da bexiga. Desinche o balão do cateter e retraia o cateter.
- Segure a sutura de permanência com a pinça bipolar fenestrada e mova-se para cima até que a parte anterior do colo da bexiga se torne visível. Incise ainda mais a mucosa e libere o colo da bexiga da base da próstata.
- Coloque uma sutura de segunda estada na face anterior do colo da bexiga com sutura absorvível de poliglactina 3-0 pouco antes de o colo da bexiga ser completamente liberado.
NOTA: Estas suturas de permanência facilitarão a identificação posterior do colo vesical para a anastomose vesico-uretral.
6. Dissecção do ápice anterior e prostática
- Dissecção anterior
- Continue a leve tensão ascendente na sutura de permanência na face posterior da bexiga com a pinça bipolar fenestrada. Coloque a pinça de Cadiere na uretra prostática e aplique tração para baixo para criar tensão na superfície anterior da próstata.
- Siga a superfície anterior da próstata usando uma combinação de dissecção contundente e incisão monopolar poupando o plexo de Santorini, os ligamentos pubostáticos e o espaço de Retzius. Mova a pinça Cadiere lateralmente para facilitar a dissecção anterolateral.
- Dissecção do ápice da próstata
- Identifique a uretra membranosa agarrando o cateter uretral com a pinça Cadière.
- Incidir as fibras circulares da uretra 1-2 mm caudalmente ao ápice da próstata. Empurre as fibras circulares em direção ao ápice da próstata para expor a camada longitudinal interna da uretra (o chamado lissoesfíncter). Transecte esta camada interna o mais próximo possível da próstata para preservar ao máximo o lissoesfíncter.
- Incise quaisquer anexos dorsalmente à uretra membranosa até que a próstata esteja completamente livre dos tecidos circundantes. Insira um endobag através do trocarte assistente de 12 mm para colocar na próstata (e vesículas seminais). Feche o endobag e deixe-o fechado na fossa ilíaca direita.
7. Anastomose vesico-uretral
- Coloque o grande driver de agulha no trocarte robótico direito e na pinça Cadiere e pinça bipolar fenestrada, respectivamente, no trocador robótico esquerdo medial e lateral. Use o fórceps bipolar fenestrado para empurrar suavemente a bexiga em direção à uretra, a fim de reduzir a tensão na anastomose.
- Sutura da anastomose vesico-uretral
- Coloque a primeira sutura do primeiro arame farpado absorvível (3-0, 23 cm de comprimento) do lado de fora lateralmente à direita da posição das 12 horas no colo da bexiga. Puxe a sutura de permanência anterior que foi colocada na etapa 5.3.4 para identificar o colo vesical e a mucosa da bexiga.
- Coloque a sutura de dentro para fora na uretra, também ligeiramente lateral à direita da posição das 12 horas. Identifique a uretra movendo a ponta do cateter uretral para a uretra membranosa.
- Coloque a primeira sutura do segundo arame farpado absorvível (3-0, 23 cm de comprimento) do lado de fora para dentro, apenas lateralmente à esquerda da posição das 12 horas no colo da bexiga e de dentro para fora na uretra na mesma posição.
- Para sutura posterior no lado esquerdo, aproximar a mucosa vesical da mucosa contra a mucosa uretral por tração progressiva em ambas as extremidades dos arames farpados. Repita a sutura com o segundo arame farpado de fora para dentro no colo da bexiga e de dentro para fora na uretra duas vezes, momento em que a posição das 9 horas é atingida. Aproxime a mucosa da bexiga contra a mucosa uretral após cada sutura.
- Para a sutura do lado direito, realize a sutura com o primeiro arame farpado de fora para dentro no colo da bexiga e de dentro para fora na uretra, até que a posição das 6 horas seja atingida. Não aproxime ainda da última sutura para permitir espaço para finalizar o lado canhoto da anastomose.
- Para sutura anterior no lado esquerdo, continue a anastomose no lado esquerdo indo das 9 horas às 6 horas. Não aproxime ainda da última sutura para permitir que a ponta do cateter passe entre os arames farpados esquerdo e direito.
- Segure a ponta do cateter e coloque-o na bexiga. Insufflate o balão.
- Aperte as últimas suturas nos lados esquerdo e direito até que a bexiga e a mucosa uretral estejam aproximadas. Verifique a estanqueidade da anastomose por instilação de 120 mL de água na bexiga (teste de vazamento).
- Coloque a primeira sutura do primeiro arame farpado absorvível (3-0, 23 cm de comprimento) do lado de fora lateralmente à direita da posição das 12 horas no colo da bexiga. Puxe a sutura de permanência anterior que foi colocada na etapa 5.3.4 para identificar o colo vesical e a mucosa da bexiga.
- Remova as suturas de suspensão na parte superior da incisão peritoneal. Use os restos dos arames farpados para fechar a incisão peritoneal de medial para lateral em ambos os lados. Realizar uma dissecção bilateral dos linfonodos pélvicos, se indicado por diretrizes contemporâneas internacionalmente aceitas1.
NOTA: Nenhum dreno cirúrgico é deixado no caso de a dissecção dos linfonodos pélvicos não ter sido realizada.
8. Extração da próstata e fechamento das incisões
- Transfira o fio de extração do endobag do trocarte robótico direito para o trocarte da câmera sob visão direta.
- Desinche o abdômen e remova os trocartes sob visão direta. Mude a posição de Trendelenburg para a posição supina neutra. Incidir ainda mais a incisão da pele supra-umbilical e incisão da fáscia para permitir a fácil extração da próstata.
NOTA: O tamanho desta incisão depende do tamanho da próstata. - Feche a fáscia do reto com uma sutura de poliglactina 1 reabsorvível. Feche o tecido subcutâneo no trocarte da câmera e no trocarte assistente de 12 mm com sutura de poliglactina 3-0 reabsorvível. Feche todas as incisões da pele com grampeadores de pele.
9. Cuidados pós-operatórios
- Transferir o paciente para a unidade de cuidados pós-operatórios e monitorar por 2-3 h. Transferir o paciente para a unidade de internação após aprovação do anestesiologista e cirurgião.
- Permita que o paciente retome a ingestão de fluidos claros. Permita a ingestão de alimentos sólidos e estimule a caminhada durante o primeiro dia de pós-operatório. Retirar o cateter uretral no terceiro dia de pós-operatório e medir o volume miccional e o volume residual da bexiga. Substitua o cateter em caso de volume residual substancial e remova-o na policlínica 1 semana depois.
- Dar alta ao paciente no terceiro dia de pós-operatório. Retirar os grampeadores cutâneos entre o 10º e o14º dia de pós-operatório pelo clínico geral. Administrar heparina de baixo peso molecular por via subcutânea até o20º dia de pós-operatório por uma enfermeira em domicílio ou pelo próprio paciente.
Resultados
Todos os pacientes com câncer de próstata local ou localmente avançado, com expectativa de vida >10 anos e sem contraindicações anestesiológicas, receberam o RS-RARP como uma das opções de tratamento para sua doença. Pacientes submetidos à prostatectomia radical citorredutora para câncer de próstata metastático no contexto de um ensaio clínico ou prostatectomia radical de resgate não receberam RS-RARP, e pacientes com tumores anteriores receberam preferencialmente SA-RARP. Pacientes com seguimento inferior...
Discussão
Durante o RS-RARP, todo o procedimento é realizado aproximando-se da bexiga através da extremidade posterior. Consequentemente, a principal diferença com o SA-RARP é a preservação do espaço dos Retzius. A preservação do espaço de Retzius tem várias vantagens anatômicas7: Primeiro, a bexiga não é separada da parede abdominal e os ligamentos umbilicais não são transectados. Portanto, a bexiga permanece em sua posição anatômica. Em segundo lugar, o avental detrusor anterior e os li...
Divulgações
Os autores não têm conflitos de interesse.
Agradecimentos
Não foi obtido financiamento para esta pesquisa.
Materiais
| Name | Company | Catalog Number | Comments |
| adhesive tape | BSNmedical | 15200028 | Tensoplast |
| assistant trocar 5mm | Aesculap | EKO17R | reusable trocar |
| assistant trocar 12mm | Conmed | iAS12-120LPi | AirSeal trocar |
| barbed wire | Covidien | VLOCM0024 | for vesico-urethral anastomosis |
| Cadiere forceps | Intuitive | 470049 | robotic instrument, grasper |
| camera 30° | Intuitive | 470027 | endoscope |
| cefazolin | Sandoz | BE217296 | Belgian farmaceutical registration |
| CO2-insufflator | Conmed | AS-iFS2 | AirSeal insufflator |
| Da Vinci Xi system | Intuitive | 600062 | robotic system |
| endobag | Covidien | 173050G | Endo Catch 10mm |
| endoscopic hem-o-lok applier | Teleflex | 544995T | to apply the locking clips |
| fenestrated bipolar forceps | Intuitive | 470205 | robotic instrument, bipolar forceps |
| Hasson cone 8mm trocar | Intuitive | 470398 | only at the camera trocar |
| heparin, low molecular weight (enoxaparin) | Sanofi | BE144347 | Belgian farmaceutical registration |
| hydrogel coated latex transurethral catheter | Bard | D226416 | Biocath |
| insufflation cable | Conmed | ASM-EVAC1 | AirSeal Tri-lumen filtered tube set |
| laparoscopic grasper | Aesculap | PO235R | Atraumatic wave grasper, double action |
| large needle driver | Intuitive | 470006 | roboic instrument, needle driver |
| locking clip | Grena | 5-13mm | Click'aVplus |
| metallic clips 5mm | Aesculap | PL453SU | for vessel ligation |
| monopolar curved scissor | Intuitive | 470179 | robotic instrument, hot shears |
| mosquito clamp | Innovia Medical | MQC2025-D | to secure bladder suspension stitch |
| natriumlaurylsulfoacetate-sorbitol-natriumcitratedihydrate clysma | Johnson & Johnson Consumer BV | RVG 05069 | Belgian farmaceutical registration |
| polyglactin 3.0 suture | Ethicon | V442H | stay suture bladder neck, subcutaneous sutures |
| polyglactin 1 suture | Ethicon | D9708 | stay suture fascia and fascia closurie |
| povidone-iodine alcoholic solution | Mylan | BE230736 | Belgian farmaceutical registration |
| robotic trocar 8mm | Intuitive | 470002 | standard length |
| Skin stapler | Covidien | 8886803712 | skin closure |
| sterile drapes robotic arms | Intuitive | 470015 | draping system robotic arms |
| suction-irrigation device | Geyi | GYSL-5X330 | laparoscopic use by assitant |
| suspension sutures | Ethicon | 628H | Ethilon 2-0 nylon suture |
| thrombo-embolus deterrent stockings | Covidien | 7203 | T.E.D. stockings |
| warming blanket device | 3M | 54200 | Bear Hugger |
Referências
- Mottet, N., et al. EAU-EANM-ESTRO-ESUR-SIOG Guidelines on Prostate Cancer-2020 Update. Part 1: Screening, Diagnosis, and Local Treatment with Curative Intent. European Urology. 79 (2), 243-262 (2021).
- Ilic, D., et al. Laparoscopic and robotic-assisted versus open radical prostatectomy for the treatment of localised prostate cancer. The Cochrane Database of Systematic Reviews. 9 (9), (2017).
- Ab del Raheem, A., et al. Retzius-sparing robot-assisted radical prostatectomy versus open retropubic radical prostatectomy: a prospective comparative study with 19-month follow-up. Minerva Urologica e Nefrologica: The Italian Journal of Urology and Nephrology. 72 (5), 586-594 (2020).
- Gandaglia, G., et al. Comparative effectiveness of robot-assisted and open radical prostatectomy in the postdissemination era. Journal of Clinical Oncology : Official Journal of the American Society of Clinical Oncology. 32 (14), 1419-1426 (2014).
- Ficarra, V., et al. Systematic review and meta-analysis of studies reporting urinary continence recovery after robot-assisted radical prostatectomy. European Urology. 62 (3), 405-417 (2012).
- Martini, A., et al. Contemporary techniques of prostate dissection for robot-assisted prostatectomy. European Urology. 78 (4), 583-591 (2020).
- Galfano, A., et al. A new anatomic approach for robot-assisted laparoscopic prostatectomy: a feasibility study for completely intrafascial surgery. European Urology. 58 (3), 457-461 (2010).
- Checcucci, E., et al. Retzius-sparing robot-assisted radical prostatectomy vs the standard approach: a systematic review and analysis of comparative outcomes. BJU International. 125 (1), 8-16 (2020).
- Montorsi, F., et al. Best practices in robot-assisted radical prostatectomy: recommendations of the Pasadena Consensus Panel. European Urology. 62 (3), 368-381 (2012).
- Stabile, A., et al. Multiparametric MRI for prostate cancer diagnosis: current status and future directions. Nature Reviews. Urology. 17 (1), 41-61 (2020).
- Dindo, D., Demartines, N., Clavien, P. A. Classification of surgical complications: a new proposal with evaluation in a cohort of 6336 patients and results of a survey. Annals of Surgery. 240 (2), 205-213 (2004).
- Xylinas, E., et al. Evaluation of combined oncological and functional outcomes after radical prostatectomy: trifecta rate of achieving continence, potency and cancer control--a literature review. Urology. 76 (5), 1194-1198 (2010).
- Walz, J., et al. A critical analysis of the current knowledge of surgical anatomy related to optimization of cancer control and preservation of continence and erection in candidates for radical prostatectomy. European Urology. 57 (2), 179-192 (2010).
- Walz, J., et al. A critical analysis of the current knowledge of surgical anatomy of the prostate related to optimisation of cancer control and preservation of continence and erection in candidates for radical prostatectomy: An update. European Urology. 70 (2), 301-311 (2016).
- Albisinni, S., et al. Systematic review comparing Anterior vs Retzius-sparing robotic assisted radical prostatectomy: can the approach really make a difference. Minerva Urology and Nephrology. , (2021).
- Menon, M., et al. Functional recovery, oncologic outcomes and postoperative complications after robot-assisted radical prostatectomy: An evidence-based analysis comparing the Retzius sparing and standard approaches. The Journal of Urology. 199 (5), 1210-1217 (2018).
- Olivero, A., et al. Retzius-sparing robotic radical prostatectomy for surgeons in the learning curve: A propensity score-matching analysis. European Urology Focus. 7 (4), 772-778 (2021).
- Galfano, A., et al. Retzius-sparing robot-assisted radical prostatectomy: early learning curve experience in three continents. BJU International. 127 (4), 412-417 (2021).
- Galfano, A., et al. Beyond the learning curve of the Retzius-sparing approach for robot-assisted laparoscopic radical prostatectomy: oncologic and functional results of the first 200 patients with >/= 1 year of follow-up. European Urology. 64 (6), 974-980 (2013).
- Hoffman, K. E., et al. Patient-reported outcomes through 5 years for active surveillance, surgery, brachytherapy, or external beam radiation with or without androgen deprivation therapy for localized prostate cancer. JAMA. 323 (2), 149-163 (2020).
- Dalela, D., et al. A pragmatic randomized controlled trial examining the impact of the Retzius-sparing approach on early urinary continence recovery after robot-assisted radical prostatectomy. European Urology. 72 (5), 677-685 (2017).
- Yossepowitch, O., et al. Positive surgical margins after radical prostatectomy: a systematic review and contemporary update. European Urology. 65 (2), 303-313 (2014).
- Vale, C. L., et al. Adjuvant or early salvage radiotherapy for the treatment of localised and locally advanced prostate cancer: a prospectively planned systematic review and meta-analysis of aggregate data. Lancet. 396 (10260), 1422-1431 (2020).
- Lumen, N., et al. Safe introduction of robot-assisted radical prostatectomy after a training program in a high-volume robotic centre. Urologia Internationalis. 91 (2), 145-152 (2013).
- Galfano, A., Secco, S., Bocciardi, A. M. Mottrie A. Retzius-sparing robot-assisted laparoscopic radical prostatectomy: An international survey on surgical details and worldwide diffusion. European Urology Focus. 6 (5), 1021-1023 (2020).
- Checcucci, E., et al. Precision prostate cancer surgery: an overview of new technologies and techniques. Minerva Urologica e Nefrologica: The Italian Journal of Urology and Nephrology. 71 (5), 487-501 (2019).
- Grasso, A. A., et al. Posterior musculofascial reconstruction after radical prostatectomy: an updated systematic review and a meta-analysis. BJU International. 118 (1), 20-34 (2016).
- Manfredi, M., et al. Total anatomical reconstruction during robot-assisted radical prostatectomy: focus on urinary continence recovery and related complications after 1000 procedures. BJU international. 124 (3), 477-486 (2019).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados