È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Prostatectomia radicale assistita da robot risparmiatrice di retzius
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
La prostatectomia radicale Retzius-sparing assistita da robot è una tecnica che consente di preservare la continenza urinaria o facilita il recupero della continenza urinaria nella maggior parte dei pazienti. I pazienti devono essere informati del rischio di un margine chirurgico positivo.
Abstract
Vengono fornite la tecnica della prostatectomia radicale assistita da robot risparmiatrice di Retzius (RS-RARP) e l'esperienza iniziale con essa in un singolo centro. La tecnica è descritta passo dopo passo e ulteriormente illustrata da un video per migliorare la riproducibilità. Sono stati valutati i primi risultati oncologici e funzionali. In totale, sono stati inclusi 77 pazienti con un follow-up mediano di 11 mesi (range: 3-21 mesi). Il cinquantuno per cento dei pazienti aveva un cancro alla prostata locale ad alto rischio o localmente avanzato. Non ci sono state complicanze intraoperatorie e tutte le complicanze di alto grado (2,6%) erano correlate alla dissezione dei linfonodi pelvici eseguita in concomitanza con RS-RARP. Il tempo medio di intervento è stato di 160 minuti (range: 122-265 min) e la degenza ospedaliera mediana è stata di 3 (range: 3-8) giorni. Un margine chirurgico positivo è stato riportato nel 42,9%. La sopravvivenza libera da recidiva biochimica a un anno è stata del 90,1%. Dopo 6 mesi, tutti i pazienti erano socialmente continentali e dopo 1 anno, il 94,3% era completamente continentale. Dei pazienti sessualmente attivi che hanno subito almeno un risparmio nervoso unilaterale, il 43,3% è stato in grado di avere rapporti sessuali. Questa serie sottolinea la sicurezza chirurgica dell'esecuzione di RS-RARP con una tecnica standardizzata e conferma l'effetto benefico sul ritorno precoce della continenza. Il paziente deve essere informato sul rischio di un margine chirurgico positivo.
Introduzione
Per curare casi localizzati e selezionati di carcinoma prostatico localmente avanzato, la prostatectomia radicale è una delle opzioni di trattamento raccomandate1. Le tecniche mini-invasive (laparoscopia convenzionale e laparoscopia robot-assistita) hanno il vantaggio di ridurre la perdita di sangue, il dolore postoperatorio e la durata del ricovero in ospedale rispetto alla prostatectomia radicale aperta 2,3. Tra le tecniche minimamente invasive, la chirurgia robot-assistita combina i vantaggi della chirurgia mini-invasiva con una maggiore destrezza e libertà di movimento degli strumenti chirurgici e con una visione perioperatoria 3-dimensionale. Nei paesi dotati di risorse adeguate, la prostatectomia radicale assistita da robot (RARP) è diventata la modalità predominante per eseguire la prostatectomia radicale4.
L'incontinenza urinaria, temporanea o definitiva, è un effetto collaterale comune della prostatectomia radicale, indipendentemente dalla modalità con cui è stata eseguita5. Con RARP anteriore aperto (addominale), laparoscopico e "standard" (SA-RARP), la prostatectomia radicale viene eseguita con un approccio anteriore in cui viene aperto lo spazio retropubico (Retzius)6. Grazie alla maggiore destrezza associata alla RARP, è possibile un approccio anatomico alternativo in cui la prostata viene resecata attraverso la sacca rettovescicale o la sacca di Douglas come descritto per la prima volta da Galfano et al.7. Questo approccio posteriore lascia intatto lo spazio di Retzius ("Retzius-sparing RARP"; RS-RARP). Il vantaggio principale di RS-RARP sembra essere un recupero più elevato e più rapido della continenza urinaria8. Questo studio si propone di descrivere in dettaglio (come suggerito dal Pasadena consensus panel9) le fasi di RS-RARP supportate da materiale audiovisivo e di riferire sugli esiti funzionali e oncologici precoci dei primi casi in un unico centro.
Protocollo
Questo studio è stato presentato al comitato etico locale dell'ospedale universitario di Gand ed è stata concessa l'approvazione istituzionale (EC UZG 2019/1506). Lo studio è stato registrato nel registro di studi belga con il riferimento B670201941650. Tutti i pazienti hanno fornito il consenso informato scritto.
1. Preparazione e posizionamento del paziente
- Preparazione
- Seguire le linee guida contemporanee accettate a livello internazionale per diagnosticare il cancro alla prostata e impostare l'indicazione per la prostatectomia radicale1. Utilizzare la risonanza magnetica multiparametrica per la stadiazione locale in quanto fornisce informazioni importanti sul volume della prostata, l'allargamento concomitante della prostata e il lobo mediano, nonché la posizione e l'estensione del tumore. Ciò aiuterà nella decisione se eseguire nerve-sparing e / o bladder-neck-sparing10. Assicurarsi che questa immagine sia disponibile al momento dell'operazione.
- Offrire RS-RARP a pazienti con carcinoma prostatico locale o localmente avanzato e un'aspettativa di vita >10 anni. Discutere opzioni di trattamento alternative come la sorveglianza attiva, altre modalità di prostatectomia radicale e irradiazione ove applicabile. Non offrire RS-RARP a pazienti con carcinoma prostatico metastatico.
- Escludere condizioni mediche che sono una controindicazione per la chirurgia robotica in posizione ripida di Trendelenburg mediante esame anestesiologico preoperatorio. Se queste condizioni mediche sono presenti, trattarle prima (se possibile) o discutere un trattamento alternativo con il paziente. Includere il tipo e lo schermo del sangue del paziente nella valutazione preoperatoria nel raro caso in cui sia necessaria una trasfusione di sangue.
- Somministrare natriumlaurylsulfoacetate-sorbitolo-natriumcitrate dihydrate clysma 4-8 h prima dell'operazione per pulire il retto. Consentire l'assunzione di cibo e l'assunzione di liquidi chiari fino a 6 ore e 4 ore prima dell'induzione, rispettivamente.
- Eseguire l'anestesia generale con intubazione endotracheale. Somministrare un colpo profilattico a colpo singolo di cefazolina 2g all'induzione.
- Inserire una linea endovenosa periferica di grande calibro e una linea arteriosa per garantire l'accesso e il monitoraggio del sistema circolatorio. Utilizzare pulsossimetria e monitoraggio cardiaco a 4 derivazioni durante l'intera procedura.
- Posizionamento
- Posizionare il paziente in posizione supina. Posizionare e fissare le braccia lungo il corpo del paziente e fissare le gambe con una cinghia a livello delle ginocchia. Fissare eventuali punti di compressione con cuscinetti in gel.
NOTA: Il paziente indossa calze dissuasive per trombo-emboli. - Applicare i supporti per le spalle per evitare spostamenti dovuti alla ripida posizione di Trendelenburg. Fissare il torace del paziente al tavolo con nastro adesivo (larghezza 7,5 cm) per evitare ulteriori spostamenti. Coprire il paziente con un dispositivo di coperta riscaldante toracica.
- Disinfettare il campo chirurgico con soluzione alcolica povidone-iodio o, in alternativa, con clorexidina in caso di allergia allo iodio. Includere l'addome anteriore, l'inguine e i genitali nel campo chirurgico. Attaccare tende sterili ai bordi del campo dopo la disinfezione.
- Posizionare un catetere transuretrale in lattice rivestito di idrogel 16 F per garantire il drenaggio urinario e lo svuotamento della vescica al momento dell'inserimento del trocar. Assicurarsi di avere un facile accesso al catetere transuretrale in quanto aiuterà nell'identificazione dell'uretra più tardi durante la procedura.
- Posizionare il paziente in posizione supina. Posizionare e fissare le braccia lungo il corpo del paziente e fissare le gambe con una cinghia a livello delle ginocchia. Fissare eventuali punti di compressione con cuscinetti in gel.
2. Aggancio del sistema robotico
- Coprire i bracci robotici del carrello paziente con teli sterili in quanto saranno successivamente a contatto con il campo chirurgico. Utilizzare una fotocamera a 30°.
NOTA: per questa operazione viene utilizzato il sistema Da Vinci Xi (Figura 1). Questo sistema è costituito da tre parti fondamentali: una console chirurgica che viene posizionata a una distanza dal tavolo operatorio; un carrello paziente con quattro bracci robotici che saranno agganciati ai trocar e un carrello di visione con il monitor per scrub infermiere e assistente, sistema di elettrocauterizzazione e CO 2-insufflatore posto accanto al paziente. - Inserimento trocar
- Inserimento della telecamera trocar
- Fare un'incisione cutanea longitudinalmente su 2-2,5 cm circa 1 cm sopra l'ombelico. Sezionare il tessuto adiposo sottocutaneo senza mezzi termini fino a identificare la fascia del retto.
- Incidere longitudinalmente la fascia retta e posizionare le suture di poliglactina 1 riassunibile sulla fascia su entrambi i lati.
- Apri il peritoneo con le forbici. Assicurati con la palpazione digitale con il dito indice che non ci sia contatto dell'intestino con questa apertura.
- Inserire un trocar robotico da 8 mm con cono di Hasson nella cavità peritoneale. Attaccare i morsetti dei coni alle suture di soggiorno alla fascia.
- Collegare il trocar della telecamera all'insufflatore CO2 e gonfiare a una pressione di 12-15 mmHg. Portare il paziente nella posizione di 30-35° Trendelenburg per liberare il bacino minore dall'intestino tenue. Assicurarsi che non vi sia spostamento del corpo durante il ripido posizionamento di Trendelenburg.
- Posizionare al livello orizzontale del trocar telecamera, due e uno trocar da 8 mm per gli strumenti robotici, rispettivamente, ai lati sinistro e destro del trocar della telecamera con una distanza di 6-8 cm tra i trocar robotici. Posiziona tutti i trocar sotto la visione diretta con la fotocamera. Utilizzare l'otturatore a punta smussata per posizionare i trocar.
- Posizionare un trocar assistente di 5 mm a 5 cm cranialmente sulla linea mediana tra il trocar della telecamera e il trocar robotico destro. Posizionare un assistente trocar di 12 mm 3 cm sopra la spina iliaca anteriore superiore.
NOTA: L'assistente è sul lato destro del paziente mentre l'infermiera dello scrub è sul lato sinistro del paziente. - Scollegare il cavo di insufflazione al trocar della telecamera e collegarlo al trocar assistente da 12 mm.
- Inserimento della telecamera trocar
- Aggancio del carrello paziente e inserimento di strumenti robotici
- Spostare il carrello paziente sul lato destro del paziente fino a quando il terzo braccio può essere collegato al trocar della telecamera. Ottimizzare ulteriormente il posizionamento del carrello paziente utilizzando l'applicazione automatica del sistema. Collegare gli altri tre trocar da 8 mm con una distanza di almeno 10 cm tra i bracci per evitare collisioni durante i movimenti operativi.
- Utilizzare come strumenti robotici, una forbice curva monopolare, una pinza bipolare fenestrata, una pinza Cadiere e un grande ago. All'inizio dell'operazione, posizionare la forbice monopolare nel trocar robotico destro, la pinza bipolare fenestrata nel trocar robotico sinistro mediale e la pinza Cadiere nel trocar robotico sinistro laterale.
- Controllare l'inserimento di strumenti robotici mediante una visione diretta per evitare perforazioni di visceri, aderenze omentali o strutture vascolari.
- Come strumenti assistenti, utilizzare un dispositivo laparoscopico di aspirazione-irrigazione posizionato nel trocar assistente da 5 mm e un rampino laparoscopico posizionato nel trocar assistente da 12 mm. Prendere posto nella console del chirurgo per avviare la parte assistita da robot dell'operazione.
NOTA: Questi strumenti laparoscopici sono maneggiati dall'assistente e non sono collegati a bracci robotici.
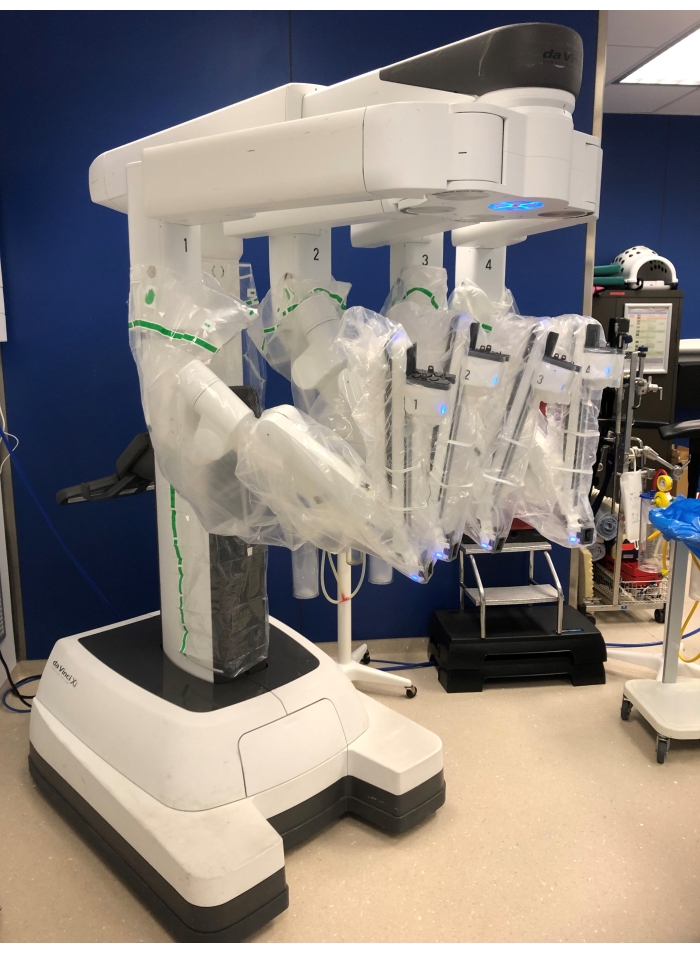
Figura 1: Il carrello paziente con 4 bracci robotici. Fare clic qui per visualizzare una versione ingrandita di questa figura.
3. Dissezione delle vescicole seminali
- Accesso al bacino minore
- Eseguire l'adesiolisi rilasciando eventuali aderenze che ostacolano un facile accesso alla pelvi minore e alla sacca rettovesicale. Eseguire questa adesiolisi con la lente ruotata di 30° verso il basso.
- Facilitare l'accesso alla sacca rettovescicale (o Douglas) spingendo la vescica verso l'alto con la pinza Cadiere e spingendo il retto verso il basso con il dispositivo di aspirazione-irrigazione.
- Accesso alle vescicole seminali
- Incidi il peritoneo sopra i dotti deferenti su entrambi i lati e continua medialmente fino a quando queste incisioni non si raggiungono l'un l'altra.
NOTA: Il dotto deferente è più facilmente identificabile quando attraversa i vasi iliaci esterni, specialmente negli uomini obesi. - Sul bordo laterale dell'incisione, sezionare i dotti deferenti in modo circonferenziale e transetto. Sezionare medialmente il dotto deferente fino a raggiungere la punta della vescicale seminale.
- Incidi il peritoneo sopra i dotti deferenti su entrambi i lati e continua medialmente fino a quando queste incisioni non si raggiungono l'un l'altra.
- Dissezione delle vescicole seminali
- Staccare medialmente la fascia di Denonvilliers dal dotto deferente nel caso in cui non vi siano prove di invasione della vescicola seminale. Se si sospetta un'invasione della vescicola seminale, incidere la fascia di Denonvilliers 1-2 mm sotto il bordo inferiore della vescicola seminale per garantire un margine chirurgico sicuro.
- Fissare i vasi dove entrano sulla punta e sulla superficie laterale della vescicola seminale mediante emostasi bipolare o con clip metalliche da 5 mm e transetto. Continuare questa dissezione fino a raggiungere la base della prostata. Eseguire la stessa procedura sul lato opposto.
NOTA: I nervi erettili sono vicini alla punta e alla superficie laterale delle vescicole seminali e la coagulazione monopolare dovrebbe essere evitata nel caso in cui si tenti di risparmiare il nervo.
4. Dissezione posterolaterale della prostata
- Dissezione laterale della prostata
- Ritrarre medialmente la vescicola seminale con la pinza Cadiere per il lato destro e con l'assistente laparoscopica per il lato sinistro. Ciò consente la visualizzazione del tessuto adiposo in un triangolo tra la base della vescicola seminale e la regione laterale alla base della prostata.
NOTA: Questo triangolo è appena sopra i nervi erettili e il peduncolo prostatico. - Eseguire la dissezione smussata in questo tessuto adiposo lungo la superficie laterale della prostata fino a quando non si incontra il riflesso della fascia endopelvica. Eseguire l'emostasi dal forcipe bipolare poiché la corrente monopolare potrebbe danneggiare i nervi erettili.
- Ritrarre medialmente la vescicola seminale con la pinza Cadiere per il lato destro e con l'assistente laparoscopica per il lato sinistro. Ciò consente la visualizzazione del tessuto adiposo in un triangolo tra la base della vescicola seminale e la regione laterale alla base della prostata.
- Sospensione del peritoneo
- Facilitare l'accesso alla prostata e al collo della vescica mediante due suture di sospensione attraverso la parte superiore dell'incisione peritoneale.
- Inserire il grande ago nel braccio robotico destro. Posizionare un ago dritto con una sutura non riassorbibile attraverso la parete addominale 2-3 cm sopra l'osso pubico appena medialmente dal legamento ombelicale mediale.
- Perforare la parte superiore dell'incisione peritoneale e il tessuto adiposo sottostante con l'ago dritto. Riportare l'ago all'esterno del corpo vicino al tratto di inserimento. Tenere questo punto di sospensione sotto tensione usando un morsetto antizanzara all'esterno dell'addome. Fai lo stesso sul lato controlaterale.
- Dissezione posteriore della prostata
- Rimuovere il driver dell'ago e riportare le forbici curve nel braccio robotico destro. Ritrarre le vescicole seminali verso l'alto e leggermente lateralmente con la pinza Cadiere e la pinza laparoscopica assistente per i lati sinistro e destro, rispettivamente, per portare la fascia di Denonvilliers sotto tensione.
- Gestione dei nervi erettili.
- Approccio bilaterale nerve-sparing: sviluppare un piano mediante dissezione smussata tra la fascia prostatica e la fascia di Denonvilliers fino all'apice della prostata e lateralmente fino a quando non si incontrano i vasi prostatici.
- Approccio non risparmiatore di nervi: incidere la fascia di Denonvilliers 1-2 mm sotto la base della prostata. Sezionare la superficie anteriore del retto e più lateralmente nel tessuto adiposo perirettale.
- Approccio unilaterale nerve-sparing: eseguire il passo 4.3.2.1 nel sito di nerve-sparing e il passaggio 4.3.2.2 nel sito di non-nerve sparing. Incidi la fascia di Denonvilliers sulla linea mediana sopra la parete rettale.
- Emostasi del peduncolo prostatico e dissezione del fascio neurovascolare
- Accesso al lato destro: afferrare la base della prostata con la pinza Cadiere appena sotto l'attacco della vescicola seminale omolaterale. Ritrarre la base della prostata medialmente e leggermente verso l'alto per portare il peduncolo prostatico in tensione.
- Crea una finestra con le forbici monopolari nel peduncolo prostatico e fissa questa parte del peduncolo usando una grande clip di bloccaggio in polimero che viene applicata attraverso i pantaloni assistenti da 12 mm. Transetto questa parte del peduncolo sul lato prostatico della clip.
- Ripetere 4.4.2 (di solito 2-3 volte) fino a quando l'intero peduncolo prostatico è fissato. Mantenere la tensione sul peduncolo prostatico dopo ogni volta che una parte del peduncolo viene transettata.
- Ripetere il passaggio 4.4.2 fino a raggiungere l'apice della prostata. Mantenere una distanza di sicurezza dalla superficie prostatica ogni volta che viene creata una finestra.
NOTA: Questo sacrificherà il fascio neurovascolare contenente i nervi erettili. - Staccare il fascio neurovascolare dalla fascia prostatica mediante dissezione smussata e mantenendo il fascio sotto leggera tensione utilizzando una progressiva retrazione mediale e verso l'alto con la pinza Cadiere.
- Fissare piccoli vasi attaccati alla prostata con clip metalliche da 5 mm e transettorli con le forbici. Procedere fino a raggiungere l'apice della prostata. Garantire l'aspirazione e l'irrigazione da parte dell'assistente attraverso il trocar da 5 mm ogni volta che è necessario.
- Accesso al lato sinistro: commutare la pinza Cadiere al trocar sinistro mediale e la pinza bipolare fenestrata al trocar laterale sinistro. Ritrarre la base della prostata medialmente e verso l'alto. Utilizzare l'endopolso dello strumento per creare un angolo di 90° verso il basso sotto il quale l'assistente ha un facile accesso per posizionare le clip. Ripetere la procedura sul lato sinistro come descritto sopra (punti da 4.4.2 a 4.4.6).
5. Dissezione del collo della vescica
- Afferrare le vescicole seminali con la pinza Cadiere e ritrarle verso il basso per creare tensione tra il collo della vescica e la base della prostata.
- Sviluppare il piano tra il collo della vescica e la base della prostata usando una combinazione di incisioni monopolari con le forbici e la dissezione smussata. Preservare le fibre muscolari circolari del collo della vescica in caso di risparmio del collo della vescica. Spostare le vescicole seminali più lateralmente per facilitare la dissezione laterale del collo della vescica.
- Apertura del collo della vescica
- Incidere la mucosa all'aspetto posteriore del collo della vescica oltre 1 cm. Visualizza il catetere uretrale.
- Posizionare una sutura di poliglactina 3-0 assorbibile nella parte posteriore del collo della vescica. Sgonfiare il palloncino del catetere e ritrarre il catetere.
- Afferrare la sutura di soggiorno con la pinza bipolare fenestrata e spostarsi verso l'alto fino a quando la parte anteriore del collo della vescica diventa visibile. Incidere ulteriormente la mucosa e rilasciare il collo della vescica dalla base della prostata.
- Posizionare una seconda sutura di soggiorno sull'aspetto anteriore del collo della vescica con una sutura riassorbibile di poliglactina 3-0 appena prima che il collo della vescica sia completamente rilasciato.
NOTA: Queste suture di soggiorno faciliteranno l'identificazione successiva del collo vescicale per l'anastomosi vescico-uretrale.
6. Dissezione dell'apice anteriore e prostatico
- Dissezione anteriore
- Continuare una leggera tensione verso l'alto alla sutura di soggiorno sull'aspetto posteriore della vescica con il forcipe bipolare fenestrato. Posizionare la pinza Cadiere nell'uretra prostatica e applicare la trazione verso il basso per creare tensione sulla superficie anteriore della prostata.
- Seguire la superficie anteriore della prostata usando una combinazione di dissezione smussata e incisione monopolare risparmiando il plesso di Santorini, i legamenti puboprostatici e lo spazio di Retzius. Spostare la pinza Cadiere lateralmente per facilitare la dissezione anterolaterale.
- Dissezione dell'apice prostatico
- Identificare l'uretra membranosa afferrando il catetere uretrale con la pinza Cadiere.
- Incidere le fibre circolari dell'uretra caudalmente di 1-2 mm all'apice della prostata. Spingere le fibre circolari verso l'apice della prostata per esporre lo strato longitudinale interno dell'uretra (il cosiddetto lissosfintere). Transect questo strato interno il più vicino possibile alla prostata per preservare al massimo il lissosfintere.
- Incidere eventuali attacchi dorsalmente all'uretra membranosa fino a quando la prostata non è completamente liberata dai tessuti circostanti. Inserire una sacca endobag attraverso il trocar assistente da 12 mm da inserire nella prostata (e nelle vescicole seminali). Chiudere l'endobag e lasciarlo chiuso nella fossa iliaca destra.
7. Anastomosi vescico-uretrale
- Posizionare il grande ago nel trocar robotico destro e la pinza Cadiere e la pinza bipolare fenestrata, rispettivamente, nel trocar robotico sinistro mediale e laterale. Utilizzare la pinza bipolare fenestrata per spingere delicatamente la vescica verso l'uretra al fine di ridurre la tensione all'anastomosi.
- Sutura dell'anastomosi vescico-uretrale
- Posizionare la prima sutura del primo filo spinato riassorbibile (3-0, 23 cm di lunghezza) all'esterno-in appena lateralmente a destra della posizione a ore 12 sul collo della vescica. Tirare la sutura anteriore che è stata posizionata nel punto 5.3.4 per identificare il collo della vescica e la mucosa della vescica.
- Posizionare la sutura al rovescio sull'uretra, anche leggermente laterale a destra della posizione a ore 12. Identificare l'uretra spostando la punta del catetere uretrale nell'uretra membranosa.
- Posizionare la prima sutura del secondo filo spinato riassorbibile (3-0, 23 cm di lunghezza) all'esterno-in appena lateralmente a sinistra della posizione a ore 12 sul collo della vescica e all'interno verso l'esterno sull'uretra nella stessa posizione.
- Per la sutura posteriore sul lato sinistro, approssimare la mucosa della vescica contro la mucosa uretrale mediante trazione progressiva su entrambe le estremità dei fili spinati. Ripetere la sutura con il secondo filo spinato all'esterno-dentro sul collo della vescica e all'interno verso l'esterno sull'uretra due volte, momento in cui viene raggiunta la posizione a ore 9. Approssimare la mucosa della vescica contro la mucosa uretrale dopo ogni sutura.
- Per la sutura sul lato destro, eseguire la sutura con il primo filo spinato all'esterno-dentro sul collo della vescica e all'interno verso l'esterno sull'uretra, fino a raggiungere la posizione a ore 6. Non approssimare ancora l'ultima sutura per lasciare spazio per finalizzare il lato sinistrorso dell'anastomosi.
- Per la sutura anteriore sul lato sinistro, continuare l'anastomosi sul lato sinistro passando dalla posizione delle ore 9 alle ore 6. Non approssimare ancora l'ultima sutura per consentire alla punta del catetere di passare tra i fili spinati sinistro e destro.
- Afferrare la punta del catetere e posizionarlo nella vescica. Insurriscaldare il palloncino.
- Stringere le ultime suture sui lati sinistro e destro fino a quando la vescica e la mucosa uretrale sono approssimate. Controllare la tenuta stagna dell'anastomosi instillando 120 ml di acqua nella vescica (prova di tenuta).
- Posizionare la prima sutura del primo filo spinato riassorbibile (3-0, 23 cm di lunghezza) all'esterno-in appena lateralmente a destra della posizione a ore 12 sul collo della vescica. Tirare la sutura anteriore che è stata posizionata nel punto 5.3.4 per identificare il collo della vescica e la mucosa della vescica.
- Rimuovere le suture di sospensione nella parte superiore dell'incisione peritoneale. Utilizzare i resti dei fili spinati per chiudere l'incisione peritoneale da mediale a laterale su entrambi i lati. Eseguire una dissezione bilaterale dei linfonodi pelvici se indicato dalle linee guida contemporanee accettate a livello internazionale1.
NOTA: Non viene lasciato alcun drenaggio chirurgico nel caso in cui non sia stata eseguita la dissezione dei linfonodi pelvici.
8. Estrazione della prostata e chiusura delle incisioni
- Trasferire il filo di estrazione dell'endobag dal trocar robotico destro al trocar della telecamera sotto visione diretta.
- Sgonfiare l'addome e rimuovere i trocar sotto visione diretta. Cambiare la posizione di Trendelenburg nella posizione supina neutra. Incidere ulteriormente l'incisione cutanea sopra-ombelicale e l'incisione della fascia per consentire una facile estrazione della prostata.
NOTA: La dimensione di questa incisione dipende dalla dimensione della prostata. - Chiudere la fascia del retto con una sutura riassorbibile di poliglactina 1. Chiudere il tessuto sottocutaneo alla telecamera trocar e 12 mm assistente trocar con sutura 3-0 poliglactina riassorbibile. Chiudere tutte le incisioni cutanee con cucitrici cutanee.
9. Cure postoperatorie
- Trasferire il paziente nell'unità di cura postoperatoria e monitorare per 2-3 ore. Trasferire il paziente all'unità di ricovero dopo l'approvazione da parte dell'anestesista e del chirurgo.
- Consentire al paziente di riprendere l'assunzione di liquidi chiari. Consentire l'assunzione di cibo solido e stimolare a camminare durante il primo giorno postoperatorio. Rimuovere il catetere uretrale al terzo giorno postoperatorio e misurare il volume di minzione e il volume residuo della vescica. Sostituire il catetere in caso di volume residuo sostanziale e rimuoverlo presso il policlinico 1 settimana dopo.
- Dimettere il paziente il terzo giorno postoperatorio. Rimuovere le cucitrici cutanee tra il 10° e il 14°giorno postoperatorio dal medico di medicina generale. Somministrare eparina a basso peso molecolare per via sottocutanea fino al 20° giorno postoperatorio da un'infermiera a casa o dal paziente stesso.
Risultati
A tutti i pazienti con carcinoma prostatico locale o localmente avanzato con un'aspettativa di vita >10 anni e senza controindicazioni anestesiologiche è stato offerto RS-RARP come una delle opzioni di trattamento per la loro malattia. Ai pazienti sottoposti a prostatectomia radicale citoriduttiva per carcinoma prostatico metastatico nel contesto di uno studio clinico o di una prostatectomia radicale di salvataggio non è stata offerta RS-RARP, e ai pazienti con tumori anteriori è stato preferibilmente offerto SA-RARP....
Discussione
Durante RS-RARP, l'intera procedura viene eseguita avvicinandosi alla vescica attraverso l'estremità posteriore. Di conseguenza, la principale differenza con SA-RARP è la conservazione dello spazio di Retzius. La conservazione dello spazio di Retzius ha diversi vantaggi anatomici7: In primo luogo, la vescica non viene staccata dalla parete addominale e i legamenti ombelicali non vengono transettati. Pertanto, la vescica rimane nella sua posizione anatomica. In secondo luogo, il grembiule del det...
Divulgazioni
Gli autori non hanno conflitti di interesse.
Riconoscimenti
Nessun finanziamento è stato ottenuto per questa ricerca.
Materiali
| Name | Company | Catalog Number | Comments |
| adhesive tape | BSNmedical | 15200028 | Tensoplast |
| assistant trocar 5mm | Aesculap | EKO17R | reusable trocar |
| assistant trocar 12mm | Conmed | iAS12-120LPi | AirSeal trocar |
| barbed wire | Covidien | VLOCM0024 | for vesico-urethral anastomosis |
| Cadiere forceps | Intuitive | 470049 | robotic instrument, grasper |
| camera 30° | Intuitive | 470027 | endoscope |
| cefazolin | Sandoz | BE217296 | Belgian farmaceutical registration |
| CO2-insufflator | Conmed | AS-iFS2 | AirSeal insufflator |
| Da Vinci Xi system | Intuitive | 600062 | robotic system |
| endobag | Covidien | 173050G | Endo Catch 10mm |
| endoscopic hem-o-lok applier | Teleflex | 544995T | to apply the locking clips |
| fenestrated bipolar forceps | Intuitive | 470205 | robotic instrument, bipolar forceps |
| Hasson cone 8mm trocar | Intuitive | 470398 | only at the camera trocar |
| heparin, low molecular weight (enoxaparin) | Sanofi | BE144347 | Belgian farmaceutical registration |
| hydrogel coated latex transurethral catheter | Bard | D226416 | Biocath |
| insufflation cable | Conmed | ASM-EVAC1 | AirSeal Tri-lumen filtered tube set |
| laparoscopic grasper | Aesculap | PO235R | Atraumatic wave grasper, double action |
| large needle driver | Intuitive | 470006 | roboic instrument, needle driver |
| locking clip | Grena | 5-13mm | Click'aVplus |
| metallic clips 5mm | Aesculap | PL453SU | for vessel ligation |
| monopolar curved scissor | Intuitive | 470179 | robotic instrument, hot shears |
| mosquito clamp | Innovia Medical | MQC2025-D | to secure bladder suspension stitch |
| natriumlaurylsulfoacetate-sorbitol-natriumcitratedihydrate clysma | Johnson & Johnson Consumer BV | RVG 05069 | Belgian farmaceutical registration |
| polyglactin 3.0 suture | Ethicon | V442H | stay suture bladder neck, subcutaneous sutures |
| polyglactin 1 suture | Ethicon | D9708 | stay suture fascia and fascia closurie |
| povidone-iodine alcoholic solution | Mylan | BE230736 | Belgian farmaceutical registration |
| robotic trocar 8mm | Intuitive | 470002 | standard length |
| Skin stapler | Covidien | 8886803712 | skin closure |
| sterile drapes robotic arms | Intuitive | 470015 | draping system robotic arms |
| suction-irrigation device | Geyi | GYSL-5X330 | laparoscopic use by assitant |
| suspension sutures | Ethicon | 628H | Ethilon 2-0 nylon suture |
| thrombo-embolus deterrent stockings | Covidien | 7203 | T.E.D. stockings |
| warming blanket device | 3M | 54200 | Bear Hugger |
Riferimenti
- Mottet, N., et al. EAU-EANM-ESTRO-ESUR-SIOG Guidelines on Prostate Cancer-2020 Update. Part 1: Screening, Diagnosis, and Local Treatment with Curative Intent. European Urology. 79 (2), 243-262 (2021).
- Ilic, D., et al. Laparoscopic and robotic-assisted versus open radical prostatectomy for the treatment of localised prostate cancer. The Cochrane Database of Systematic Reviews. 9 (9), (2017).
- Ab del Raheem, A., et al. Retzius-sparing robot-assisted radical prostatectomy versus open retropubic radical prostatectomy: a prospective comparative study with 19-month follow-up. Minerva Urologica e Nefrologica: The Italian Journal of Urology and Nephrology. 72 (5), 586-594 (2020).
- Gandaglia, G., et al. Comparative effectiveness of robot-assisted and open radical prostatectomy in the postdissemination era. Journal of Clinical Oncology : Official Journal of the American Society of Clinical Oncology. 32 (14), 1419-1426 (2014).
- Ficarra, V., et al. Systematic review and meta-analysis of studies reporting urinary continence recovery after robot-assisted radical prostatectomy. European Urology. 62 (3), 405-417 (2012).
- Martini, A., et al. Contemporary techniques of prostate dissection for robot-assisted prostatectomy. European Urology. 78 (4), 583-591 (2020).
- Galfano, A., et al. A new anatomic approach for robot-assisted laparoscopic prostatectomy: a feasibility study for completely intrafascial surgery. European Urology. 58 (3), 457-461 (2010).
- Checcucci, E., et al. Retzius-sparing robot-assisted radical prostatectomy vs the standard approach: a systematic review and analysis of comparative outcomes. BJU International. 125 (1), 8-16 (2020).
- Montorsi, F., et al. Best practices in robot-assisted radical prostatectomy: recommendations of the Pasadena Consensus Panel. European Urology. 62 (3), 368-381 (2012).
- Stabile, A., et al. Multiparametric MRI for prostate cancer diagnosis: current status and future directions. Nature Reviews. Urology. 17 (1), 41-61 (2020).
- Dindo, D., Demartines, N., Clavien, P. A. Classification of surgical complications: a new proposal with evaluation in a cohort of 6336 patients and results of a survey. Annals of Surgery. 240 (2), 205-213 (2004).
- Xylinas, E., et al. Evaluation of combined oncological and functional outcomes after radical prostatectomy: trifecta rate of achieving continence, potency and cancer control--a literature review. Urology. 76 (5), 1194-1198 (2010).
- Walz, J., et al. A critical analysis of the current knowledge of surgical anatomy related to optimization of cancer control and preservation of continence and erection in candidates for radical prostatectomy. European Urology. 57 (2), 179-192 (2010).
- Walz, J., et al. A critical analysis of the current knowledge of surgical anatomy of the prostate related to optimisation of cancer control and preservation of continence and erection in candidates for radical prostatectomy: An update. European Urology. 70 (2), 301-311 (2016).
- Albisinni, S., et al. Systematic review comparing Anterior vs Retzius-sparing robotic assisted radical prostatectomy: can the approach really make a difference. Minerva Urology and Nephrology. , (2021).
- Menon, M., et al. Functional recovery, oncologic outcomes and postoperative complications after robot-assisted radical prostatectomy: An evidence-based analysis comparing the Retzius sparing and standard approaches. The Journal of Urology. 199 (5), 1210-1217 (2018).
- Olivero, A., et al. Retzius-sparing robotic radical prostatectomy for surgeons in the learning curve: A propensity score-matching analysis. European Urology Focus. 7 (4), 772-778 (2021).
- Galfano, A., et al. Retzius-sparing robot-assisted radical prostatectomy: early learning curve experience in three continents. BJU International. 127 (4), 412-417 (2021).
- Galfano, A., et al. Beyond the learning curve of the Retzius-sparing approach for robot-assisted laparoscopic radical prostatectomy: oncologic and functional results of the first 200 patients with >/= 1 year of follow-up. European Urology. 64 (6), 974-980 (2013).
- Hoffman, K. E., et al. Patient-reported outcomes through 5 years for active surveillance, surgery, brachytherapy, or external beam radiation with or without androgen deprivation therapy for localized prostate cancer. JAMA. 323 (2), 149-163 (2020).
- Dalela, D., et al. A pragmatic randomized controlled trial examining the impact of the Retzius-sparing approach on early urinary continence recovery after robot-assisted radical prostatectomy. European Urology. 72 (5), 677-685 (2017).
- Yossepowitch, O., et al. Positive surgical margins after radical prostatectomy: a systematic review and contemporary update. European Urology. 65 (2), 303-313 (2014).
- Vale, C. L., et al. Adjuvant or early salvage radiotherapy for the treatment of localised and locally advanced prostate cancer: a prospectively planned systematic review and meta-analysis of aggregate data. Lancet. 396 (10260), 1422-1431 (2020).
- Lumen, N., et al. Safe introduction of robot-assisted radical prostatectomy after a training program in a high-volume robotic centre. Urologia Internationalis. 91 (2), 145-152 (2013).
- Galfano, A., Secco, S., Bocciardi, A. M. Mottrie A. Retzius-sparing robot-assisted laparoscopic radical prostatectomy: An international survey on surgical details and worldwide diffusion. European Urology Focus. 6 (5), 1021-1023 (2020).
- Checcucci, E., et al. Precision prostate cancer surgery: an overview of new technologies and techniques. Minerva Urologica e Nefrologica: The Italian Journal of Urology and Nephrology. 71 (5), 487-501 (2019).
- Grasso, A. A., et al. Posterior musculofascial reconstruction after radical prostatectomy: an updated systematic review and a meta-analysis. BJU International. 118 (1), 20-34 (2016).
- Manfredi, M., et al. Total anatomical reconstruction during robot-assisted radical prostatectomy: focus on urinary continence recovery and related complications after 1000 procedures. BJU international. 124 (3), 477-486 (2019).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon