É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Análise de Infecção de Células Epiteliais com Shigella
Neste Artigo
Resumo
O presente protocolo descreve ensaios de infecção para interrogar a adesão, invasão e replicação intracelular de Shigella usando linhagens celulares epiteliais in vitro .
Resumo
O patógeno bacteriano entérico adaptado ao ser humano Shigella causa milhões de infecções a cada ano, cria efeitos de crescimento a longo prazo entre pacientes pediátricos e é uma das principais causas de mortes diarreicas em todo o mundo. A infecção induz diarreia aquosa ou sanguinolenta como resultado do patógeno transitar pelo trato gastrointestinal e infectar as células epiteliais que revestem o cólon. Com aumentos impressionantes na resistência aos antibióticos e a atual falta de vacinas aprovadas, protocolos de pesquisa padronizados são críticos para estudar esse formidável patógeno. Aqui, metodologias são apresentadas para examinar a patogênese molecular de Shigella usando análises in vitro de adesão, invasão e replicação intracelular bacteriana em células epiteliais colônicas. Antes das análises da infecção, o fenótipo de virulência das colônias de Shigella foi verificado pela absorção do corante vermelho Congo em placas de ágar. Meios laboratoriais suplementados também podem ser considerados durante a cultura bacteriana para mimetizar condições in vivo . As células bacterianas são então utilizadas em um protocolo padronizado para infectar células epiteliais colônicas em placas de cultura de tecidos em uma multiplicidade estabelecida de infecção com adaptações para analisar cada estágio da infecção. Para os ensaios de aderência, as células de Shigella são incubadas com níveis reduzidos de meios para promover o contato bacteriano com as células epiteliais. Tanto para ensaios de invasão quanto para replicação intracelular, a gentamicina é aplicada por vários intervalos de tempo para eliminar bactérias extracelulares e permitir a avaliação da invasão e/ou a quantificação das taxas de replicação intracelular. Todos os protocolos de infecção enumeram bactérias aderentes, invadidas e/ou intracelulares diluindo em série lisados de células epiteliais infectadas e plaqueando unidades formadoras de colônias bacterianas em relação aos títulos infectantes em placas de ágar vermelho Congo. Em conjunto, esses protocolos permitem caracterizar e comparar de forma independente cada estágio da infecção por Shigella em células epiteliais para estudar este patógeno com sucesso.
Introdução
As doenças diarreicas causadas por patógenos bacterianos entéricos são um importante fardo global para a saúde. Em 2016, as doenças diarreicas foram responsáveis por 1,3 milhão de mortes no mundo e foram a quarta causa de morte em crianças menores de cinco anos 1,2. O patógeno bacteriano entérico Gram-negativo Shigella é o agente causador da shiguelose, uma das principais causas de mortes diarreicas no mundo3. A shigelose causa morbidade e mortalidade significativas a cada ano em crianças de países de baixa e média renda 4,5, enquanto infecções em países de alta renda estão ligadas a surtos de creches, alimentos e água 6,7,8,9. O desenvolvimento ineficaz devacinas10 e o aumento das taxas de resistência antimicrobiana (RAM)11,12 têm dificultado o manejo de surtos de Shigella em larga escala. Dados recentes do Centers for Disease Control and Prevention mostram que quase 46% das infecções por Shigella nos Estados Unidos apresentaram resistência aos medicamentos em 202013,14, enquanto a Organização Mundial da Saúde declarou a Shigella como um patógeno prioritário para a RAM, para o qual novas terapias são urgentemente necessárias15.
As infecções por Shigella são facilmente transmitidas pela via fecal-oral após a ingestão de água ou alimentos contaminados, ou através do contato humano direto. Shigella evoluiu para ser um patógeno eficiente, adaptado ao homem, com uma dose infecciosa de 10-100 bactérias suficiente para causar doença16. Durante o trânsito do intestino delgado, Shigella é exposta a sinais ambientais, como temperatura elevada e bile17. A detecção desses sinais induz alterações transcricionais para expressar fatores de virulência que aumentam a capacidade da bactéria de infectar o cólon humano 17,18,19. Shigella não invade o epitélio colônico a partir da superfície apical, mas transita através da camada epitelial após captação em células especializadas de microdobras apresentadoras de antígenos (células M) dentro do epitélio associado ao folículo 20,21,22. Após a transcitose, as células de Shigella são fagocitadas por macrófagos residentes. Shigella escapa rapidamente do fagossomo e desencadeia a morte celular de macrófagos, resultando na liberação de citocinas pró-inflamatórias 5,23,24. Shigella então invade células epiteliais colônicas do lado basolateral, lisa o vacúolo macropinocítico e estabelece um nicho replicativo no citoplasma 5,25. As citocinas pró-inflamatórias, particularmente a interleucina-8 (IL-8), recrutam leucócitos polimorfonucleares neutrófilos (PMNs) para o local da infecção, o que enfraquece as tight junctions epiteliais e permite a infiltração bacteriana do revestimento epitelial para exacerbar a infecção basolateral5. Os PMNs destroem o revestimento epitelial infectado para conter a infecção, o que resulta nos sintomas característicos da disenteria bacilar (sangrenta)5. Embora os mecanismos de invasão e replicação intracelular tenham sido completamente caracterizados, novas pesquisas estão demonstrando novos conceitos importantes na infecção por Shigella, incluindo regulação da virulência durante o trânsito gastrointestinal (GI)17, adesão19, melhor acesso basolateral através da permeabilidade da barreira26 e carreamento assintomático em crianças desnutridas27.
A capacidade de Shigella spp causar doença diarreica é restrita a humanos e primatas não humanos (PNH)28. Modelos de infecção intestinal por Shigella foram desenvolvidos para zebrafish29, camundongos30, cobaias31, coelhos 21,32,33 e suínos34,35. No entanto, nenhum desses sistemas-modelo pode replicar com precisão as características da doença observadas durante a infecção humana36. Embora modelos de shigelose do NHP tenham sido estabelecidos para estudar a patogênese da Shigella, esses sistemas modelo são caros de implementar e requerem doses infecciosas artificialmente altas, até nove ordens de magnitude superiores à dose infecciosa em humanos 37,38,39,40,41,42. Assim, a notável adaptação de Shigella para infecção de hospedeiros humanos requer o uso de culturas de células derivadas de humanos para recriar modelos fisiologicamente relevantes para interrogação precisa da patogênese de Shigella.
Aqui, procedimentos detalhados são descritos para medir as taxas de aderência, invasão e replicação de Shigella dentro de células epiteliais colônicas HT-29. Usando esses protocolos padronizados, os mecanismos moleculares pelos quais os genes de virulência bacteriana e os sinais ambientais impactam cada etapa da infecção por Shigella podem ser interrogados para melhor entender a relação dinâmica de interação patógeno-hospedeiro.
Protocolo
1. Preparação de reagentes e materiais
NOTA: Todos os volumes são consistentes com um ensaio usando duas placas de 6 poços.
- Meio TSB: Adicionar 0,5 L de água deionizada (DI) a 15 g de caldo de soja tríptico (TSB, ver Tabela de Materiais) meio e autoclave. Conservar à temperatura ambiente.
- Meio de sais biliares (TSB + BS): Para preparar TSB contendo 0,4% (p/v) de sais biliares, ressuspenda 0,06 g de sais biliares (BS, ver Tabela de Materiais) em 15 mL de TSB autoclavado. Esterilizar o filtro usando um filtro de PES de 0,22 μm.
NOTA: Os sais biliares consistem numa mistura 1:1 de colato de sódio e desoxicolato de sódio. Preparar meios frescos imediatamente antes da utilização. - DMEM + 10% (v/v) de SFB: Adicionar 5 mL de soro fetal bovino (SFB) a 45 mL de meio de águia modificado (DMEM) de Dulbecco. Conservar a 4 °C.
- DMEM + gentamicina: Para um tubo de 50 mL, adicionar 50 mL de DMEM e 50 μL de 50 mg/mL de gentamicina (ver Tabela de Materiais).
NOTA: Fazer alíquota fresca e aquecer em banho-maria a 37 °C antes de cada experimento. - PBS + 1% (v/v) Triton X-100: Adicionar 150 μL de Triton X-100 a 15 mL de solução salina tamponada com fosfato (PBS).
NOTA: Fazer alíquota fresca e aquecer em banho-maria a 37 °C antes de cada experimento. - TSB + placas indicadoras vermelhas Congo: Adicione 15 g de TSB, 7,5 g de ágar selecionado e 0,125 g de corante vermelho Congo (ver Tabela de Materiais) a um frasco de 1 L. Adicione 0,5 L de água DI e autoclave. Despeje 10-20 mL de meio em placas de Petri estéreis individuais (100 mm x 15 mm) e deixe solidificar.
CUIDADO: O vermelho Congo é cancerígeno e uma toxina reprodutiva. Certifique-se de que o manuseio do vermelho Congo seja realizado usando o equipamento de proteção individual apropriado. Consulte a ficha de dados de segurança do produto para obter informações adicionais.
NOTA: Aproximadamente 20 placas são feitas de 0,5 L de mídia vermelha Congo. As placas podem ser preparadas com 2-3 dias de antecedência e deixadas invertidas à temperatura ambiente até o uso. Para armazenamento a longo prazo, coloque placas invertidas em mangas plásticas a 4 °C por até 3 meses. - DMEM + 10% (v/v) de SFB e 5% (v/v) de dimetilsulfóxido (DMSO): Adicionar 42,5 mL de DMEM, 5 mL de SFB e 2,5 mL de DMSO a um tubo de 50 mL. Conservar a 4 °C.
2. Preparação de bactérias
NOTA: Todos os protocolos de cultivo e armazenamento em laboratório de Shigella são adaptados de Payne, S. M.43.
CUIDADO: Shigella spp são patógenos do Grupo de Risco2 44. Realizar todo o trabalho laboratorial em ambiente BSL-2, com medidas adicionais de segurança tomadas para limitar exposições acidentais devido à baixa dose infecciosa de Shigella spp.
- Crescimento de Shigella a partir de estoques congelados
- Transfira uma pequena quantidade de cultura congelada do frasco criogênico para uma placa de ágar vermelho TSB + Congo usando um aplicador estéril.
- Chamas esterilizar um ciclo de inoculação e deixá-lo esfriar. Estria o inóculo para frente e para trás em um quadrante da placa. Chame o laço, deixe esfriar e, em seguida, passe do primeiro quadrante para o segundo quadrante da placa. Repita para colocar o inóculo no terceiro e quarto quadrantes da placa.
NOTA: Alternativamente, estriar o inóculo usando um aplicador estéril fresco entre cada quadrante. - Inverter a placa e incubar a 37 °C durante a noite.
NOTA: A incubação a temperaturas ≥37 °C é necessária para a expressão dos fatores de virulência de Shigella necessários para a observação do fenótipo vermelho Congo positivo (CR+)45. As colônias avirulantes terão uma aparência branca e não serão invasivas. - Selar a placa com filme de parafina e conservar refrigerado a 4 °C.
NOTA: As colônias bacterianas permanecerão viáveis em placas de ágar por 1-2 semanas.
- Crescimento noturno de Shigella em cultura líquida
- Alíquota 3 mL de TSB em tubos de cultura estéreis de 14 mL.
- Escolha uma única colônia vermelha (CR+) bem isolada usando um aplicador estéril e ressuspenda em meio líquido.
- Incubar culturas durante a noite (16-18 h) a 37 °C com agitação a 250 rotações por minuto (rpm).
3. Preparação de células eucarióticas HT-29
NOTA: Todos os volumes são consistentes com um ensaio usando duas placas de 6 poços. As linhagens celulares HT-29 foram adquiridas da American Type Culture Collection (ATCC). Os protocolos de manutenção do HT-29 são adaptados das recomendações da ATCC46. Todos os meios devem ser pré-aquecidos em banho-maria a 37 °C antes da utilização. Todos os protocolos de manutenção do HT-29 devem ser realizados em gabinete de biossegurança. Abster-se de produzir bolhas ao misturar/trabalhar com células HT-29 em meios para evitar mudanças dramáticas no pH.
- Descongelamento de células HT-29 de estoque congelado
- Descongelar o frasco para injetáveis de células HT-29 num banho-maria a 37 °C.
NOTA: Certifique-se de que a tampa permaneça totalmente acima da água para evitar contaminação. O descongelamento deve demorar menos de 2 min. - Retire o frasco para injetáveis da água imediatamente após a cultura estar totalmente descongelada e descontamine com etanol a 70%. Certifique-se de que todas as etapas a partir deste ponto sejam executadas usando técnicas assépticas.
- Adicionar todo o conteúdo do frasco para injetáveis a um tubo de centrífuga de 15 ml contendo 9 ml de DMEM + 10% de SFB. Centrifugar a 125 x g durante 5 min à temperatura ambiente.
- Decantar o sobrenadante em um recipiente de resíduos e ressuspender o pellet em 10 mL de DMEM quente + 10% FBS. Transferir as células ressuspensas para um frasco de cultura de tecidos (T75) de 75cm2 contendo 10 mL de DMEM quente + 10% de SFB (volume total de 20 mL).
- Incubar as células a 37 °C com 5% de CO2 até que as células atinjam 90% de confluência (aproximadamente 6-7 dias).
NOTA: A confluência é estimada através de aproximação visual.
- Descongelar o frasco para injetáveis de células HT-29 num banho-maria a 37 °C.
- Semeadura de células HT-29
- Pré-aquecer 20 mL de PBS e 50 mL de DMEM + 10% FBS em banho-maria a 37 °C e pré-aquecer 3 mL de tripsina-EDTA a 0,25% (p/v) à temperatura ambiente.
- Uma vez que as células HT-29 (a partir do passo 3.1) atinjam 90% de confluência, decantar o meio de cultura de células HT-29 do frasco T75 para um recipiente de resíduos. Despeje ~10 mL de PBS quente no frasco e gire suavemente para lavar. Decantar o PBS em um recipiente de resíduos. Lave com PBS morno novamente e decante.
- Adicionar 2-3 mL de 0,25% (p/v) de tripsina-EDTA e girar suavemente por toda a área de superfície. Incubar a 37 °C com 5% de CO2 durante 4 min.
- Retire o balão da incubadora e gire suavemente a tripsina-EDTA, garantindo visualmente que todas as células se desprendem da superfície.
- Adicione imediatamente 6 mL de DMEM quente + FBS a 10% para desativar a tripsina. Pipetar para cima e para baixo para misturar completamente.
- Transfira todo o conteúdo para um tubo de centrífuga de 15 mL e gire-o a 500 x g por 5 min à temperatura ambiente.
- Decantar suavemente o sobrenadante em um recipiente de resíduos e ressuspender o pellet em 6 mL de DMEM quente + 10% FBS.
- Imediatamente após a ressuspensão, transferir 10 μL de células HT-29 suspensas do meio da cultura para um tubo de PCR de 0,2 mL. Adicionar 10 μL de corante azul de Trypan ao tubo de PCR e misturar.
- Adicione 10 μL de mistura de células HT-29/azul de Trypan a uma lâmina descartável da câmara de contador de células da Condessa (ver Tabela de Materiais). Enumere o número de células vivas e calcule a viabilidade celular.
Observação : ao documentar o número de células no exemplo, leia o número sob a contagem de células "ao vivo", não a contagem total de células. Alternativamente, a enumeração celular pode ser realizada manualmente usando um hemocitômetro. - As células HT-29 ressuspendidas da semente em um frasco T75 fresco ou placa de 6 poços.
- Para o balão T75:
- Pipetar suavemente para misturar e, em seguida, transferir 2,5 x 106 células para um balão T75 fresco de acordo com a equação abaixo:
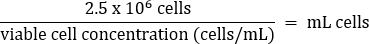
- Adicionar DMEM quente + meio FBS a 10% para um volume final de 20 mL (concentração final de 1,25 x 105 células/mL).
- Dispersar as células uniformemente pelo balão, balançando suavemente para frente e para trás.
- Incubar a 37 °C com 5% de CO2 até que as células atinjam 80% de confluência.
NOTA: Para um crescimento ideal, substitua o meio DMEM + 10% FBS no frasco T75 a cada ~3 dias. Decantar o meio para um recipiente de resíduos e adicionar 10 ml de PBS quente ao balão. Gire o PBS suavemente e decante-o no recipiente de resíduos. Em seguida, adicionar 20 mL de DMEM fresco e quente + FBS a 10% ao balão e retornar à incubadora a 37 °C, 5% CO2 .
- Pipetar suavemente para misturar e, em seguida, transferir 2,5 x 106 células para um balão T75 fresco de acordo com a equação abaixo:
- Para placa de 6 poços:
- Pipetar suavemente para misturar e, em seguida, transferir 5,85 x 106 células para um tubo cônico fresco de 50 mL de acordo com a equação abaixo:
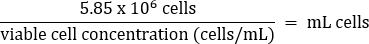
- Adicionar DMEM quente + meio FBS a 10% para um volume final de 26 mL (concentração final de 2,25 x 105 células/mL).
- Pipetar suavemente para misturar e, em seguida, distribuir 2 mL (4,5 x 105 células) em poços individuais de placas de 6 poços.
- Disperse as células uniformemente pelo poço, balançando suavemente para cima/para baixo e esquerda/direita 2-3x.
- Incubar a 37 °C com 5% de CO2 até que as células atinjam 80%-95% de confluência (aproximadamente 3-4 dias).
NOTA: 85% de confluência é recomendada para ensaios de invasão e replicação intracelular, enquanto 90%-95% de confluência é recomendada para ensaios de adesão. As células devem atingir ~85% de confluência após 48 h de incubação com uma concentração final de aproximadamente 1 x 106 células/poço. Podem ser necessários ajustes no número de células semeadas e no comprimento de incubação.
- Pipetar suavemente para misturar e, em seguida, transferir 5,85 x 106 células para um tubo cônico fresco de 50 mL de acordo com a equação abaixo:
- Para o balão T75:
- Fabricação de estoques HT-29 congelados
- Alíquota 1 mL de DMEM + 10% FBS + 5% meio DMSO em frascos criogênicos individuais.
- Adicionar 1 x 106 células HT-29 do passo 3.2.7 a cada frasco para injetáveis. Calcule o volume de células de acordo com a fórmula abaixo:
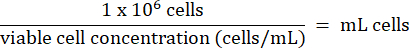
- Loja HT-29 células a longo prazo abaixo de -130 °C em congelador de armazenamento de vapor de nitrogênio líquido.
4. Ensaio de adesão
NOTA: Todos os volumes são consistentes com um ensaio usando duas placas de 6 poços.
- Subcultura durante a noite culturas de Shigella via diluição 1:50 em meios frescos.
- Vórtice e, em seguida, adicionar 100 μL de cada cultura noturna a 5 mL de TSB fresco ou TSB + BS em um tubo de cultura de tamanho adequado.
NOTA: Limitar o volume de cultura a <20% do volume do frasco ou tubo de cultura para garantir a aeração adequada. - Incubar a 37 °C com agitação a 250 rpm até que as células atinjam uma densidade óptica (OD600) de 0,7 (fase logarítmica média de crescimento de Shigella ); cerca de 2-2,5 h.
NOTA: Durante a subcultura, alíquota 50 mL de DMEM e um volume suficiente de PBS para todas as etapas de lavagem e colocar em banho-maria a 37 °C. Permitir que os meios atinjam 37 °C antes da utilização.
- Vórtice e, em seguida, adicionar 100 μL de cada cultura noturna a 5 mL de TSB fresco ou TSB + BS em um tubo de cultura de tamanho adequado.
- Transferir 2 x 108 unidades formadoras de colônias (UFCs) Shigella subcultivadas para tubos individuais de microcentrífuga de 2 mL.
NOTA: 2 x 108 UFC corresponde a aproximadamente 1 mL de células bacterianas em um OD600 de 0,7. Use leituras OD600 para aproximar UFC/mL de acordo com a calibração de cada espectrofotômetro individual. - Lave cada amostra de Shigella 2x com PBS.
- Células de pellet por centrifugação a 17.000 x g por 2 min à temperatura ambiente. Aspirar o sobrenadante, adicionar 1 mL de PBS morno e ressuspender bem o pellet, pipetando suavemente a amostra para cima e para baixo até que a mistura esteja totalmente homogênea (8-10x).
- Repita a etapa 4.3.1 1x tempo adicional.
- As células de pellets, por centrifugação a 17.000 x g por 2 min à temperatura ambiente, aspiram o sobrenadante e ressuspendem os pellets em 2 mL de DMEM quente.
OBS: A concentração final das bactérias ressuspensas será de 1 x 108 UFC/mL.
- Vórtice e, em seguida, adicionar 1 ml (1 x 108 UFC) de Shigella ressuspendida a cada poço das monocamadas epiteliais colónicas HT-29 preparadas em placas de 6 poços (a partir do passo 3.2.10.2).
NOTA: As infecções são normalmente realizadas em uma multiplicidade de infecção (MOI; proporção de células bacterianas para epiteliais) de 100. Para testar diferentes MOIs, diluir Shigella ressuspendida em DMEM quente até a concentração desejada e, em seguida, adicionar 1 mL de bactérias diluídas às monocamadas HT-29. Por exemplo, para testar um MOI de 10, dilua as bactérias 1:10 adicionando 150 μL de 1 x 108 UFC/mL de bactérias a 1,35 mL de DMEM aquecido e, em seguida, aplique 1 mL (1 x 107 UFCs) às células HT-29. - Incubar as placas de 6 poços a 37 °C com 5% de CO2 durante 3 horas.
- Durante a incubação, determinar o título de infecção bacteriana.
- Preparar diluições seriadas de 10 vezes de células de Shigella ressuspensas (do passo 4.3.3) em PBS.
- Placa 100 μL das diluições 1 x 10-5 e 1 x 10-6 em placas TSB + vermelho Congo e incubar durante a noite a 37 °C.
NOTA: O revestimento de 100 μL das diluições 1 x 10-5 e 1 x 10-6 corresponde a um fator de diluição final de 1 x 10-6 e 1 x 10-7, respectivamente.
- Após a incubação, lavar as monocamadas 4-5x com PBS.
- Aspirar o meio de cada poço.
OBS: Ao aspirar o meio a partir de placas de 6 poços, guie a ponta do aspirador ao longo do lado inferior dos poços, tentando evitar o contato com as células HT-29. - Adicione 1 mL de PBS morno a cada poço e lave delicadamente.
NOTA: Para lavar suavemente as monocamadas de 6 poços com PBS, mova a placa para cima e para baixo e de um lado para o outro na bancada. Lavar placas em movimento circular e/ou remover a placa da superfície da bancada pode causar a remoção mecânica de células do plástico. - Repita as etapas 4.7.1 e 4.7.2 4x vezes adicionais.
- Aspirar o meio de cada poço.
- Remover PBS por aspiração e lisar células HT-29 adicionando 1 mL de PBS + 1% Triton X-100 a cada poço.
- Incubar placas de 6 poços a 37 °C durante 5 minutos.
- Use um raspador de células ou uma ponta de pipeta dobrada para raspar as células lisadas do fundo do poço e transferir o 1 mL completo para um tubo de microcentrífuga fresco de 1,7 mL.
- Determine o número de bactérias associadas às células.
- Vórtice cada tubo (a partir do passo 4.10) durante pelo menos 30 s para deslocar ainda mais Shigella das células eucarióticas lisadas.
- Preparar diluições seriadas de lisados de 10 vezes em PBS.
- Placa 100 μL das diluições 1 x 10-2, 1 x 10-3 e 1 x 10-4 em placas TSB + vermelho Congo e incubar durante a noite a 37 °C.
NOTA: O chapeamento de 100 μL das diluições 1 x 10-2, 1 x 10-3 e 1 x 10-4 corresponde a um fator de diluição final de 1 x 10-3, 1 x 10-4 e 1 x 10-5, respectivamente.
5. Ensaio de invasão
NOTA: Todos os volumes são consistentes com um ensaio usando duas placas de 6 poços.
- Subcultura durante a noite culturas de Shigella via diluição 1:50 em meios frescos.
- Vórtice e, em seguida, adicionar 100 μL de cada cultura noturna a 5 mL de TSB fresco ou TSB + BS em um tubo de cultura de tamanho adequado.
NOTA: Limitar o volume de cultura a <20% do volume do frasco ou tubo de cultura para garantir a aeração adequada. - Incubar a 37 °C com agitação a 250 rpm até que as células atinjam um OD600 de 0,7 (fase logarítmica média de crescimento de Shigella ); cerca de 2-2,5 h.
NOTA: Durante a subcultura, alíquota 50 mL de DMEM + 50 mg/mL de gentamicina e um volume suficiente de PBS para todas as etapas de lavagem e colocar em banho-maria a 37 °C. Permitir que os meios atinjam 37 °C antes da utilização.
- Vórtice e, em seguida, adicionar 100 μL de cada cultura noturna a 5 mL de TSB fresco ou TSB + BS em um tubo de cultura de tamanho adequado.
- Transfira 2 x 108 UFCs subcultivadas Shigella para tubos individuais de microcentrífuga de 2 mL.
NOTA: 2 x 108 UFC corresponde a aproximadamente 1 mL de células bacterianas em um OD600 de 0,7. Use leituras OD600 para aproximar UFC/mL de acordo com a calibração de cada espectrofotômetro individual. - Lave amostras de Shigella 1x com PBS.
- Células de pellet por centrifugação a 17.000 x g por 2 min à temperatura ambiente. Aspirar o sobrenadante, adicionar 1 mL de PBS morno e ressuspender bem o pellet, pipetando suavemente a amostra para cima e para baixo até que a mistura esteja totalmente homogênea (8-10x).
- Repita a etapa 5.3.1. 1x tempo adicional.
- As células de pellets, por centrifugação a 17.000 x g por 2 min à temperatura ambiente, aspiram o sobrenadante e ressuspendem os pellets em 2 mL de DMEM quente.
OBS: A concentração final das bactérias ressuspensas será de 1 x 108 UFC/mL.
- Vórtice e, em seguida, adicionar 1 mL (1 x 108 UFCs) de Shigella ressuspendida mais 1 mL de DMEM a cada poço das monocamadas epiteliais colônicas HT-29 preparadas em placas de 6 poços (a partir da etapa 3.2.10.2).
NOTA: As infecções são normalmente realizadas em uma multiplicidade de infecção (MOI; proporção de células bacterianas para epiteliais) de 100. Para testar diferentes MOIs, diluir Shigella ressuspendida em DMEM até a concentração desejada e, em seguida, adicionar 1 mL de bactérias diluídas às monocamadas HT-29. Por exemplo, para testar um MOI de 10, dilua as bactérias 1:10 adicionando 150 μL de 1 x 108 UFC/mL de bactérias a 1,35 mL de DMEM e, em seguida, adicione 1 mL (1 x 107 UFCs) às células HT-29. - Para promover o contato bacteriano com as células HT-29, centrifugar as placas de 6 poços a 2.000 x g por 10 min à temperatura ambiente ou 37 °C se o ajuste de temperatura puder ser ajustado.
NOTA: A centrifugação promove o contato bacteriano com as células HT-29, o que ignora a necessidade de fatores de aderência e permite que as bactérias invadam rapidamente as células. - Incubar placas de 6 poços a 37 °C com 5% de CO2 durante 45 minutos.
- Durante a incubação, determinar o título de infecção bacteriana.
- Preparar diluições seriadas de 10 vezes de células de Shigella ressuspensas (do passo 5.3.3) em PBS.
- Placa 100 μL das diluições 1 x 10-5 e 1 x 10-6 em placas TSB + vermelho Congo e incubar durante a noite a 37 °C.
NOTA: O revestimento de 100 μL das diluições 1 x 10-5 e 1 x 10-6 corresponde a um fator de diluição final de 1 x 10-6 e 1 x 10-7, respectivamente.
- Lave bem as células HT-29 infectadas 3x com 1 mL de PBS.
- Aspirar o meio de cada poço.
OBS: Ao aspirar o meio a partir de placas de 6 poços, guie a ponta do aspirador ao longo do lado inferior dos poços, tentando evitar o contato com as células HT-29. - Adicione 1 mL de PBS morno a cada poço e lave delicadamente.
NOTA: Para lavar suavemente as monocamadas de 6 poços com PBS, mova a placa para cima e para baixo e de um lado para o outro na bancada. Lavar placas em movimento circular e/ou remover a placa da superfície da bancada pode causar a remoção mecânica de células do plástico. - Repita as etapas 5.8.1 e 5.8.2 2x vezes adicionais.
- Aspirar o meio de cada poço.
- Remover PBS por aspiração, em seguida, adicionar 2 mL de DMEM quente suplementado com 50 μg/mL de gentamicina em cada poço e incubar por 30 min a 37 °C com 5% de CO2.
- Lave bem as células HT-29 infectadas 3x com 1 mL de PBS.
- Repita o passo de lavagem 5.8.
- Remover PBS por aspiração, em seguida, adicionar 2 mL de DMEM quente suplementado com 50 μg/mL de gentamicina em cada poço e incubar por 60 min a 37 °C com 5% de CO2.
- Lave bem as células HT-29 infectadas 3x com 1 mL de PBS.
- Repita o passo de lavagem 5.8.
- Remover PBS por aspiração e lisar células HT-29 adicionando 1 mL de PBS + 1% Triton X-100 a cada poço.
- Incubar placas de 6 poços a 37 °C durante 5 minutos.
- Use um raspador de células ou uma ponta de pipeta dobrada para raspar as células lisadas do fundo do poço e transferir o 1 mL completo para um tubo de microcentrífuga fresco de 1,7 mL.
- Determine o número de bactérias intracelulares.
- Vórtice cada tubo (a partir do passo 5.15) durante pelo menos 30 s para deslocar ainda mais Shigella das células eucarióticas lisadas.
- Preparar diluições seriadas de lisados de 10 vezes em PBS.
- Placa 100 μL das diluições 1 x 10-2 e 1 x 10-3 em placas TSB + vermelho Congo e incubar durante a noite a 37 °C.
NOTA: O chapeamento de 100 μL das diluições 1 x 10-2 e 1 x 10-3 corresponde a um fator de diluição final de 1 x 10-3 e 1 x 10-4, respectivamente.
6. Ensaio de replicação intracelular
NOTA: Todos os volumes são consistentes com um ensaio usando duas placas de 6 poços.
- Subcultura durante a noite culturas de Shigella via diluição 1:50 em meios frescos.
- Vórtice e, em seguida, adicionar 100 μL de cada cultura noturna a 5 mL de TSB fresco ou TSB + BS em um tubo de cultura de tamanho adequado.
NOTA: Limitar o volume de cultura a <20% do volume do frasco ou tubo de cultura para garantir a aeração adequada. - Incubar a 37 °C com agitação a 250 rpm até que as células atinjam um OD600 de 0,7 (fase logarítmica média de crescimento de Shigella ); cerca de 2-2,5 h.
NOTA: Durante a subcultura, alíquota 50 mL de DMEM + 50 mg/mL de gentamicina e um volume suficiente de PBS para todas as etapas de lavagem e colocar em banho-maria a 37 °C. Permitir que os meios atinjam 37 °C antes da utilização.
- Vórtice e, em seguida, adicionar 100 μL de cada cultura noturna a 5 mL de TSB fresco ou TSB + BS em um tubo de cultura de tamanho adequado.
- Transfira 2 x 108 UFCs subcultivadas Shigella para tubos individuais de microcentrífuga de 2 mL.
NOTA: 2 x 108 UFC corresponde a aproximadamente 1 mL de células bacterianas em um OD600 de 0,7. Use leituras OD600 para aproximar UFC/mL de acordo com a calibração de cada espectrofotômetro individual. - Lave amostras de Shigella 1x com PBS.
- Células de pellet por centrifugação a 17.000 x g por 2 min à temperatura ambiente. Aspirar o sobrenadante, adicionar 1 mL de PBS morno e ressuspender bem o pellet, pipetando suavemente a amostra para cima e para baixo até que a mistura esteja totalmente homogênea (8-10x).
- Repita a etapa 6.3.1. 1x tempo adicional.
- As células de pellets, por centrifugação a 17.000 x g por 2 min à temperatura ambiente, aspiram o sobrenadante e ressuspendem os pellets em 2 mL de DMEM quente.
OBS: A concentração final das bactérias ressuspensas será de 1 x 108 UFC/mL.
- Vórtice e, em seguida, adicionar 1 mL (1 x 108 UFCs) de Shigella ressuspendida mais 1 mL de DMEM a cada poço de monocamadas epiteliais colônicas HT-29 preparadas em placas de 6 poços (a partir da etapa 3.2.10.2).
NOTA: As infecções são normalmente realizadas em uma multiplicidade de infecção (MOI; proporção de células bacterianas para epiteliais) de 100. Para testar diferentes MOIs, diluir Shigella ressuspendida em DMEM até a concentração desejada e, em seguida, adicionar 1 mL de bactérias diluídas às monocamadas HT-29. Por exemplo, para testar um MOI de 10, dilua as bactérias 1:10 adicionando 150 μL de 1 x 108 UFC/mL de bactérias a 1,35 mL de DMEM e, em seguida, aplique 1 mL (1 x 107 UFCs) às células HT-29. - Para promover o contato bacteriano com as células HT-29, centrifugar as placas de 6 poços a 2.000 x g por 10 min à temperatura ambiente ou 37 °C se o ajuste de temperatura puder ser ajustado.
NOTA: A centrifugação promove o contato bacteriano com as células HT-29, o que ignora a necessidade de fatores de aderência e permite que as bactérias invadam rapidamente as células. - Incubar placas de 6 poços a 37 °C com 5% de CO2 durante 45 minutos.
- Durante a incubação, determinar o título de infecção bacteriana.
- Preparar diluições seriadas de 10 vezes de células de Shigella ressuspensas (do passo 6.3.3) em PBS.
- Placa 100 μL das diluições 1 x 10-5 e 1 x 10-6 em placas TSB + vermelho Congo e incubar durante a noite a 37 °C.
NOTA: O revestimento de 100 μL das diluições 1 x 10-5 e 1 x 10-6 corresponde a um fator de diluição final de 1 x 10-6 e 1 x 10-7, respectivamente.
- Lave bem as células HT-29 infectadas 3x com 1 mL de PBS.
- Aspirar o meio de cada poço.
OBS: Ao aspirar o meio a partir de placas de 6 poços, guie a ponta do aspirador ao longo do lado inferior dos poços, tentando evitar o contato com as células HT-29. - Adicione 1 mL de PBS morno a cada poço e lave delicadamente.
NOTA: Para lavar suavemente as monocamadas de 6 poços com PBS, mova a placa para cima e para baixo e de um lado para o outro na bancada. Lavar placas em movimento circular e/ou remover a placa da superfície da bancada pode causar a remoção mecânica de células do plástico. - Repita as etapas 6.8.1 e 6.8.2 2x vezes adicionais.
- Aspirar o meio de cada poço.
- Remover PBS por aspiração, em seguida, adicionar 2 mL de DMEM quente suplementado com 50 μg/mL de gentamicina em cada poço e incubar por 30 min a 37 °C com 5% de CO2.
- Lave bem as células HT-29 infectadas 3x com 1 mL de PBS.
- Repetir o passo de lavagem 6.8.
- Remover PBS por aspiração, em seguida, adicionar 2 mL de DMEM quente com 50 μg/mL de gentamicina a cada poço das placas de 6 poços e incubar a 37 °C com 5% de CO2 pelo tempo desejado para permitir a replicação intracelular (até 24 h).
- Lave bem as células 2x com 1 mL de PBS.
- Repetir o passo de lavagem 6.8.
- Remover PBS por aspiração e lisar células HT-29 adicionando 1 mL de PBS + 1% Triton X-100 a cada poço.
- Incubar placas de 6 poços a 37 °C durante 5 minutos.
- Use um raspador de células ou uma ponta de pipeta dobrada para raspar as células lisadas do fundo do poço e transferir o 1 mL completo para um tubo de microcentrífuga fresco de 1,7 mL.
- Determine o número de bactérias intracelulares.
- Vórtice cada tubo (a partir do passo 6.15) durante pelo menos 30 s para deslocar ainda mais Shigella das células eucarióticas lisadas.
- Preparar diluições seriadas de lisados de 10 vezes em PBS.
- Placa 100 μL das diluições 1 x 10-2, 1 x 10-3 e 1 x 10-4 em placas TSB + Congo Red e incubar durante a noite a 37 °C.
NOTA: O chapeamento de 100 μL das diluições 1 x 10-2, 1 x 10-3 e 1 x 10-4 corresponde a um fator de diluição final de 1 x 10-3, 1 x 10-4 e 1 x 10-5, respectivamente.
Resultados
Ensaios de aderência, invasão e replicação intracelular foram realizados comparando S. flexneri 2457T wild type (WT) com S. flexneri ΔVF (ΔVF), um mutante hipotetizado para regular negativamente a virulência de Shigella. Como Shigella utiliza sais biliares como sinal para regular a virulência 17,18,47, experimentos foram realizados após subcultivo bacteriano em meio TSB e TSB suplementado com sais biliares a 0,4% (p/v)
Discussão
Este protocolo descreve um conjunto de três ensaios padronizados para estudar a adesão, invasão e replicação intracelular de células epiteliais intestinais por Shigella. Embora esses métodos sejam apenas versões modificadas dos ensaios clássicos de gentamicina usados para estudar a invasão e replicação intracelular de vários patógenos bacterianos dentro das células hospedeiras 49,50,51, considerações especiais devem ser aplicadas no estudo
Divulgações
Os autores declaram não haver conflitos de interesse.
Agradecimentos
O apoio aos autores inclui o Departamento de Pediatria do Hospital Geral de Massachusetts, o prêmio 2022A009041 do Comitê Executivo de Financiamento de Apoio Provisório à Pesquisa (ISF), o R21AI146405 de concessão do Instituto Nacional de Alergia e Doenças Infecciosas e o Instituto Nacional de Diabetes e Doenças Digestivas e Renais concedem o Centro de Pesquisa em Obesidade Nutricional em Harvard (NORCH) 2P30DK040561-26. Os financiadores não tiveram nenhum papel no desenho do estudo, coleta e análise de dados, decisão de publicação ou preparação do manuscrito.
Materiais
| Name | Company | Catalog Number | Comments |
| 0.22 μm PES filter | Millipore-Sigma | SCGP00525 | Sterile, polyethersulfone filter for sterilizing up to 50 mL media |
| 14 mL culture tubes | Corning | 352059 | 17 mm x 100 mm polypropylene test tubes with cap |
| 50 mL conical tubes | Corning | 430829 | 50 mL clear polypropylene conical bottom centrifuge tubes with leak-proof cap |
| 6-well tissue culture plates | Corning | 3516 | Plates are treated for optimal cell attachment |
| Bile salts | Sigma-Aldrich | B8756 | 1:1 ratio of cholate to deoxycholate |
| Congo red dye | Sigma-Aldrich | C6277 | A benzidine-based anionic diazo dye, >85% purity |
| Countess cell counting chamber slide | Invitrogen | C10283 | To be used with the Countess Automated Cell Counter |
| Dimethyl sulfoxide (DMSO) | Sigma-Aldrich | D8418 | A a highly polar organic reagent |
| Dulbecco’s Modified Eagle Medium (DMEM) | Gibco | 10569-010 | DMEM is supplemented with high glucose, sodium pyruvate, GlutaMAX, and Phenol Red |
| Fetal Bovine Serum (FBS) | Sigma-Aldrich | F4135 | Heat-inactivated, sterile |
| Gentamicin | Sigma-Aldrich | G3632 | Stock concentration is 50 mg/mL |
| HT-29 cell line | ATCC | HTB-38 | Adenocarcinoma cell line; colorectal in origin |
| Paraffin film | Bemis | PM999 | Laboratory sealing film |
| Petri dishes | Thermo Fisher Scientific | FB0875713 | 100 mm x 15 mm Petri dishes for solid media |
| Phosphate-buffered saline (PBS) | Thermo Fisher Scientific | 10010049 | 1x concentration; pH 7.4 |
| Select agar | Invitrogen | 30391023 | A mixture of polysaccharides extracted from red seaweed cell walls to make bacterial plating media |
| T75 flasks | Corning | 430641U | Tissue culture flasks |
| Triton X-100 | Sigma-Aldrich | T8787 | A common non-ionic surfactant and emulsifier |
| Trypan blue stain | Invitrogen | T10282 | A dye to detect dead tissue culture cells; only live cells can exclude the dye |
| Trypsin-EDTA | Gibco | 25200-056 | Reagent for cell dissociation for cell line maintenance and passaging |
| Tryptic Soy Broth (TSB) | Sigma-Aldrich | T8907 | Bacterial growth media |
Referências
- Karambizi, N. U., McMahan, C. S., Blue, C. N., Temesvari, L. A. Global estimated Disability-Adjusted Life-Years (DALYs) of diarrheal diseases: A systematic analysis of data from 28 years of the global burden of disease study. PloS one. 16 (10), e0259077 (2021).
- WHO. WHO methods and data sources for country-level causes of death 2000-2016. World Health Organization. , (2018).
- Kotloff, K. L. Shigella infection in children and adults: a formidable foe. Lancet Glob Health. 5 (12), e1166-e1167 (2017).
- Kotloff, K. L., et al. Burden and aetiology of diarrhoeal disease in infants and young children in developing countries (the Global Enteric Multicenter Study, GEMS): A prospective, case-control study. Lancet. 382 (9888), 209-222 (2013).
- Schroeder, G. N., Hilbi, H. Molecular pathogenesis of Shigella spp.: Controlling host cell signaling, invasion, and death by type III secretion. Clin Microbiol Rev. 21 (1), 134-156 (2008).
- Arvelo, W., et al. Transmission risk factors and treatment of pediatric shigellosis during a large daycare center-associated outbreak of multidrug resistant shigella sonnei: Implications for the management of shigellosis outbreaks among children. Pediatr Infect Dis J. 28 (11), 976-980 (2009).
- Kozyreva, V. K., et al. Recent outbreaks of Shigellosis in California caused by two distinct populations of Shigella sonnei with either increased virulence or fluoroquinolone resistance. mSphere. 1 (6), 1-18 (2016).
- Bowen, A., et al. Importation and domestic transmission of Shigella sonnei resistant to ciprofloxacin - United States, May 2014-February 2015. MMWR Morb Mortal Wkly Rep. 64 (12), 318-320 (2015).
- Tansarli, G. S., et al. Genomic reconstruction and directed interventions in a multidrug-resistant Shigellosis outbreak in Seattle, WA, USA: a genomic surveillance study. Lancet. 3099 (22), 1-11 (2023).
- Barry, E. M., et al. Progress and pitfalls in Shigella vaccine research. Nat Rev Gastroenterol Hepatol. 10 (4), 245-255 (2013).
- Increase in Extensively Drug-Resistant Shigellosis in the United States. CDC Health Alert Network. Centers for Disease Control and Prevention Available from: https://emergency.cdc.gov/han/2023/han00486.asp?ACSTrackingID=USCDC_511-DM100260&ACSTrackingLabel=HAN%20486%20-%20General%20Public&deliveryName=USCDC_511-DM100260 (2023)
- Shiferaw, B., et al. Antimicrobial susceptibility patterns of Shigella isolates in Foodborne Diseases Active Surveillance Network (FoodNet) sites, 2000-2010. Clin Infect Dis. 54, S458-S463 (2012).
- Centers for Disease Control and Prevention. COVID-19: U.S. Impact on Antimicrobial Resistance, Special Report 2022. Atlanta, GA: U.S. Department of Health and Human Services. CDC. , (2022).
- Centers for Disease Control and Prevention. Antibiotic resistance threats in the United States, 2019. CDC. 10 (1), (2019).
- WHO. Prioritization of pathogens to guide discovery, research and development of new antibiotics for drug-resistant bacterial infections, including tuberculosis. WHO. , (2017).
- DuPont, H. L., Levine, M. M., Hornick, R. B., Formal, S. B. Inoculum size in shigellosis and implications for expected mode of transmission. J Infect Dis. 159 (6), 1126-1128 (1989).
- Nickerson, K. P., et al. Analysis of Shigella flexneri resistance, biofilm formation, and transcriptional profile in response to bile salts. Infect Immun. 85 (6), 1-18 (2017).
- Faherty, C. S., Redman, J. C., Rasko, D. A. Shigella flexneri effectors OspE1 and OspE2 mediate induced adherence to the colonic epithelium following bile salts exposure. Mol Microbiol. 85 (1), 107-121 (2012).
- Chanin, R. B., et al. Shigella flexneri adherence factor expression in in vivo-like conditions. mSphere. 4 (6), e00751 (2019).
- Baranov, V., Hammarström, S. Carcinoembryonic antigen (CEA) and CEA-related cell adhesion molecule 1 (CEACAM1), apically expressed on human colonic M cells, are potential receptors for microbial adhesion. Histochem Cell Biol. 121 (2), 83-89 (2004).
- Wassef, J. S., Keren, D. F., Mailloux, J. L. Role of M cells in initial antigen uptake and in ulcer formation in the rabbit intestinal loop model of shigellosis. Infect Immun. 57 (3), 858-863 (1989).
- Sansonetti, P. J., Arondel, J., Cantey, J. R., Prévost, M. C., Huerre, M. Infection of rabbit Peyer's patches by Shigella flexneri: Effect of adhesive or invasive bacterial phenotypes on follicle-associated epithelium. Infect Immun. 64 (7), 2752-2764 (1996).
- Sansonetti, P. J., et al. Caspase-1 activation of IL-1beta and IL-18 are essential for Shigella flexneri-induced inflammation. Immunity. 12 (5), 581-590 (2000).
- Zychlinsky, A., Fitting, C., Cavaillon, J. M., Sansonetti, P. J. Interleukin 1 is released by murine macrophages during apoptosis induced by Shigella flexneri. J Clin Invest. 94 (3), 1328-1332 (1994).
- Sansonetti, P. J., Ryter, A., Clerc, P., Maurelli, A. T., Mounier, J. Multiplication of Shigella flexneri within HeLa cells: lysis of the phagocytic vacuole and plasmid-mediated contact hemolysis. Infect Immun. 51 (2), 461-469 (1986).
- Maldonado-Contreras, A., et al. Shigella depends on SepA to destabilize the intestinal epithelial integrity via cofilin activation. Gut Microbes. 8 (6), 544-560 (2017).
- Collard, J. -. M., et al. High prevalence of small intestine bacteria overgrowth and asymptomatic carriage of enteric pathogens in stunted children in Antananarivo, Madagascar. PLoS Negl Trop Dis. 16 (5), e0009849 (2022).
- Mattock, E., Blocker, A. J. How do the virulence factors of shigella work together to cause disease. Front Cell Infect Microbiol. 7, 1-24 (2017).
- Mostowy, S., et al. The zebrafish as a new model for the in vivo study of Shigella flexneri interaction with phagocytes and bacterial autophagy. PLoS Pathog. 9 (9), e1003588 (2013).
- Martinez-Becerra, F. J., et al. Parenteral immunization with IpaB/IpaD protects mice against lethal pulmonary infection by Shigella. Vaccine. 31 (24), 2667-2672 (2013).
- Shim, D. -. H., et al. New animal model of shigellosis in the Guinea pig: its usefulness for protective efficacy studies. J Immunol. 178 (4), 2476-2482 (2007).
- Marteyn, B., et al. Modulation of Shigella virulence in response to available oxygen in vivo. Nature. 465 (7296), 355-358 (2010).
- West, N. P., et al. Optimization of virulence functions through glucosylation of Shigella LPS. Science. 307 (5713), 1313-1317 (2005).
- Maurelli, A. T., et al. Shigella infection as observed in the experimentally inoculated domestic pig, Sus scrofa domestica. Microbial Pathog. 25 (4), 189-196 (1998).
- Jeong, K. -. I., Zhang, Q., Nunnari, J., Tzipori, S. A piglet model of acute gastroenteritis induced by Shigella dysenteriae Type 1. J Infect Dis. 201 (6), 903-911 (2010).
- Kim, Y. -. J., Yeo, S. -. G., Park, J. -. H., Ko, H. -. J. Shigella vaccine development: prospective animal models and current status. Curr Pharm Biotechnol. 14 (10), 903-912 (2013).
- Kent, T. H., Formal, S. B., LaBrec, E. H., Sprinz, H., Maenza, R. M. Gastric shigellosis in rhesus monkeys. Am J Pathol. 51 (2), 259-267 (1967).
- Shipley, S. T., et al. A challenge model for Shigella dysenteriae 1 in cynomolgus monkeys (Macaca fascicularis). Comp Med. 60 (1), 54-61 (2010).
- Higgins, R., Sauvageau, R., Bonin, P. Shigella flexneri Type 2 Infection in captive nonhuman primates. Can Vet J. 26 (12), 402-403 (1985).
- Oaks, E. V., Hale, T. L., Formal, S. B. Serum immune response to Shigella protein antigens in rhesus monkeys and humans infected with Shigella spp. Infect Immun. 53 (1), 57-63 (1986).
- Formal, S. B., et al. Protection of monkeys against experimental shigellosis with a living attenuated oral polyvalent dysentery vaccine. J Bacteriol. 92 (1), 17-22 (1966).
- Levine, M. M., Kotloff, K. L., Barry, E. M., Pasetti, M. F., Sztein, M. B. Clinical trials of Shigella vaccines: two steps forward and one step back on a long, hard road. Nat Rev Microbiol. 5 (7), 540-553 (2007).
- Payne, S. M. Laboratory cultivation and storage of Shigella. Curr Protoc Microbiol. 55 (1), 93 (2019).
- NIH Guidelines. NIH guidelines for research involving recombinant or synthetic nucleic acid molecules. NIH Guidelines. 2, 142 (2019).
- Maurelli, A. T., Blackmon, B., Curtiss, R. Loss of pigmentation in Shigella flexneri 2a is correlated with loss of virulence and virulence-associated plasmid. Infect Immun. 43 (1), 397-401 (1984).
- HT-29 cell line product sheet. ATCC Available from: https://www.atcc.org/products/htb-38 (2023)
- Sistrunk, J. R., Nickerson, K. P., Chanin, R. B., Rasko, D. A., Faherty, C. S. Survival of the fittest: How bacterial pathogens utilize bile to enhance infection. Clin Microbiol Rev. 29 (4), 819-836 (2016).
- Stensrud, K. F., et al. Deoxycholate interacts with IpaD of Shigella flexneri in inducing the recruitment of IpaB to the type III secretion apparatus needle tip. J Biol Chem. 283 (27), 18646-18654 (2008).
- Mandell, G. L. Interaction of intraleukocytic bacteria and antibiotics. J Clin Invest. 52 (7), 1673-1679 (1973).
- Elsinghorst, E. A. Measurement of invasion by gentamicin resistance. Methods Enzymo. 236 (1979), 405-420 (1994).
- Elsinghorst, E. A., Weitz, J. A. Epithelial cell invasion and adherence directed by the enterotoxigenic Escherichia coli tib locus is associated with a 104-kilodalton outer membrane protein. Infect Immun. 62 (8), 3463-3471 (1994).
- Dorman, C. J., McKenna, S., Beloin, C. Regulation of virulence gene expression in Shigella flexneri, a facultative intracellular pathogen. Int J Med Microbiol. 291 (2), 89-96 (2001).
- Porter, M. E., Dorman, C. J. Positive regulation of Shigella flexneri virulence genes by integration host factor. J Bacteriol. 179 (21), 6537-6550 (1997).
- Maurelli, A. T., Blackmon, B., Curtiss, R. Temperature-dependent expression of virulence genes in Shigella species. Infect Immun. 43 (1), 195-201 (1984).
- Schuch, R., Maurelli, A. T. Virulence plasmid instability in Shigella flexneri 2a is induced by virulence gene expression. Infect Immun. 65 (9), 3686-3692 (1997).
- Formal, S. B., Hale, T. L., Sansonetti, P. J. Invasive enteric pathogens. Rev Infect Dis. 5, S702-S707 (1983).
- Pál, T., Hale, T. L. Plasmid-associated adherence of Shigella flexneri in a HeLa cell model. Infect Immun. 57 (8), 2580-2582 (1989).
- Noben, M., et al. Human intestinal epithelium in a dish: Current models for research into gastrointestinal pathophysiology. United European Gastroenterol J. 5 (8), 1073-1081 (2017).
- Liévin-Le Moal, V., Servin, A. L. Pathogenesis of human enterovirulent bacteria: lessons from cultured, fully differentiated human colon cancer cell lines. Microbiol Mol Biol Rev R. 77 (3), 380-439 (2013).
- Mitchell, D. M., Ball, J. M. Characterization of a spontaneously polarizing HT-29 cell line, HT-29/cl.f8. In Vitro Cell Dev Biol - Anim. 40 (10), 297-302 (2004).
- Gagnon, M., Zihler Berner, A., Chervet, N., Chassard, C., Lacroix, C. Comparison of the Caco-2, HT-29 and the mucus-secreting HT29-MTX intestinal cell models to investigate Salmonella adhesion and invasion. J Microbiol Methods. 94 (3), 274-279 (2013).
- Koestler, B. J., et al. Human intestinal enteroids as a model system of Shigella pathogenesis. Infect Immun. 87 (4), 00733 (2019).
- Ranganathan, S., et al. Evaluating Shigella flexneri pathogenesis in the human enteroid model. Infect Immun. 87 (4), (2019).
- Nickerson, K. P., et al. A versatile human intestinal organoid-derived epithelial monolayer model for the study of enteric pathogens. Microbiol Spectr. 9 (1), 1-17 (2021).
- Perlman, M., Senger, S., Verma, S., Carey, J., Faherty, C. S. A foundational approach to culture and analyze malnourished organoids. Gut Microbes. 15 (2), 2248713 (2023).
- Pope, L. M., Reed, K. E., Payne, S. M. Increased protein secretion and adherence to HeLa cells by Shigella spp. following growth in the presence of bile salts. Infect Immun. 63 (9), 3642-3648 (1995).
- Faherty, C. S., et al. The synthesis of OspD3 (ShET2) in Shigella flexneri is independent of OspC1. Gut Microbes. 7 (6), 486-502 (2016).
- Ridlon, J. M., Kang, D. -. J., Hylemon, P. B. Bile salt biotransformations by human intestinal bacteria. J Lipid Res. 47 (2), 241-259 (2006).
- Köseoğlu, V. K., Hall, C. P., Rodríguez-López, E. M., Agaisse, H. The Autotransporter IcsA promotes Shigella flexneri biofilm formation in the presence of bile salts. Infect Immun. 87 (7), 1-14 (2019).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados