Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Murin Artrit Dokusundan Primer Sinovyal Makrofaj ve Fibroblastların İzolasyonu ve Kültürü
Bu Makalede
Özet
Bu çalışma, sinovyal makrofajları ve fibroblastları murin inflamatuar artrit dokusundan izole etmek için modifiye edilmiş bir protokol sunmaktadır.
Özet
Romatoid artrit, eklemlerin kronik iltihaplanmasına yol açan otoimmün bir hastalıktır. Romatoid artrit patogenezinde sinovyal makrofajlar ve sinovyal fibroblastlar merkezi rol oynarlar. İnflamatuar artritte patolojik progresyon ve remisyonun altında yatan mekanizmaları ortaya çıkarmak için her iki hücre popülasyonunun fonksiyonlarını anlamak önemlidir. Genel olarak in vitro deneysel koşullar, mümkün olduğunca in vivo ortamı taklit etmelidir. Primer doku kaynaklı hücreler, artritte sinovyal fibroblastları karakterize eden deneylerde kullanılmıştır. Buna karşılık, inflamatuar artritte makrofajların biyolojik fonksiyonlarını araştıran deneylerde, hücre hatları, kemik iliği kaynaklı makrofajlar ve kan monosit kaynaklı makrofajlar kullanılmıştır. Bununla birlikte, bu tür makrofajların aslında dokuda yerleşik makrofajların işlevlerini yansıtıp yansıtmadığı belirsizdir. Yerleşik makrofajlar elde etmek için, önceki protokoller, inflamatuar artrit fare modelinde sinovyal dokudan hem primer makrofajları hem de fibroblastları izole etmek ve genişletmek için değiştirildi. Bu primer sinovyal hücreler, inflamatuar artritin in vitro analizi için yararlı olabilir.
Giriş
Romatoid artrit (RA), sinovyumun hiperplazisi ile karakterize, eklem yıkımına yol açan otoimmün bir hastalıktır 1,2. Dokuda yerleşik makrofajlar ve fibroblastlar, eklem homeostazını korumak için sağlıklı sinovyumda bulunur. RA hastalarında, sinovyal fibroblastlar (SF'ler) çoğalır ve monositler de dahil olmak üzere bağışıklık hücreleri, inflamasyonla ilişkili süreçlerolan sinovyum ve eklem sıvısına sızar 1,3,4. Yerleşik makrofajları ve periferik kan monosit kaynaklı makrofajları içeren sinovyal makrofajlar (SM'ler) ve SF'ler anormal bir şekilde aktive olurlar ve RA patogenezinde önemli rollere sahiptirler. Son çalışmalar, SM'ler ve SF'ler arasındaki hücre-hücre etkileşimlerinin RA5,6'nın hem alevlenmesine hem de remisyonuna katkıda bulunduğunu göstermiştir.
RA patogenezini anlamak için, K/BxN serum transfer artriti, kollajen kaynaklı artrit ve kollajen antikoru kaynaklı artrit dahil olmak üzere çeşitli kemirgen inflamatuar artrit modelleri kullanılmıştır. Artritte moleküler fonksiyonları açıklığa kavuşturmak için genellikle hücre bazlı tahliller gereklidir. Bu nedenle, hayvan artrit modellerinden birincil hücreler izole edilmiştir. SF'leri murin artrit dokusundan izole etme yöntemi iyi bilinmektedir ve bu hücreler artrit patogenezinde moleküler mekanizmaların aydınlatılmasına katkıda bulunmuştur 7,8. Öte yandan, kemik iliği kaynaklı makrofajlar, kan monosit kaynaklı makrofajlar ve makrofaj hücre hatları, artrit çalışmaları için sıklıkla makrofaj kaynakları olarak kullanılmıştır 9,10. Makrofajlar mikroçevreleri ile ilişkili işlevler kazanabildiklerinden, genel makrofaj kaynakları artrit dokusuna özgü yanıtlardan yoksun olabilir. Ayrıca murin sinovyum artrit modellerinde bile çok küçük bir doku olduğu için sıralama ile yeterli sinovyal hücre elde etmek zordur. İn vitro çalışmalarda sinovyal makrofajların kullanılmaması artrit çalışmalarında bir sınırlama olmuştur. Sinovyal makrofajları izole etmek ve genişletmek için bir protokolün oluşturulması, RA'daki patolojik mekanizmaların aydınlatılması için bir avantaj olacaktır.
SF'leri izole etmek için önceki yöntemde, SM'ler atıldı7. Bunun yanı sıra, yerleşik makrofajları bazı organlardan izole etmek ve genişletmek için bir yöntem bildirilmiştir11. Bu nedenle, mevcut protokoller kombinasyon halinde değiştirildi. Değişiklik, hem SM'lerin hem de SF'lerin birincil kültürünü yüksek saflıkta elde etmeyi amaçlamaktadır. Bu yöntemin genel amacı, hem SM'leri hem de SF'leri murin artrit dokusundan izole etmek ve genişletmektir.
Protokol
Hayvanları içeren deneyler, Ehime Üniversitesi Hayvan Deneyleri Komitesi tarafından onaylandı ve Ehime Üniversitesi Hayvan Deneyleri Yönergesi'ne (37A1-1*16) uygun olarak gerçekleştirildi.
1. Aletlerin, reaktiflerin ve kültür ortamının hazırlanması
- Kültür ortamını aşağıdaki gibi hazırlayın: Dulbecco'nun Modifiye Eagle Medium'unu (DMEM) %10 fetal sığır serumu (FBS) ve %1 antibiyotik-antimikotik solüsyon (anti-anti) ile takviye edin.
- Sindirim ortamını aşağıdaki gibi hazırlayın: kültür ortamını 1 mg / mL kollajenaz tip IV ile destekleyin. Kullanmadan hemen önce kollajenaz konsantrasyonunu ayarlayın.
- Tip IC kollajeni 1 mM HCl çözeltisi ile 0.15 mg / mL konsantrasyona seyreltin. Seyreltilmiş kollajen çözeltisi ile sel kültürü kapları (40 veya 60 mm çapında). Oda sıcaklığında 6-12 saat sonra, kollajen çözeltisini bulaşıklardan çıkarın ve oda sıcaklığında kurutun. Kollajen kaplı bulaşıklar oda sıcaklığında en az 1 hafta saklanabilir. Önceden kaplanmış bulaşıkları kullanmadan önce fosfat tamponlu salin (PBS) veya orta ile yıkayın.
- Makas, tırtıklı uçlu cımbız ve ince uçlu cımbız gibi steril cerrahi aletler hazırlayın. Kullanmadan önce %70 etanole batırın.
2. Farelerde sinovit dokusunun hazırlanması ( Şekil 1A)
- Arka pençelerinde enflamatuar artritli bir fare hazırlayın.
NOT: Bu protokol için kollajen antikoru kaynaklı artrit (CAIA) veya K/BxN serum transfer artriti (STA) olan doğumdan 7-8 hafta sonra dişi C57BL / 6 fareler (18-20 g) kullanıldı8. SM'leri şişmemiş (yani sağlıklı) dokudan izole etmek, hücre sayısı yetersiz olduğu için zor olabilir. - Fareleri 80 mg / kg ketamin ve 16 mg / kg ksilazin intraperitoneal enjeksiyonu ile uyuşturun. Fareleri% 70 etanol ile temizleyin.
- Kalbi ortaya çıkarmak için göğüs bölgesini makasla kesin. Kalbin sağ kulak kepçesini makasla kesin ve ardından kalbin tepesinden sol ventriküle 23 G'lık bir kelebek iğne batırın, ardından periferik kanı manuel olarak çıkarmak için bir şırınga kullanarak 15-20 mL steril PBS reflüsü uygulayın (yaklaşık 1 mL / 2 s).
- Makas kullanarak cildi keserek ve tırtıklı uçlu cımbız kullanarak cildi çekerek arka pençeleri süsleyin.
NOT: Bu adımdan sonra numunelerin taşınması için cımbız kullanılması tavsiye edilir. Fare kıllarının yapışmasını önlemek için süslenmiş dokuya parmaklarınızla dokunmayın. - Metatarsofalangeal eklemleri çekerek yerinden çıkarın, ardından ayak parmaklarını çıkarmak için makas kullanarak eklemlerin bağlarını kesin.
- Ayak bileğine yakın alt bacak kaslarının tendonlarını makas kullanarak kesin. Tendonu cımbızla kavrayın ve tibiayı ortaya çıkarmak için alt bacaktaki kasları proksimal olarak soyun. Fibulayı çıkarın.
- Diz eklemini çekerek yerinden çıkarın, ardından şişmiş arka pençe ile tibiayı ayırmak için makas kullanarak eklemlerin bağlarını kesin. Numuneleri adım 3.1'e kadar işlenene kadar buz gibi soğuk kültür ortamında (0,3 mL/cm2) tutun.
3. Sinovit dokusunun sindirimi ( Şekil 1B)
- Numuneden kaçınarak kültür ortamını aspire edin ve ardından taze kültür ortamı (0.3 mL/cm2) ekleyin. Yıkama işlemini üç veya dört kez tekrarlayın.
NOT: Bu adımdan itibaren, numunelerin taşınması temiz bir tezgahta veya güvenlik kabininde aseptik olarak gerçekleştirilmelidir. - Stereomikroskop altında (10x-20x büyütmede) kültür ortamında ince uçlu cımbız kullanarak çekerek numunelerin tüm eklemlerini yerinden çıkarın. İnce uçlu cımbız bu adımda uygundur. Kaval kemiğini ve mümkün olduğunca çok sayıda damarı, tendonu ve bağı çıkarın. Yerinden çıkarken kemikleri kırmamaya dikkat edin.
- Numune başına iki adet 15 mL'lik tüp hazırlayın. Çıkık kemikleri yumuşak dokularla birlikte cımbızla ilk 15 mL'lik tüpe aktarın. Her iki arka pençeden elde edilen numune başına 4 mL sindirim ortamı tüpe ekleyin.
- Artık hücreleri ve doku parçalarını toplamak için, numunenin bulunduğu ortamı ikinci 15 mL'lik tüpe aktarın. Ortamı oda sıcaklığında 5 dakika boyunca 500 x g'da santrifüjleyin. Süpernatanı çıkardıktan sonra, peleti 1 mL sindirim ortamı ile yeniden süspanse edin ve hücre ve doku parçası çözeltisini hemen hemen tüm dokuyu içeren ilk 15 mL'lik tüpe aktarın (toplam 5 mL sindirim ortamı / arka pençeler).
- Numuneyi 37 °C'de 60-120 dakika hibridizasyon fırınında çalkalayarak sindirin.
NOT: Numuneleri sindirmek için en uygun zamana karar verilmelidir. Süre, ayak bileklerindeki ve kollajenazlardaki şişliğin derecesine bağlıdır. Çoğu durumda, 60-120 dakika yeterlidir. 60 dakikalık inkübasyondan sonra, sindirilmiş numunenin bir kısmını pipetleme ile toplayın ve mikroskop altında gözlemleyin. Sindirim yetersizse, inkübasyon devam etmeli ve sindirim her 30 dakikada bir kontrol edilmelidir. - Çözeltiyi iyice pipetleyin. Hücre çözeltisini bir hücre süzgecinden (40 μm gözenek boyutu) 50 mL'lik bir tüpe süzün.
- Hücre süzgecinden 50 mL'lik tüpe 10 mL kültür ortamı ekleyin. Oda sıcaklığında 5 dakika boyunca 300 x g'da santrifüjleyin.
- Süpernatanı çıkardıktan sonra, 10 mL kültür ortamı ile tekrar süspanse edin. Santrifüjlemeyi tekrarlayın. Süpernatanı çıkardıktan sonra, 2 mL kültür ortamı ile tekrar süspanse edin.
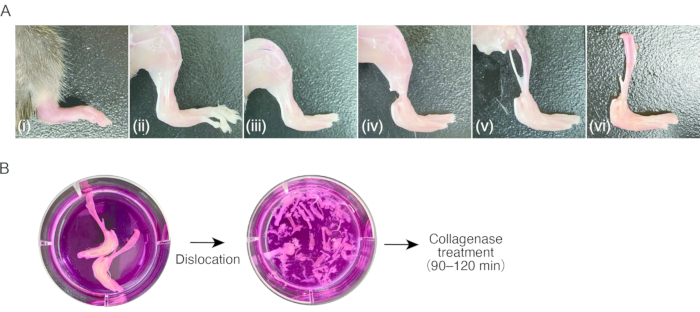
Şekil 1: Murin artrit dokusu ve kollajenaz sindirimi örneklemesi prosedürü . (A) (i) İnflamatuar artritli murin arka pençesi. (ii) Arka pençedeki derinin çıkarılması. (iii) Metatarsofalangeal eklemlerin çıkığı ve ayak parmaklarının çıkarılması. (iv) Ayak bileğindeki tendonların kesilmesi. (v) Alt bacaklardaki kasların çıkarılması. (vi) Diz ekleminin çıkığı. (b) Solda; kültür ortamında eksize edilmiş bacaklar. Sağ; kültür ortamında çıkık tarsus ve metatars. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
4. Sinovyal fibroblastların izolasyonu ( Şekil 2A)
- Her iki ayak bileğinden elde edilen tüm hücre süspansiyonlarını kollajen kaplı kap üzerine tohumlayın.
NOT: Hücreleri elde etmek için zayıf veya orta derecede şişliği olan ayak bilekleri kullanılıyorsa, 40 mm çapında bir çanak uygulanır. Kollajen kaplı çanak boyutu, her iki ayak bileğinde de şiddetli şişlik varsa 60 mm çapında bir çanak olarak değiştirilebilir. - Kültür ortamı ekleyin (yaklaşık 222 μL/cm2). % 5 CO 2 ile nemlendirilmiş bir atmosferde 37 ° C'de 1 saat inkübe edin.
- Bir pipet kullanarak yapışmayan hücreleri toplayın (adım 5.1'de kullanın). Kollajen kaplı kabı kültür ortamıyla yıkayın ve ortamı toplayın. Yapışık hücreleri taze ortamda kültürleyin (Şekil 2B,i). Kollajen kaplı çanağa hızla yapışan hücrelerin çoğu, fibroblastoid (iğ şeklinde) bir morfoloji sergiler.
- Hanks'in dengeli tuz çözeltisinde (HBSS) %0.05 tripsin ile muamele edilerek alt birleşen hücrelerin geçişi. Bu yöntemde, ilk genişlemede bile olsa diğer hücrelerin kontaminasyonu sınırlıdır. Daha saflaştırılmış fibroblast benzeri hücreler gerekiyorsa, saflığın arttırılmasına izin vermek için tekrarlanan geçiş yapın; bununla birlikte, adezyon halinde hücrelerin sitoplazmasının genişlemesi de gözlenir (Şekil 2B,ii). Aşırı pasajlar hücrelerdeki naif özelliklerin kaybına etki ettiğinden, 5'ten az pasajlı hücreler kullanın.
5. Sinovyal makrofajların izolasyonu ( Şekil 2A)
- Adım 4.4'ten itibaren tüm yapışmayan hücreleri, kollajen ile kaplanmamış bulaşıklara (40 veya 60 mm çapında) tohumlayın.
NOT: Yapışık olmayan hücreler arasında makrofajlar, diğer lenfositler ve sinovit dokusundan kalan fibroblastlar bulunur. - Toplu hücreleri% 5 CO2 ile nemlendirilmiş bir atmosferde 37 ° C'de 1 gün boyunca kültürleyin.
- Yapışmayan lenfositleri çıkarmak için, kültürlenmiş ortamı aspire edin ve ardından taze kültür ortamı ekleyin. Bu işlemi iki veya üç kez tekrarlayın (Şekil 2B,iii).
- Yapışık yığın hücrelerini kültür ortamında 1-2 hafta boyunca kültürleyin, birleşmeyi korurken her 2 günde bir ortam değişir (Şekil 2B, iv).
NOT: SF'lerle ko-kültür koşulları altında SM'lerin sayısı yavaş yavaş artar. Bu nedenle, ko-kültür periyodu gerektiği gibi ayarlanmalıdır. - PBS veya HBSS ile iki kez yıkayın. HBSS'de (yaklaşık 55 μL/cm2) %0.05 tripsin ile 37 ° C'de 3 dakika boyunca% 5 CO2 ile nemlendirilmiş bir atmosferde muamele edin. Fibroblastlar, tripsin tedavisi ile kültür kabından kolayca ayrılır ve makrofajlar, tripsin tedavisine direnç gösterir. Sinovyal makrofajların seçimi için bu özelliği kullanın.
- HBSS'de kültür ortamını (yaklaşık 222 μL /cm2) nazikçe% 0.05 tripsine ekleyin. Bu adımdan sonra, ortamı doğrudan hücrelerin üzerine dökmeyin.
- Ayrılmış hücreleri çıkarmak için, kültürlenmiş ortamı aspire edin ve ardından taze kültür ortamını nazikçe ekleyin. Bu işlemi iki veya üç kez tekrarlayın. Kullanana kadar tabak üzerinde kalan hücreleri taze kültür ortamında tutun (Şekil 2B,v).
NOT: Tripsin tedavisini takiben, yapışık hücreler makrofaj benzeri morfolojik özellikler sergiler.

Şekil 2: İnflamatuar artrit dokusundan makrofajdan zengin ve fibroblasttan zengin fraksiyonların ayrılması. (A) Makrofajdan zengin ve fibroblasttan zengin hücreleri artrit dokusundan ayırma prosedürünün şeması. (B) Prosedürün aşamalarının temsili faz kontrast görüntüleri, Şekil 2A'da (i) ila (v). Ölçek çubuğu 100 μm'yi temsil eder. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Sonuçlar
7-8 haftalıkken dişi C57BL/6 farelerine kollajen antikoru kaynaklı artrit uygulandı. Makrofaj benzeri hücreler ve fibroblast benzeri hücreler, yukarıda tarif edilen prosedüre göre inflamatuar artrit dokusundan bağımsız olarak izole edildi (Şekil 2A,B). Makrofaj benzeri hücreler adım 5.7'den hemen sonra kullanıldı. Fibroblast benzeri hücreler başlangıçta adım 4.4'ten sonra alt birleşim olacak şekilde kültürlendi ve daha sonra yeni bir kültür kabın...
Tartışmalar
Burada geliştirilen bu yöntem, hem SF'leri murin artritinden hem de yerleşik makrofajları bir dizi organdan izole etmek için önceki teknikleri geliştirir 7,11. Modifiye yöntem, hem makrofajları hem de fibroblastları enflamatuar sinovyumdan yüksek saflıkta izole edebilir ve basit ve tekrarlanabilir. Yöntem, hücre sıralayıcı gibi karmaşık aletler gerektirmediğinden, herkes bunu gerçekleştirebilir. Ek olarak, mevcut teknik, antikorlarla tedavi ...
Açıklamalar
Yazarlar herhangi bir çıkar çatışması olmadığını beyan ederler.
Teşekkürler
Yazarlar, Tıbbi Araştırma Destek Bölümü, İleri Araştırma Destek Merkezi (ADRES) personeline ve Ehime Üniversitesi Proteo-Bilim Merkezi (PROS) Bütünleştirici Patofizyoloji Bölümü üyelerine teknik yardımları ve yardımcı destekleri için teşekkür eder. Bu çalışma kısmen Japonya Bilimi Teşvik Derneği (JSPS) KAKENHI hibeleri JP17K17929, JP19K16015, JP21K05974 (NS'ye) ve JP23689066, JP15H04961, JP15K15552, JP17K19728, JP19H03786 (YI'ye); Osaka İnatçı Hastalıklar Tıbbi Araştırma Vakfı, Nakatomi Vakfı, Japon Kemik ve Mineral Araştırmaları Derneği (JSBMR) Yükselen Yıldızlar Hibesi, Sumitomo Vakfı, SENSHIN Tıbbi Araştırma Vakfı, Mochida Memorial Vakfı (NS'ye); ve Takeda Bilim Vakfı Tıbbi Araştırma hibesi, UCB Japonya (UCBJ) proje hibesi ve JSBMR Frontier Scientist hibesi 2019 (YI'ye).
Malzemeler
| Name | Company | Catalog Number | Comments |
| 5.0 g/L Trypsin/5.3 mmol/L EDTA solution | nacalai tesque | 35556-44 | Diluted with HBSS |
| Antibiotic–antimycotic (anti/anti) | Gibco | 15240-062 | |
| Butterfly needle | TERUMO | SV-23DLK | 23G |
| Cell strainer | Falcon | 352340 | 40 µm pore, Nylon |
| Cellmatrix Type I-C | Nitta gelatin | 637-00773 | Type I-C collagen |
| Centriguge tube 15 | TPP | 91014 | 15 mL tube |
| Centriguge tube 50 | TPP | 91050 | 50 mL tube |
| Collagenase from C. Histolyticum | Sigma | C5138 | Type IV collagenase |
| Dulbecco’s Modified Eagle Medium GlutaMax (DMEM) | Gibco | 10569-010 | |
| Fetal bovine serum (FBS) | SIGAM | 173012 | Heat inactivation was performed |
| Hanks' balanced salt solution (HBSS) | Wako | 085-09355 | |
| Scissors | Bio Research Center | PRI28-1525A | |
| Tissue culture dish 40 | TPP | 93040 | For cell culture |
| Tissue culture dish 60 | TPP | 92006 | For cell culture |
| Tweezers | KFI | 1-9749-31 | Fine-point |
| Tweezers | Bio Research Center | PRI28-1522 | Serrated tip |
| ZEISS Stemi 305 | ZEISS | STEMI305-EDU | Stereomicroscope |
Referanslar
- Smolen, J. S., Aletaha, D., McInnes, I. B. Rheumatoid arthritis. Lancet. 388 (10055), 2023-2038 (2016).
- McInnes, I. B., Schett, G. The pathogenesis of rheumatoid arthritis. The New England Journal of Medicine. 365 (23), 2205-2219 (2011).
- Kurowska-Stolarska, M., Alivernini, S. Synovial tissue macrophages: friend or foe. RMD Open. 3 (2), (2017).
- Hannemann, N., Apparailly, F., Courties, G. Synovial macrophages: from ordinary eaters to extraordinary multitaskers. Trends in Immunology. 42 (5), 368-371 (2021).
- Alivernini, S., et al. Distinct synovial tissue macrophage subsets regulate inflammation and remission in rheumatoid arthritis. Nature Medicine. 26 (8), 1295-1306 (2020).
- Saeki, N., Imai, Y. Reprogramming of synovial macrophage metabolism by synovial fibroblasts under inflammatory conditions. Cell Communication and Signaling. 18 (1), 188 (2020).
- Armaka, M., Gkretsi, V., Kontoyiannis, D., Kollias, G. A standardized protocol for the isolation and culture of normal and arthritogenic murine synovial fibroblasts. Protocol Exchange. , (2009).
- Saeki, N., et al. Epigenetic regulator UHRF1 orchestrates proinflammatory gene expression in rheumatoid arthritis in a suppressive manner. The Journal of Clinical Investigation. 132 (11), (2022).
- Midwood, K., et al. Tenascin-C is an endogenous activator of Toll-like receptor 4 that is essential for maintaining inflammation in arthritic joint disease. Nature Medicine. 15 (7), 774-780 (2009).
- You, D. G., et al. Metabolically engineered stem cell-derived exosomes to regulate macrophage heterogeneity in rheumatoid arthritis. Science Advances. 7 (23), 0083 (2021).
- Ogawa, K., Tsurutani, M., Hashimoto, A., Soeda, M. Simple propagation method for resident macrophages by co-culture and subculture, and their isolation from various organs. BMC Immunology. 20 (1), 34 (2019).
- Andrä, I., et al. An evaluation of T-cell functionality after flow cytometry sorting revealed p38 MAPK activation. Cytometry Part A. 97 (2), 171-183 (2020).
- Ryan, K., Rose, R. E., Jones, D. R., Lopez, P. A. Sheath fluid impacts the depletion of cellular metabolites in cells afflicted by sorting induced cellular stress (SICS). Cytometry Part A. 99 (9), 921-929 (2021).
- Llorente, I., García-Castañeda, N., Valero, C., González-Álvaro, I., Castañeda, S. Osteoporosis in rheumatoid arthritis: dangerous liaisons. Frontiers in Medicine. 7, 601618 (2020).
- Croft, A. P., et al. Distinct fibroblast subsets drive inflammation and damage in arthritis. Nature. 570 (7760), 246-251 (2019).
- Wei, K., et al. Notch signalling drives synovial fibroblast identity and arthritis pathology. Nature. 582 (7811), 259-264 (2020).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır