Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Temiz Oda Ortamları ve Hücresel Terapiler için Mikrobiyal Kontrol ve İzleme Stratejileri
Bu Makalede
Özet
Protokol, temiz oda ortamında mikrobiyal biyolojik yükü en aza indirmek için en iyi uygulamaları özetler ve çevresel izleme, proses izleme ve ürün sterilite testi gibi stratejileri içerir. Mevcut iyi doku uygulamaları standartlarını ve mevcut iyi üretim uygulamaları standartlarını karşılamak için gerekli olan üretim ve test tesisleri ile ilgilidir.
Özet
Sağlam önlük, temizlik, çevresel izleme ve personel izleme önlemlerini içeren iyi doğrulanmış ve bütünsel bir program, tesislerin kontrol durumunda çalışmasını sağlamak için hücresel terapi üretim paketlerinde ve ilgili test laboratuvarlarında mikrobiyal biyoyükü en aza indirmek için kritik öneme sahiptir. Sterilite testi gibi kalite kontrol önlemleri yoluyla ürün güvenliğinin sağlanması, hem minimum düzeyde manipüle edilmiş (bölüm 361) hem de minimum düzeyde manipüle edilmiş (bölüm 351) insan hücreleri, dokuları ve hücresel ve doku bazlı ürünler (HCT/P) için düzenleyici bir gerekliliktir. Bu videoda, Amerika Birleşik Devletleri Farmakopesi (USP<71>) ve Ulusal Sağlık Enstitüleri (NIH) Alternatif Sterilite Test Yöntemi tarafından sağlanan, önlük, temizlik, malzemelerin evrelendirilmesi, çevresel izleme, süreç izleme ve doğrudan aşılama kullanılarak ürün sterilite testi dahil olmak üzere temiz oda ortamında çalışmak için en iyi aseptik uygulamaların nasıl geliştirileceği ve dahil edileceği konusunda adım adım bir kılavuz sunuyoruz. Bu protokol, mevcut iyi doku uygulamalarını (cGTP) ve mevcut iyi üretim uygulamalarını (cGMP) karşılaması beklenen kuruluşlar için bir referans kılavuzu olarak tasarlanmıştır.
Giriş
Çevresel izleme (EM), proses izleme ve ürün sterilite testi yoluyla güçlü bir mikrobiyal izleme programının uygulanması, hücresel terapi laboratuvarlarında mevcut iyi doku uygulamaları (cGTP) ve mevcut iyi üretim uygulamaları (cGMP) için düzenleyici bir gerekliliktir1. Ek olarak, Amerika Birleşik Devletleri Gıda ve İlaç Dairesi (FDA), ürünün kalite kontrol (QC) testini gerçekleştiren laboratuvarın da aseptik dolum işlemleri için kullanılanlarla karşılaştırılabilir tesisler ve kontroller kullanmasını beklemektedir2.
Bu protokolün dört ana bölümü vardır: 1) Personel önlükleme, temizlik ve malzemelerin sahnelenmesi dahil olmak üzere aseptik uygulamalar; 2) EM, uygulanabilir hava ve yüzey kültürleri ve canlı olmayan partikül hava izleme dahil; 3) çökeltme plakaları ve eldivenli parmak ucu örneklemesi dahil olmak üzere proses izleme; ve 4) özet Amerika Birleşik Devletleri Farmakopesi (USP) <71> yöntem3 veya NIH Alternatif Sterilite Test Yöntemi4 aracılığıyla ürün sterilite testi. Birlikte kullanıldığında, bu önlemler bir tesisin kontrol durumunda kalmasını sağlamak için etkili bir yöntem olabilir.
Burada anlatılan teknikler yeni değildir; Bununla birlikte, düzenleyicilerden ve meslek örgütlerinden gelen mevcut standartlar ayrıntıdan yoksundur, bu da özellikle yerinde üretim ve ürün sterilite testlerinin hızlı bir şekilde ortaya çıktığı akademik merkezlerde, mikrobiyal izlemenin veya standart dışı uygulamaların uygulanmasının olmamasına neden olmuştur 1,5,6 . Bu protokol, son kullanıcı doğrulama ve risk değerlendirmeleri ile birlikte kullanıldığında yasal gereklilikleri karşılayan bir mikrobiyal izleme ve kontrol programı oluşturmak için bir kılavuz olarak kullanılabilir.
Protokol
1. Aseptik uygulamalar
- Temiz oda alanı için personel önlüğü
NOT: Bu prosedür, sınıflandırılmamış bir alanda ilk önlük, ardından Uluslararası Standartlar Örgütü (ISO) 8 alanına ve ardından bir ISO7 alanına girmeye dayanmaktadır. Bu prosedür, mevcut alanı temiz oda işlevine dönüştürmeye çalışan laboratuvarlar için geçerlidir. İdeal olarak, tüm ilk önlükler ISO8 sınıflandırılmış bir alanda (sınıflandırılmamış bir alanda değil) gerçekleşir.- Gevşek saçları sabitleyin. Ellerinizi yıkayın ve ovma pantolonlarına dönüştürün (uzun kollu ovma üstleri ve tam boy ovma pantolonları tercih edilir). Toplanın ve ayakkabı kapakları açık temiz oda ayakkabılarına geçin.
- Başlangıçta alkol bazlı bir el dezenfektanı kullanarak elleri sterilize edin ve daha sonra aşağıdaki adımların her biri arasında tekrar uygulayın: steril olmayan eldivenler ve daha sonra varsa sakal örtüsü (herhangi bir miktarda görünür yüz kılı için) giyin. Steril olmayan bir kabarık giyin ve uzun kollu ovma üstleri kullanılmamışsa ön kolları steril olmayan kollarla örtün.
- Ayakkabı kapağı çıkarıldıktan sonra her ayağınızla ISO8 antre kapısının önündeki yapışkan paspasa basarak ayakkabı kapaklarını çıkarın. Girişten önce ayağın tamamının yapışkan paspasla temas ettiğinden emin olun. Ayakkabı kapaklarını atın ve eldivenleri ve kapı kolunu %70 steril izopropil alkol (sIPA) ile dekontamine edin. ISO8 antresine girin.
- Steril bir başlık, steril yüz maskesi, steril tulumlar, steril bot kılıfları ve güvenlik gözlükleri toplayın. Eldivenleri %70 sIPA ile dekontamine edin. Güvenlik gözlükleri takın ve malzemeleri adım 1.5'e göre temiz bir yüzeye yerleştirin.
- Özel temiz oda ayakkabılarının üzerine yeni bir çift steril olmayan ayakkabı kılıfı takın ve ikincil antrenin önündeki yapışkan paspasa adım atın. Her ayağın tamamının yapışkan paspasla temas ettiğinden emin olun. Eldivenleri %70 sIPA ile dekontamine edin. Sahnelenmiş önlük malzemelerini toplayın ve sınır çizgisinin kirli tarafında kalan ikincil ISO7 antresine girin.
- Steril başlığı ve steril tulumu takın, sadece önlük malzemesinin iç kısmına dokunun ve tam bir sızdırmazlık oluşturmak için davlumbazın boynunun tulumun içine sıkışmasını sağlayın. İkincil steril bot kapaklarını takın. Her takma adımı arasında eldivenleri %70 sIPA ile dekontamine edin.
- Önlüğün uygun şekilde giyildiğini doğrulayın, eldivenleri %70 sIPA ile dekontamine edin ve ISO7 alanına girin.
NOT: Önlük malzemesinin bütünlüğünü periyodik olarak kontrol edin. Tehlikeye girerse, derhal temiz odadan çıkın ve yeniden önlük giyin.
- Biyolojik güvenlik kabini (BSC) için takma
- Bu ek uygulamalarla yukarıdaki adım 1.1'e göre giyin.
- Steril eldivenleri ve steril kolları toplayın. BSC'yi adım 1.4'e göre temizleyin ve malzemeleri adım 1.5'e göre hazırlayın. Eldivenleri %70 sIPA ile dekontamine edin.
- Aseptik olarak tulumun üzerine steril manşonlar takın, varsa başparmak halkalarını kullanın. Mevcut eldivenlerin üzerine steril eldivenler takın ve eldivenin manşetinin steril manşonun üzerine uzanmasını sağlayın. Her adım arasında eldivenleri %70 sIPA ile dekontamine edin. BSC'ye girin.
NOT: Önlük malzemesinin bütünlüğünü periyodik olarak kontrol edin. Tehlikeye girerse, derhal temiz odadan çıkın ve yeniden önlük giyin.
- Önlük malzemelerinin sökülmesi
- BSC'den çıkın ve üst eldiven çiftini ve steril kolları dikkatlice çıkarın. İç eldivenleri %70 sIPA ile dekontamine edin.
- İkincil ve ardından birincil antreye girin ve kapının her adım arasında tamamen kapanmasını bekleyin. Malzemeleri aşağıdaki sırayla çıkarın: dış steril bagaj kapakları, tulum, başlık ve yüz maskesi.
- Birincil antreden çıkın ve steril olmayan önlüğü çıkarın.
NOT: Sınıflandırılmamış alandaki kaldırma sırası önemli değildir; Bununla birlikte, steril olmayan iç ayakkabı kapakları, sınıflandırılmamış alanlarda saklanmak üzere temiz oda ayakkabılarında kalmalıdır. - Alkol bazlı bir el dezenfektanı kullanarak elleri sterilize edin ve sokak kıyafetlerine geri dönün.
- Temiz oda yüzeylerinin ve BSC'nin temizlenmesi
- Elde taşınan bir temizleme paspası takın veya temiz, az tiftikli bir mendil edinin. Düşük tiftikli bir mendil kullanıyorsanız, mendili dörde katlayın ve her yüzey arasında döndürün. Paspas kafasını veya düşük tiftikli mendili onaylı bir dezenfektanla doyurun.
- Arkadan öne (veya yukarıdan aşağıya) çalışarak, üst üste binen mendilleri kullanarak BSC'yi aşağıdaki sırayla temizleyin: HEPA difüzör ızgarası (BSC'nin üst kısmı), BSC'nin arka duvarı, BSC'nin her iki yan duvarı, kanat ve çalışma yüzeyi. Son olarak, kalan dezenfektanı çıkarmak için BSC'nin kanadını %70 sIPA kullanarak silin. Tipik bir BSC temizleme modeli için Şekil 1'e bakın.
- Malzeme ve ekipmanların sınıflandırılmış ortamlara hazırlanması
- Mikropların transferini en aza indirmek için sınıflandırılmamış veya daha düşük sınıflandırılmış bir alandan daha yüksek sınıflandırılmış bir alana (örneğin, bir ISO8'den ISO7 alanına) transfer gerektiren tüm malzemeleri dekontamine edin (yani aşamalandırın). Malzemelerin aynı ISO sınıflandırma seviyesindeki alanlar arasında aktarılması evreleme gerektirmez.
NOT: Malzemeler terminal olarak sterilize edilmişse ve birden fazla torba içindeyse, dış torbayı/torbayı çıkarın ve malzemeyi sınıflandırılmış alana taşıyın; iç torbanın/poşetin silinmesi gerekli değildir. - Düşük tiftikli bir mendil elde edin ve mendil kirlendikçe temiz bir tarafa döndürmek için mendili dörde katlayın. Mendili %70 sIPA veya onaylı bir dezenfektan ile doyurun.
- Üst üste binen mendiller kullanarak malzemenin/ekipmanın dışını silin. Sökülebilir paket contalarının iç kısımları ve ekipman üzerindeki köşeler/girintiler ve diğer düzensiz şekilli sarf malzemeleri de dahil olmak üzere öğenin tüm alanlarının silindiğinden emin olun. Tekerlekli ekipmanlar için, hazırlama işlemi sırasında tüm tekerleğin silindiğinden emin olun (tekerleklerin döndürülmesine izin vermek için ekipmanın hafifçe devrilmesi gerekebilir).
- Mikropların transferini en aza indirmek için sınıflandırılmamış veya daha düşük sınıflandırılmış bir alandan daha yüksek sınıflandırılmış bir alana (örneğin, bir ISO8'den ISO7 alanına) transfer gerektiren tüm malzemeleri dekontamine edin (yani aşamalandırın). Malzemelerin aynı ISO sınıflandırma seviyesindeki alanlar arasında aktarılması evreleme gerektirmez.

Şekil 1: BSC temizleme modeli örneği. Arkadan öne (veya yukarıdan aşağıya) çalışarak, üst üste binen mendilleri kullanarak BSC'yi aşağıdaki sırayla temizleyin: HEPA difüzör ızgarası (BSC'nin üst kısmı), BSC'nin arka duvarı, BSC'nin her iki yan duvarı, kanat ve çalışma yüzeyi. Son olarak, kalan dezenfektanı çıkarmak için BSC'nin kanadını %70 sIPA kullanarak silin. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
2. Çevresel izleme (EM)
- Uygulanabilir yüzey örneklemesi
- Örnekleme oturumu için gerekli malzemeleri adım 1.5'e göre hazırlayın ve bölüm 1'e göre sınıflandırılmış alana giyin.
NOT: Yüzey örneklemesi, belirtilen herhangi bir yerde hava örneklemesinden önce yapılmalıdır. Bir alanı yüzey örneklemesi için birden fazla plaka kullanıyorsanız, tam olarak aynı konumu örneklemeyin. Sadece tam teması sağlamak ve agarın potansiyel hasarını önlemek için düz yüzeyleri örneklemek için temas plakaları kullanın. - Her örnekleme alanı için lesitinaz ve ara (TSALT) plakalı bir triptik soya agarını ve lesitinaz ve ara (SABLT) plakalı bir Sabouraud dekstroz agarını toplayın ve etiketleyin. Plakanın tabanını bir elinizle tutarak, yükseltilmiş agar yüzeyine dokunmamaya dikkat ederek kapağı aseptik olarak çıkarın.
- Yükseltilmiş agar'ı numune alınan yüzeye dokundurun, tüm yüzeyin temas halinde olduğundan emin olun ve plakaya sert basınç uygulayın. Plakayı en az 5 saniye boyunca yüzeyle temas halinde bırakın.
- KRİTİK: Plakayı numune alınan yüzey üzerinde yanal olarak hareket ettirmeyin, çünkü bu, potansiyel büyümeyi yüzey alanına yayabilir ve bireysel kolonilerin çözünürlüğünü zorlaştırabilir. Numune alma sırasında temas plakasına aşırı kuvvet uygulamayın, çünkü agar yüzeyi çatlayabilir.
- Yükseltilmiş agar yüzeyine dokunmamaya dikkat ederek kapağı aseptik olarak değiştirin. Kontak plakasında kilitleme sistemi varsa kapağı yerine kilitleyin. Yüzeydeki artık ortamları temizlemek için numune alma alanını %70 sIPA ile temizleyin. Plakaları gevşek bir şekilde torbalayın ve kültürleri Tablo 1'de açıklandığı gibi inkübe edin. Bir TSALT yüzey örnekleme plakası üzerinde iki ayrı koloni morfolojisine sahip üç koloni oluşturan birimin (CFU) büyümesini gösteren temsili bir görüntü Şekil 2'de gösterilmiştir. Şekil 3, numune toplama sırasında zayıf aseptik tekniğe atfedilebilen, plakanın kenarında büyüme ile bir TSALT plakasının kontaminasyonunu göstermektedir.
- Örnekleme oturumu için gerekli malzemeleri adım 1.5'e göre hazırlayın ve bölüm 1'e göre sınıflandırılmış alana giyin.
- Canlı hava örneklemesi
- Örnekleme oturumu için gerekli malzemeleri adım 1.5'e göre hazırlayın ve bölüm 1'e göre sınıflandırılmış alana giyin.
- Her örnekleme alanı için bir triptik soya agar (TSA) plakası ve bir Sabouraud dekstroz agar (SAB) plakası toplayın ve etiketleyin. Kafanın kirlenmesini önlemek için numune alma kafasını aseptik olarak çıkararak hava numune alma cihazını hazırlayın.
- Numune alma kafasını bir elinizde tutarak, ortamı aseptik olarak numune alma cihazındaki plaka tutucuya yerleştirin. Diğerlerinden daha uzun bir çatal varsa, önce ortamı daha uzun uçlara yerleştirin ve ardından plakayı sabitlemek için plakayı kalan uçlara doğru itin.
- Plaka kapağını aseptik olarak çıkarın ve numune alma işlemi tamamlanana kadar temizlenmiş bir yüzeye yerleştirin. Numune alma kafasını aseptik olarak değiştirin ve sabitleyin, kafanın kirlenmesini önlemek için sadece dış kenarı kavrayın. Çok başlı hava örnekleyici kullanılıyorsa, kalan ortam için 2.2.2-2.2.4 arasındaki adımları tekrarlayın.
- Hava örnekleyiciyi, numune alma kafaları hava akımı hareketinin baskın yönüne bakacak şekilde numune alma konumuna yerleştirin. Canlı olmayan hava numune alma cihazından gelen egzozun (aynı anda numune alıyorsanız) uygulanabilir numune alma cihazına müdahale etmediğinden emin olun. Hava örnekleyicinin doğrulanmış ayarlara ayarlandığından emin olun ve numune alma döngüsünü başlatın.
- Numune alma döngüsü tamamlandığında, kafanın kirlenmesini önlemek için sadece dış kenarı kavrayarak numune alma kafasını numune alma cihazından aseptik olarak çıkarın. Örnekleme kafasını bir elinizde tutun ve agar plakasının kapağını aseptik olarak değiştirin. Plakayı plaka tutucusundan çıkarın. Plakaları gevşek bir şekilde torbalayın ve kültürleri Tablo 1'de açıklandığı gibi inkübe edin.
- Numune alma kafasını ve plaka tutucunun etrafındaki alanı %70 sIPA ile dezenfekte edin. Numune alma kafasını aseptik olarak sabitleyin ve sadece dış kenarı kavrayın. Çok başlı bir hava örnekleyici kullanılıyorsa, kalan ortam için adım 2.2.6 ve adım 2.2.7'yi tekrarlayın.
NOT: Şekil 4, kontamine bir örnekleme kafasının neden olduğu büyüme ile TSA aktif hava örnekleme kültürünü göstermektedir. Tersine, Şekil 5, büyüme olmayan bir TSA aktif hava örnekleme kültürünü temsil etmektedir. Örnekleme kafasından hava etkisi girintileri görüntüde görülebilir.
- Canlı olmayan örnekleme
- Her kullanım günü için numune alma faaliyetlerinden önce lazer partikül sayacında sıfır kontrol gerçekleştirin. İzokinetik kafayı partikül sayacının örnekleme portuna doğrudan veya numune alma yeri için gerektiği şekilde bir boru uzunluğuna yapıştırın.
- Boru uygulanırsa, kısa bir uzunluk kullanın, çünkü >1 m uzunluğundaki borular ≥1 μm'lik parçacıkların numaralandırılmasında sorunlara neden olabilir ve ayrıca tüpte gereksiz bükülmelere neden olabilir. Partikül sayacının doğrulanmış ayarlara ayarlandığından emin olun. Numune alma sırasında hava akımının bozulmasını önlemek amacıyla numune alma alanından çıkışa izin vermek için yaklaşık 30 sn'lik bir gecikme ayarlanması önerilir.
- Lazer parçacık sayacının izokinetik kafasını, izokinetik kafa hava akımı hareketinin baskın yönüne bakacak şekilde örnekleme konumuna yerleştirin. Uygun hava numune alma cihazından gelen egzozun (aynı anda numune alıyorsa) uygun olmayan numune alma cihazına müdahale etmediğinden emin olun. Hava akışının tek yönlü olmadığı veya hava akış düzeninin bilinmediği alanlar için, izokinetik başlığın dikey olarak yukarı baktığından emin olun.
NOT: Hava numune alma cihazının yakınında rotasyonel dezenfektan veya %70 sIPA aerosol haline getirilmişse, numune alma döngüsüne başlamadan önce en az 5 dakika bekleyin. - Örnekleme döngüsünü başlatın ve hava akışını kesintiye uğratmamak için örnekleme alanından yavaşça çıkın.
KRİTİK: Bir numune alma döngüsü sırasında hava numune alma cihazının yakınındaki sıvıları aerosol haline getirmeyin, çünkü bu yüksek canlı olmayan sayımlara neden olur. - Örnekleme tamamlandığında, lazer parçacık sayacını alın. Ortalama parçacık sayılarını 0,5 μm olarak kaydedin. Bazı tesisler ayrıca 5,0 μm'yi izleyebilir ve trend gösterebilir.
- Bir sonraki örnekleme konumu için 2.3.3-2.3.6 adımlarını yineleyin. Odalar veya BSC'ler arasında hareket ediyorsanız, uygun olmayan partikül numune alma cihazının dışını %70 sIPA veya onaylanmış bir dezenfektan ile silin. İzokinetik kafanın içine dezenfektan almaktan kaçının, çünkü bu yanlış partikül sayımlarına neden olabilir.
| Kategori | Medya | Kültür koşulları | Kültür gözlemi | Sonuç -ları | ||||||
| Çevresel izleme | TSA (canlı hava) | 30 °C-35 °C, hava, en az 3 gün | Kuluçka sonu | Her tesisin KG grubu, her örnekleme türü ve konumu için uyarı ve eylem sınırları belirlemelidir. ISO sınıflandırmasına dayalı uygulanabilir numuneler için eylem sınırları PIC/S 009-16 (Ekler) 18 ve ISO-14644-1 7 kullanılarak yönlendirilebilir. Canlı olmayan hava numuneleri için eylem sınırları tipik olarak ISO sınırının bir yüzdesine ayarlanır (ör. %99). Uygun numuneler için uyarı sınırları tipik olarak Eylem sınırının veya ISO sınırının bir yüzdesine ayarlanır (ör. %95). Uyarı ve eylem seviyelerinin belirlenmesi ve seçilen kültür koşullarının doğrulanması ile ilgili daha fazla ayrıntı için PDA TR-13 ve USP<1116> 8,9'a bakın. | ||||||
| SAB (canlı hava) | 20 °C-25 °C, hava, en az 7 gün | |||||||||
| TSALT (canlı yüzey) | 30 °C-35 °C, hava, en az 3 gün | EM plakalarının temsili görüntüleri Şekil 2, Şekil 3, Şekil 4 ve Şekil 5'te gösterilmiştir. | ||||||||
| SABLT (canlı yüzey) | 20 °C-25 °C, hava, en az 7 gün | |||||||||
| Süreç izleme | TSA (çökeltme plakası) | 30 °C-35 °C, hava, en az 3 gün | Sadece bilgi amaçlıdır. Başarısız bir ürün sterilite testine yanıt olarak bir OOS araştırması durumunda yararlı bilgiler sağlar. | |||||||
| SAB (çökeltme plakası) | 20 °C-25 °C, hava, en az 7 gün | Pozitif bir çökeltme plakası örneği için Şekil 6'ya bakın. | ||||||||
| Eldivenli parmak ucu örneklemesi | cesaret | 30 °C-35 °C, hava, en az 48 saat gün ve ardından 20 °C -25 °C en az 5 gün 19. | GFS için kabul edilebilirlik kriterleri, PIC / S 009-16 (Ekler) 18'e göre < 1 CFU / plakadır (yani, büyüme yoktur). Kabul edilebilirlik kriterleri, tesis QA'sının takdirine bağlı olarak değiştirilebilir. | |||||||
| Ürün sterilite testi | TSB (USP<71>) | 20 °C-25 °C, hava, en az 14 gün boyunca | Kuluçka dönemi boyunca periyodik olarak (3, 5, 7 ve 14. günler) | Büyüme yok. | ||||||
| FTM (USP<71>) | 30 °C-35 °C, hava, en az 14 gün boyunca | |||||||||
| iFA+ (NIH yöntemi) | 30 °C-35 °C, hava, en az 14 gün boyunca | BacT/ALERT Dual-T cihazı ile otomatik olarak izleme. Kalıp topları için inkübasyonun sonunda her şişenin görsel kontrolü şiddetle tavsiye edilir. | BacT/ALERT tarafından otomatik olarak algılanamayan görünür kalıp toplarının bir örneği için Şekil 8'e bakın. | |||||||
| iFN+ (NIH yöntemi) | ||||||||||
| SAB (NIH yöntemi) | En az 14 gün boyunca 20 °C-25 °C | Kuluçka dönemi boyunca periyodik olarak (3, 5, 7 ve 14. günler) | ||||||||
Tablo 1: Önerilen kültür koşullarının ve beklenen sonuçların özeti. Burada açıklanan kültür koşulları, NIH'de kullanılan doğrulanmış bir programa dayanan önerilerdir. Her son kullanıcının kendi mikrobiyoloji test programını doğrulaması gerekmektedir. Mikrobiyal kontrol ve test stratejileri, tesis tasarımı, tesis florası ve ürün risk sınıflandırması gibi değişkenlere bağlı olarak enstitüler arasında farklılık gösterebilir.
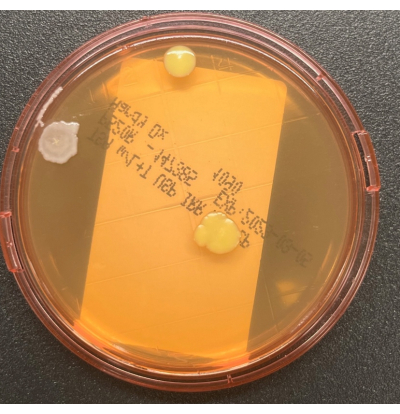
Şekil 2: TSALT plakasındaki büyüme. İki ayrı koloni morfolojisinin üç CFU'sunu gösteren TSALT yüzey örnekleme plakası. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
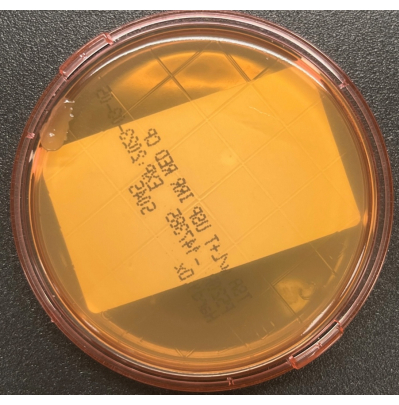
Şekil 3: Toplama sırasında TSALT plakasının kirlenmesi. Plakanın kenarında tek bir koloni gösteren TSALT yüzey kültürü, örnekleme işlemi sırasında zayıf aseptik kullanımın göstergesidir. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.

Şekil 4: Kirlenmiş hava örnekleme kafası kullanılarak elde edilen kültür. Karışık morfolojilerin >100 koloni oluşturan birimini (CFU) gösteren bir TSA aktif hava örnekleme kültürü örneği. Büyüme paterni, örnekleme kafasının kirlendiğini gösterir. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.

Şekil 5: TSA aktif uygulanabilir hava plakasında büyüme yok. TSA aktif uygulanabilir hava plakası, inkübasyondan sonra büyüme göstermez. Görüntüde aktif hava örnekleyici kafasından girintiler görülebilir. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
3. Süreç izleme
- Çökeltme plakaları (pasif hava izleme)
- TSA ve SAB plakalarını etiketli plakaları çalışma alanının yakınına, ancak teste müdahale etmeyecek bir alana yerleştirin. Numune alma başlangıç zamanını belgeleyin ve kapakları BSC'de çalışma alanından uzakta temiz bir yüzeye yerleştirerek her iki plakayı da aseptik olarak açın.
- Çökeltme plakaları, agarın kurumasını önlemek için maksimum 4 saat boyunca açık olabilir. İşlemin sonunda plakaların kapaklarını kapatın. Plakaları gevşek bir şekilde torbalayın ve kültürleri Tablo 1'de açıklandığı gibi inkübe edin. Şekil 6, bir TSA hava çökeltme plakası üzerinde tek bir koloni kirleticisini göstermektedir.
- Eldivenli parmak ucu örneklemesi (GFS)
- İki etiketli TSALT plakası edinin. Bir plakanın kapağını aseptik olarak çıkarın ve numune alma alanından uzakta temiz bir çalışma yüzeyine yerleştirin.
- Her parmağın pedini ve bir elin baş parmağını plakanın yüzeyine yavaşça yuvarlayın (Şekil 7). Uç yerine her parmağın / başparmağın en büyük yüzey alanını örnekleyin. Agar yüzeyini çatlatmadan agar üzerinde hafif çöküntüler yapmak için yeterli kuvvet kullanın.
- Aseptik olarak kapağı tekrar plakanın üzerine yerleştirin ve diğer el için adım 3.2.2'yi tekrarlayın. Numune alma işleminin tamamlanmasında elleri %70 sIPA ile sterilize edin. Plakaları gevşek bir şekilde torbalayın ve kültürleri Tablo 1'de açıklandığı gibi inkübe edin.
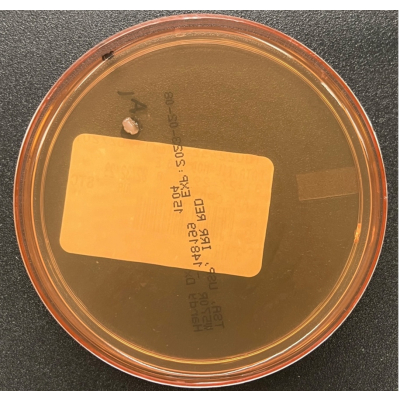
Şekil 6: TSA hava çökeltme plakasındaki büyüme. BSC'de pasif hava prosesi izlemesi sırasında kültürlenen tek bir kirletici madde kolonisini gösteren bir TSA hava çökeltme plakası. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.

Şekil 7: Eldivenli parmak ucu örneklemesi. Her parmağın/başparmağın en geniş yüzey alanını (veya pedini) kullanarak eldivenli parmak ucu örnekleri elde etmek için doğru yöntem solda gösterilir. Yalnızca parmak ucunun örneklendiği yanlış işlem sağda gösterilir. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
4. Doğrudan ürün aşılaması ile sterilite testi
- USP<71'i takiben doğrudan aşılama>
- Gönderilen her test makalesi için bir etiketli triptik soya suyu (TSB) şişesi ve bir etiketli sıvı tiyoglikolat ortamı (FTM) şişesi edinin. Test oturumu için, uygulanabilir yüzey örneklemesi için bir TSALT ve bir SABLT, plakaları çökertmek için bir TSA ve bir SAB plakası ve GFS için iki TSALT plakası edinin.
- Adım 1.2'ye göre BSC içinde çalışmak için önlük. BSC'yi adım 1.4'e göre temizleyin. Malzemeleri adım 1.5'e göre BSC'ye yerleştirin. Kritik çalışma alanının temaslı örneklemesini adım 2.1'e göre gerçekleştirin, örneklemeden sonra yüzeyi% 70 sIPA ile silin. TSA ve SAB çökeltme plakalarını çalışma alanının yakınında adım 3.1'e göre hazırlayın.
- Test makalesini ve ilgili TSB ve FTM şişelerini edinin. TSB ve FTM şişelerinde septum varsa, koruyucu kapakları her şişeden çıkarın ve septumu steril bir alkollü mendille silin. TSB ve FTM şişelerinin vidalı bir üst kısmı varsa, kapağı şişelerden gevşetin (ancak kapağı çıkarmayın).
- Homojen bir süspansiyon sağlamak için test ürününü vorteks. Şişeleri, steril bir şırınga ve bir hipodermik iğne (septum kapakları için) veya bir pipetleyici (vidalı kapaklar için) kullanarak test ürününün doğrulanmış hacmiyle (10 mL / şişeye kadar) aşılayın.
- Aşılamadan sonra, septumu steril bir alkollü mendille silin ve inkübasyon sırasında hava değişimine izin vermek için steril bir havalandırma ünitesi yerleştirin. Vidalı şişeler için, şişeyi kapatın, ancak inkübasyon sırasında hava değişimine izin vermek için kapağı 1/4 ila 1/2 bir tur gevşek bırakın. Bu oturumda test edilecek her test makalesi için 4.1.3-4.1.5 arasındaki adımları yineleyin.
- TSA ve SAB çökeltme plakalarını aseptik olarak kapatın ve numune alma bitiş zamanını belgeleyin. GFS'yi adım 3.2'ye göre uygulayın, numune aldıktan sonra eldivenleri% 70 sIPA ile silin. Plakaları gevşek bir şekilde torbalayın ve kültürleri Tablo 1'de açıklandığı gibi inkübe edin.
- Tüm test malzemelerini BSC'nin dışına aktarın ve BSC'yi adım 1.4'e göre temizleyin.
- NIH Alternatif Sterilite Test Yöntemini takiben doğrudan aşılama
- Her test makalesi için biri FA +, bir i FN + etiketli ve birSAB plakası edinin. Test oturumu için, uygulanabilir yüzey örneklemesi için bir TSALT ve bir SABLT, plakaları çökertmek için bir TSA ve bir SAB plakası ve GFS için iki TSALT plakası edinin.
- Adım 1.2'ye göre BSC içinde çalışmak için önlük. BSC'yi adım 1.4'e göre temizleyin. Malzemeleri adım 1.5'e göre BSC'ye yerleştirin. Kritik çalışma alanının temaslı örneklemesini adım 2.1'e göre gerçekleştirin, örneklemeden sonra yüzeyi% 70 sIPA ile silin. TSA ve SAB çökeltme plakalarını çalışma alanının yakınında adım 3.1'e göre hazırlayın.
- Test makalesini ve ilişkili i FA +, iFN + ve SAB plakasını edinin. Koruyucukapakları i FA+ ve iFN+ şişelerinden çıkarın ve septumu steril alkollü mendille silin.
- Homojen bir süspansiyon sağlamak için test ürününü vorteks. Şişeleri, steril bir şırınga ve hipodermik iğne kullanarak test ürününün doğrulanmış hacmi (10 mL / şişeye kadar) ile aşılayın. Aşılamadan sonra septumu steril bir alkollü mendille silin. Şişeleri BacT/ALERT Dual-T cihazında Tablo 1'de açıklandığı gibi inkübe edin.
- Bir pipetleyici kullanarak, SAB plakasını test maddesinin doğrulanmış miktarı (en fazla 500 μL/plaka) ile aşılayın ve steril bir döngü kullanarak izolasyon için çizgi çizin. Numunenin inkübasyon için ters çevrildiğinde plaka kapağına akmadığından emin olmak için 10 dakika bekletin. Test makalesiyle aşılanmış her SAB plakasını plastik bir torbaya yerleştirin, gevşek bir şekilde bağlayın ve Tablo 1'de açıklandığı gibi inkübe edin.
- TSA ve SAB çökeltme plakalarını aseptik olarak kapatın ve numune alma bitiş zamanını belgeleyin. GFS'yi adım 3.2'de açıklandığı gibi uygulayın, numune aldıktan sonra eldivenleri %70 sIPA ile silin. Plakaları gevşek bir şekilde torbalayın ve kültürleri Tablo 1'de açıklandığı gibi inkübe edin. Kuluçka süresinin sonunda BacT/ALERT şişelerinin görsel muayenesi, cihaz tarafından tespit edilmemiş olabilecek küf toplarının tespiti için gereklidir (Şekil 8).
- Tüm test malzemelerini BSC'nin dışına aktarın ve BSC'yi adım 1.4'e göre temizleyin.
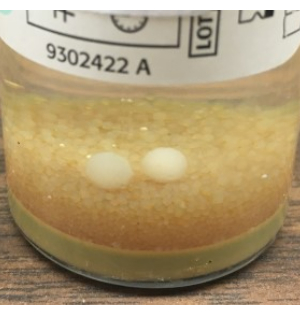
Şekil 8: BacT/ALERT tarafından tespit edilemeyen küf büyümesi. BacT/ALERT sistemi tarafından otomatik olarak algılanamayan, çıplak gözle görülebilen kalıp topları örneği. Bu bulgulara dayanarak, tüm BacT / ALERT şişelerinin terminal görsel muayenesini ve NIH Alternatif Sterilite Test Yöntemini kullanarak mantar kültürü için SAB plakasının eklenmesini öneririz. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
Sonuçlar
Beklenen sonuçlar Tablo 1'de açıklanmıştır. EM verileri gözden geçirilmeli ve uygun bir araştırma ve eylem, uyarı veya ISO limit sapmalarına yanıt verilerek takip edilmelidir. Canlı olmayan parçacıklar için bir sapma meydana gelirse, ISO 14644-Ek A, saniye A.5.57'ye göre devam edilmelidir. Gezi hemen tanımlanabilir anormal bir olaya atfedilebiliyorsa, orijinal örnekleme sonuçları belgelenmeli, orijinal sonuçları göz ardı etmek için bir not eklenmeli ve a...
Tartışmalar
Bu protokolde, temiz odalarda ve BSC'lerde aseptik tekniğin ve tek yönlü hava akışının sürdürülmesi de dahil olmak üzere birkaç kritik alan vardır. Aseptik manipülasyonlar, yukarıdan değil, ürünün yanından yapılmalıdır. Kapalı sistem işleme ve terminal olarak sterilize edilmiş hammaddelerin kullanılması tavsiye edilir. Kritik alanlarda konuşmaktan ve duvarlara veya ekipmanlara yaslanmaktan kaçınılmalıdır. Benzer şekilde, steril olmayan eşyalara gereksiz yere dokunmaktan ve düşen eşy...
Açıklamalar
Yazarlar çıkar çatışması olmadığını beyan ederler.
Teşekkürler
Bu çalışma, Ulusal Sağlık Enstitüleri Klinik Merkezi'nin Intramural Araştırma Programı tarafından desteklenmiştir. İçerik yalnızca yazarların sorumluluğundadır ve Ulusal Sağlık Enstitüleri'nin resmi görüşlerini temsil etmemektedir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 20-25°C Incubator | Lab preference | ||
| 30-35°C Incubator | Lab preference | ||
| Alcohol-based hand sanitizer | Lab preference | ||
| BacT/ALERT Dual-T instrument | BioMerieux Industry | ||
| Beard cover | Lab preference | ||
| Biosafety cabinet (BSC) | Lab preference | ||
| Cleanroom shoes | Lab preference | ||
| Fluidthioglycollate medium (FTM) | Hardy Diagnostics | U84 | USP |
| Handheld cleaning mop | Contec | 2665LF | |
| Hypodermic needle | Lab preference | ||
| iFA+ BacT/ALERT bottle | Biomerieux | 412990 | |
| iFN+ BacT/ALERT bottle | Biomerieux | 412991 | |
| Isokinetic head | Lab preference | ||
| Laser particle counter | TSI Incorporated | 9500-01 | |
| LpH III | Steris | 1S16CX | |
| Mirror | Lab preference | ||
| Non-sterile bouffant | Lab preference | ||
| Non-sterile gloves | Lab preference | ||
| Non-sterile shoe covers | Lab preference | ||
| Non-sterile sleeve covers | Lab preference | ||
| Parafilm | Lab preference | ||
| Peridox RTU | Contec | CR85335IR | |
| Plastic bag | Lab preference | ||
| Sabouraud Dextrose Agar with Lecithinase and Tween (SABLT) | Hardy Diagnostics | P595 | USP, irradiated |
| Sabouraurd Dextrose Agar (SAB) | Hardy Diagnostics | W565 | USP, irradiated |
| Safety glasses | Lab preference | ||
| Scrubs (top and bottom) | Lab preference | ||
| Spor-Klenx RTU | Steris | 6525M2 | |
| Sterile 70% isopropyl alcohol (IPA) | Decon CiDehol | 8316 | |
| Sterile alcohol wipe | Lab preference | ||
| Sterile boot covers | Kimberly Clark | Cat# varies based on size | |
| Sterile coveralls | Kimberly Clark | Cat# varies based on size | |
| Sterile face mask | Lab preference | ||
| Sterile gloves | Lab preference | ||
| Sterile hood | Kimberly Clark | Cat# varies based on size | |
| Sterile low-lint wipes | Texwipe | TX3210 | |
| Sterile mop cleaning pads | Contec | MEQT0002SZ | |
| Sterile sleeve covers | Kimberly Clark | 36077 | |
| Sterile spreading rod | Fisher Scientific | 14665231 | |
| Sterile syringe | Lab preference | ||
| Tacky mats | Lab preference | ||
| Tryptic Soy Agar (TSA) | Hardy Diagnostics | W570R | USP, irradiated |
| Tryptic Soy Agar with Lecithinase and Tween (TSALT) | Hardy Diagnostics | P520R | USP, irradiated |
| Tryptic Soy Broth (TSB) | Hardy Diagnostics | U46 | USP |
| Tubing | Lab preference | ||
| Vesphene III | Steris | 1S15CX | |
| Viable air sampler | Hardy Diagnostics | BAS22K | |
| Vortex | Lab preference |
Referanslar
- Cundell, T., Atkins, J. W., Lau, A. F. Sterility testing for hematopoietic stem cells. Journal of Clinical Microbiology. , (2023).
- United States Food and Drug Administration. Guidance for Industry. Sterile Drug Products Produced by Aseptic Processing - Current Good Manufacturing Practice. United States Food and Drug Administration. , (2004).
- United States Pharmacopeia - National Formulary. USP<71> Sterility Tests in USP43-NF38. United States Pharmacopeia - National Formulary. , (2022).
- England, M. R., Stock, F., Gebo, J. E. T., Frank, K. M., Lau, A. F. Comprehensive evaluation of compendial USP<71>, BacT/Alert Dual-T, and Bactec FX for detection of product sterility testing contaminants. Journal of Clinical Microbiology. 57 (2), 01548 (2019).
- Gebo, J. E. T., East, A. D., Lau, A. F. A side-by-side comparison of clinical versus current good manufacturing practices (cGMP) microbiology laboratory requirements for sterility testing of cellular and gene therapy products. Clinical Microbiology Newsletter. 43 (21), 181-191 (2021).
- Gebo, J. E. T., Lau, A. F. Sterility testing for cellular therapies: What is the role of the clinical microbiology laboratory. Journal of Clinical Microbiology. 58 (7), 01492 (2020).
- International Organization for Standardization. ISO 14644-1:2015 Cleanrooms and associated controlled environments - Part 1: Classification of air cleanliness by particle concentration. International Organization for Standardization. , (2015).
- Parenteral Drug Association. PDA Technical Report No. 13 Revised 2022 (TR 13) Fundamentals of an Environmental Monitoring Program. Parenteral Drug Association, Inc. , (2022).
- United States Pharmacopeia - National Formulary. USP<1116> Microbiological Evaluation of Cleanrooms and Other Controlled Environments in USP43-NF38 2S. United States Pharmacopeia - National Formulary. , (2020).
- Guinet, R., et al. Multicenter study on incubation conditions for environmental monitoring and aseptic process simulation. PDA journal of pharmaceutical science and technology. 71 (1), 43-49 (2017).
- Gordon, O., Berchtold, M., Staerk, A., Roesti, D. Comparison of different incubation conditions for microbiological environmental monitoring. PDA Journal of Pharmaceutical Science and Technology. 68 (5), 394-406 (2014).
- Anders, H. J., et al. Multisite qualification of an automated incubator and colony counter for environmental and bioburden applications in pharmaceutical microbiology. PDA Journal of Pharmaceutical Science and Technology. , (2022).
- United States Pharmacopeia - National Formulary. USP<1072> Disinfectants and Antiseptics. United States Pharmacopeia - National Formulary. , (2020).
- United States Pharmacopeia - National Formulary. USP<1071> Rapid Microbial Tests for Release of Sterile Short-Life Products: A Risk-Based Approach in USP43-NF38 2S. United States Pharmacopeia - National Formulary. , (2020).
- United States Pharmacopeia - National Formulary. PUSP<1223> Validation of Alternative Microbiological Methods in USP43-NF38 2S. United States Pharmacopeia - National Formulary. , (2020).
- Parenteral Drug Association. PDA Technical Report No. 33, Revised 2013 (TR 33) Evaluation, Validation and Implementation of Alternative and Rapid Microbiological Methods. Parenteral Drug Association, Inc. , (2013).
- Putnam, N. E., Lau, A. F. Comprehensive study identifies a sensitive, low-risk, closed-system model for detection of fungal contaminants in cell and gene therapy products. Journal of Clinical Microbiology. 59 (11), 0135721 (2021).
- Pharmaceutical Inspection Convention & Pharmaceutical Inspection Co-operation. Guide to Good Manufacturing Practice for Medicinal Products Annexes (PE 009-16 (Annexes)). Pharmaceutical Inspection Convention & Pharmaceutical Inspection Co-operation Scheme. , (2022).
- United States Pharmacopeia - National Formulary. USP<825> Radiopharmaceuticals - Preparation, Compounding, Dispensing, and Repackaging in USP43-NF38 2S. United States Pharmacopeia - National Formulary. , (2020).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır