Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Flujo de trabajo experimental y de análisis de datos para nanoindentación de materia blanda
En este artículo
Resumen
El protocolo presenta un flujo de trabajo completo para experimentos de nanoindentación de materiales blandos, incluidos hidrogeles y células. En primer lugar, se detallan los pasos experimentales para adquirir datos de espectroscopia de fuerza; luego, el análisis de dichos datos se detalla a través de un software Python de código abierto recientemente desarrollado, que se puede descargar gratis desde GitHub.
Resumen
La nanoindentación se refiere a una clase de técnicas experimentales en las que se utiliza una sonda de fuerza micrométrica para cuantificar las propiedades mecánicas locales de biomateriales blandos y células. Este enfoque ha ganado un papel central en los campos de la mecanobiología, el diseño de biomateriales y la ingeniería de tejidos, para obtener una caracterización mecánica adecuada de materiales blandos con una resolución comparable al tamaño de células individuales (μm). La estrategia más popular para adquirir tales datos experimentales es emplear un microscopio de fuerza atómica (AFM); Si bien este instrumento ofrece una resolución sin precedentes en fuerza (hasta pN) y espacio (sub-nm), su usabilidad a menudo está limitada por su complejidad que impide mediciones rutinarias de indicadores integrales de propiedades mecánicas, como el módulo de Young (E). Una nueva generación de nanoindentadores, como los basados en la tecnología de detección de fibra óptica, ha ganado popularidad recientemente por su facilidad de integración al tiempo que permite aplicar fuerzas sub-nN con resolución espacial μm, por lo que es adecuado para sondear las propiedades mecánicas locales de hidrogeles y células.
En este protocolo, se presenta una guía paso a paso que detalla el procedimiento experimental para adquirir datos de nanoindentación en hidrogeles y células utilizando un nanopenetrador de detección de fibra óptica en la parte superior de la virola disponible comercialmente. Mientras que algunos pasos son específicos para el instrumento utilizado en este documento, el protocolo propuesto se puede tomar como guía para otros dispositivos de nanoindentación, siempre que algunos pasos se adapten de acuerdo con las pautas del fabricante. Además, se presenta un nuevo software Python de código abierto equipado con una interfaz gráfica de usuario fácil de usar para el análisis de datos de nanoindentación, que permite la detección de curvas adquiridas incorrectamente, el filtrado de datos, el cálculo del punto de contacto a través de diferentes procedimientos numéricos, el cálculo convencional de E, así como un análisis más avanzado particularmente adecuado para datos de nanoindentación de células individuales.
Introducción
El papel fundamental de la mecánica en biología está hoy establecido 1,2. Desde tejidos enteros hasta células individuales, las propiedades mecánicas pueden informar sobre el estado fisiopatológico del biomaterial investigado 3,4. Por ejemplo, el tejido mamario afectado por el cáncer es más rígido que el tejido sano, un concepto que es la base de la popular prueba de palpación5. En particular, recientemente se ha demostrado que la enfermedad por coronavirus 2019 (COVID-19) causada por el coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) está subrayada por cambios en las propiedades mecánicas de las células sanguíneas, incluida la disminución de la deformabilidad de los eritrocitos y la disminución de la rigidez de los linfocitos y neutrófilos en comparación con las células sanguíneas de individuos sin SARS-CoV-26.
En general, la mecánica de las células y los tejidos está inherentemente entrelazada: cada tejido tiene propiedades mecánicas específicas que influyen y dependen simultáneamente de las células constituyentes y de la matriz extracelular (MEC)5. Debido a esto, las estrategias para estudiar mecánica en biología a menudo implican sustratos de ingeniería con estímulos mecánicos fisiológicamente relevantes para dilucidar el comportamiento celular en respuesta a esos estímulos. Por ejemplo, el trabajo seminal de Engler y sus colegas demostró que el compromiso del linaje de células madre mesenquimales está controlado por la elasticidad de la matriz, como se estudió en hidrogeles de poliacrilamida bidimensional blanda y rígida (PAAm)7.
Existen muchas estrategias para caracterizar mecánicamente el biomaterial bajo investigación, variando en escala espacial (es decir, local a granel) y en el modo de deformación (por ejemplo, axial vs cizallamiento), lo que produce información diferente, lo que requiere una interpretación cuidadosa 3,8,9,10. La mecánica de los biomateriales blandos se expresa comúnmente en términos de rigidez. Sin embargo, la rigidez depende tanto de las propiedades del material como de la geometría, mientras que los módulos elásticos son propiedades fundamentales de un material y son independientes de la geometría del material11. Como tal, diferentes módulos elásticos están relacionados con la rigidez de una muestra dada, y cada módulo elástico abarca la resistencia del material a un modo específico de deformación (por ejemplo, axial vs cizallamiento) bajo diferentes condiciones de contorno (por ejemplo, expansión libre vs confinamiento)11,12. Los experimentos de nanoindentación permiten la cuantificación de propiedades mecánicas a través de la E que se asocia con deformación uniaxial (indentación) cuando el biomaterial no está confinado lateralmente10,11,12.
El método más popular para cuantificar E de sistemas biológicos a microescala es AFM13,14,15,16. AFM es una herramienta extremadamente poderosa con resolución de fuerza hasta el nivel de pN y resolución espacial hasta la escala sub-nm. Además, AFM ofrece una flexibilidad extrema en términos de acoplamiento con herramientas ópticas y mecánicas complementarias, ampliando sus capacidades para extraer una gran cantidad de información del biomaterial bajo investigación13. Esas características atractivas, sin embargo, vienen con una barrera de entrada representada por la complejidad de la configuración experimental. AFM requiere una amplia capacitación antes de que los usuarios puedan adquirir datos sólidos, y su uso para la caracterización mecánica diaria de materiales biológicos a menudo no está justificado, especialmente cuando no se requiere su fuerza única y resoluciones espaciales.
Debido a esto, una nueva clase de nanoindentadores ha ganado popularidad recientemente debido a su facilidad de uso, al tiempo que ofrece datos comparables con AFM con resolución de fuerza sub-nN y resolución espacial μm, reflejando las fuerzas ejercidas y percibidas por las células en escalas de longitud relevantes2. En particular, los dispositivos de nanoindentación de la parte superior de la virola basados en la tecnología de detección de fibra óptica17,18 han ganado popularidad entre los investigadores activos en el campo de la mecanobiología y más allá; y se han publicado una gran cantidad de trabajos que informan sobre las propiedades mecánicas de los biomateriales que utilizan estos dispositivos, incluidas las células19,20, los hidrogeles8,21 y los tejidos22,23. A pesar de las capacidades de estos sistemas para sondear las propiedades mecánicas dinámicas locales (es decir, el módulo de almacenamiento y pérdida), los experimentos cuasiestáticos que producen E siguen siendo la opción más popular 8,19,20,21. En resumen, los experimentos de nanoindentación cuasiestática consisten en sangrar la muestra con una velocidad constante hasta un punto de ajuste definido por un desplazamiento máximo, fuerza o profundidad de hendidura, y registrar tanto la fuerza como la posición vertical del voladizo en las llamadas curvas de fuerza-distancia (F-z). Las curvas F-z se convierten en curvas de fuerza-indentación (F-δ) a través de la identificación del punto de contacto (CP), y se ajustan con un modelo mecánico de contacto apropiado (generalmente el modelo de Hertz13) para calcular E.
Si bien el funcionamiento de los nanopenetradores superiores de virola se asemeja a las mediciones de AFM, hay especificidades que vale la pena considerar. En este trabajo, se proporciona una guía paso a paso para adquirir robustamente curvas F-z de células e hidrogeles que imitan tejidos utilizando un nanoindenter superior de virola disponible comercialmente, con el fin de fomentar la estandarización de procedimientos experimentales entre grupos de investigación que utilizan este y otros dispositivos similares. Además, se dan consejos sobre cómo preparar mejor las muestras y células de hidrogel para realizar experimentos de nanoindentación, junto con consejos de solución de problemas a lo largo de la vía experimental.
Además, gran parte de la variabilidad en los resultados de nanoindentación (es decir, E y su distribución) depende del procedimiento específico utilizado para analizar los datos, que no es trivial. Para abordar este problema, se proporcionan instrucciones para el uso de un software de código abierto recientemente desarrollado programado en Python y equipado con una interfaz gráfica de usuario (GUI) fácil de usar para el análisis por lotes de curvas F-z . El software permite una rápida selección de datos, filtrado de datos, cálculo del CP a través de diferentes procedimientos numéricos, el cálculo convencional de E, así como un análisis más avanzado llamado espectros de elasticidad24, lo que permite estimar el módulo de Young a granel de la célula, el módulo de Young de la corteza de actina y el grosor de la corteza de actina. El software se puede descargar libremente desde GitHub y se puede adaptar fácilmente para analizar datos procedentes de otros sistemas agregando un analizador de datos apropiado. Se enfatiza que este protocolo se puede usar para otros dispositivos de nanoindentación superior de virola, y otros dispositivos de nanoindentación en general, siempre que algunos pasos se adapten de acuerdo con las pautas específicas del instrumento. El protocolo se resume esquemáticamente en la figura 1.
Protocolo
1. Preparación de sustratos/células para mediciones de nanoindentación
- Siga los pasos indicados en el Protocolo suplementario para la preparación de hidrogeles/células PAAm para experimentos de nanoindentación. El procedimiento se resume en la figura 2.
NOTA: Los hidrogeles PAAm han sido elegidos ya que son los hidrogeles más comunes utilizados en el campo de la mecanobiología. Sin embargo, el protocolo es igualmente aplicable a cualquier tipo de hidrogel25 (ver Discusión, modificaciones del método).
2. Inicio del dispositivo, elección de la sonda y calibración de la sonda
- Siga los pasos indicados en el Protocolo suplementario para iniciar el dispositivo. Para obtener detalles técnicos sobre el funcionamiento de los nanodentadores superiores de virola de fibra óptica, consulte estas referencias17,18.
- Seleccione la sonda de nanoindentación como se describe a continuación.
NOTA: Todas las sondas disponibles comercialmente, como las utilizadas en este protocolo, están equipadas con una punta esférica (Figura 3A). Por lo tanto, la elección se reduce a dos variables: rigidez del voladizo y radio de la punta (Figura 3B).- Elija la rigidez de un voladizo (k en N/m) que coincida con la rigidez esperada de la muestra para obtener mejores resultados15 (consulte la Figura 3C y Discusión, pasos críticos en el protocolo). Para las celdas, seleccione una sonda con k en el rango 0.01-0.09 N/m. Para hidrogeles, seleccione una sonda con k en el rango de 0.1-0.9 N/m, que produzca resultados óptimos para geles con E esperado entre unos pocos kPa y 100 kPa (ver Resultados representativos).
- Elija el radio de la punta (R en μm) de acuerdo con la resolución espacial deseada del proceso de indentación. Para células pequeñas como las células de riñón embrionario humano 293T (HEK293T) (diámetro promedio de ~ 10-15 μm26) seleccione una esfera con R = 3 μm. Para hidrogeles, seleccione una esfera con R = 10-250 μm para sondear las propiedades mecánicas del biomaterial en una gran área de contacto y evitar heterogeneidades locales.
- Consulte la Figura 3C y las directrices adicionales del fabricante para seleccionar la sonda adecuada.
- Una vez seleccionada la sonda, siga los pasos del Protocolo Suplementario para montarla en el nanopenetrador.
3. Calibración de la sonda
NOTA: Los siguientes pasos son específicos de los dispositivos de nanoindentación superior de virola basados en la tecnología de detección de fibra óptica y se detallan para la versión de software 3.4.1. Para otros dispositivos de nanoindentación, siga los pasos recomendados por el fabricante del dispositivo.
- En la ventana principal del software, haga clic en Inicializar. Aparecerá un menú de calibración. Ingrese los detalles de la sonda (se pueden encontrar en el costado de la caja de la sonda; k en N/m, R en μm y factor de calibración en aire) en las cajas de entrada.
- Prepare el plato de calibración: una placa de Petri de vidrio grueso con un fondo plano (consulte Discusión, pasos críticos en el protocolo). Llene el plato con el mismo medio que el plato de muestra (esto también puede ser aire). Haga coincidir la temperatura del medio con la de la muestra.
- Coloque el plato de calibración debajo de la sonda. Si es necesario, deslice la sonda desde el soporte del brazo del nanoindentador y sosténgala con una mano para dejar espacio para la colocación del plato de calibración. Deslice la sonda hacia atrás en su lugar.
- Realice los dos pasos siguientes para la calibración en líquido. Si realiza la medición en aire, utilice el sustrato de politetrafluoroetileno suministrado para la calibración y vaya al paso 5.
- Prehumedezca la sonda con una gota de etanol al 70% utilizando una pipeta Pasteur con el extremo de la pipeta en contacto ligero con la virola de vidrio, para que la gota se deslice sobre el voladizo y la punta esférica27 (ver Discusión, pasos críticos en el protocolo).
- Deslice manualmente el brazo del nanoindentador hacia abajo hasta que la sonda esté completamente sumergida, pero aún lejos del fondo de la placa de Petri. Si es necesario, agregue más medio al plato de calibración. Espere 5 minutos para que se alcancen las condiciones de equilibrio en el líquido.
- En el menú Inicializar del software, haga clic en Escanear longitud de onda. La pantalla del interferómetro mostrará una barra de progreso y la ventana Live Signal en el software de la computadora mostrará el patrón que se muestra en la Figura S1A, izquierda. Para comprobar si el escaneo óptico se realizó correctamente, navegue hasta el panel Escaneo de longitud de onda en el cuadro del interferómetro. Si tiene éxito, una onda sinusoidal debe ser visible (Figura 1A, derecha). Consulte Discusión (solución de problemas del método) si aparece un error.
- En el menú Inicializar , haga clic en Buscar superficie, que bajará progresivamente la sonda hasta que se alcance un umbral establecido en la flexión del voladizo. La sonda deja de moverse cuando se hace contacto con la placa de Petri de vidrio.
- Compruebe si la sonda está en contacto con la superficie. Mueva la sonda hacia abajo 1 μm usando el botón de flecha y hacia abajo en la ventana principal del software. Observe la señal verde (desviación del voladizo) en la ventana activa del software para detectar cambios en la línea de base con cada paso, cuando el voladizo está en contacto con el sustrato (Figura S1B). Si no hay ningún cambio, el voladizo no está en contacto (consulte el paso siguiente).
- Aumente el valor de umbral en el menú Opciones de la ficha Buscar superficie desde su valor predeterminado de 0,01 en un paso de 0,01 a la vez y repita el paso Buscar superficie hasta que esté en contacto. Alternativamente, baje la sonda para que entre en contacto en pequeños pasos de 1 μm hasta que la línea de base verde comience a desplazarse en cada paso hacia abajo.
NOTA: Para los voladizos más suaves (k = 0,025 Nm-1), aumente el valor de umbral en el menú Opciones en la ficha Buscar superficie a priori de realizar el paso 6. Comience desde un valor umbral de 0.06 o 0.07 y auméntelo hasta 0.1 si es necesario. Esto se debe a que el ruido ambiental probablemente hará que el voladizo se doble por encima del umbral antes del contacto. Para sondas blandas, disminuir la velocidad de aproximación (μm/s) en el mismo menú también mejora el procedimiento. - En el menú Inicializar , haga clic en Calibrar.
- Compruebe la ventana Live Signal del software y asegúrese de que tanto el desplazamiento del piezo como las señales de deflexión del voladizo se muevan hacia arriba al mismo tiempo (Figura S1C).
- Si hay un desajuste en el tiempo, la sonda no está completamente en contacto con el vidrio. Desplácese hacia abajo de la sonda en pasos de 1 μm hasta que cambie la línea de base de la señal en voladizo (consulte el paso 7) y repita el paso 9.
- Si la señal en voladizo no cambia en absoluto durante el paso Calibrar , entonces la sonda está lejos de la superficie. Aumente el umbral de contacto de forma iterativa (consulte el paso 8) hasta que la superficie se encuentre correctamente y repita la calibración desde el principio comenzando con el escaneo de longitud de onda.
- Cuando se complete la calibración, compruebe los factores de calibración antiguos y nuevos en la ventana emergente que se muestra. Si el nuevo factor de calibración está en el rango correcto, haga clic en Usar nuevo factor. Si se produce un error en la calibración y el nuevo factor es NaN o no está en el intervalo esperado, consulte Discusión (solución de problemas del método) para obtener información sobre la resolución.
NOTA: El nuevo factor debe ser ~ n veces menor que el proporcionado en la caja de la sonda si la calibración se realizó en un medio líquido con índice de refracción n (n = 1.33 para agua). Si la calibración se realizó en aire, entonces los factores de calibración nuevos y antiguos deben ser aproximadamente iguales. - Compruebe si el círculo de demodulación se ha calibrado correctamente de la siguiente manera. Vaya a la pestaña Demodulación en el escritorio del interferómetro. Golpee suavemente la mesa óptica o el nanopenetrador para inducir suficiente ruido. Un círculo blanco formado por puntos de datos discretos debe cubrir aproximadamente el círculo rojo (Figura S1D).
- Si el círculo blanco no se superpone con el círculo rojo, o aparece una advertencia en la pantalla del interferómetro, el círculo de demodulación necesita recalibración. Esto se puede hacer de dos maneras, como se describe a continuación.
- Toque continuamente el cuerpo del nanoindentador para inducir un círculo completo de ruido y presione el botón Calibrar en el interferómetro.
- Entra en contacto con el sustrato de vidrio y pulsa Calibrar desde el menú Inicializar de la ventana principal del software. No guarde el factor de calibración. En este punto, verifique nuevamente y asegúrese de que el círculo blanco se superponga con el círculo rojo.
NOTA: Si la señal no solo se desplaza ligeramente del círculo de demodulación, sino que se vuelve muy pequeña o no es visible en absoluto, significa que el voladizo está pegado a la fibra óptica. Siga los consejos de solución de problemas para este problema (consulte Discusión, solución de problemas del método) y repita los pasos 13.1 o 13.2. Una vez que el voladizo vuelve a su posición horizontal (Figura 3A), la señal se recuperará al círculo de demodulación.
- Verifique la calibración realizando una hendidura en el sustrato de vidrio directamente después de la calibración como se describe a continuación.
- Cargue o cree un archivo de experimento haciendo clic en Configurar experimento y agregue un paso Buscar superficie y un paso de sangría . Para el paso de sangría, utilice la configuración predeterminada del modo de desplazamiento y cambie el desplazamiento máximo a la distancia de calibración (3.000 nm) para desplazar la sonda contra el sustrato rígido.
- Haga clic en Ejecutar experimento y compruebe el círculo de demodulación en la ventana del interferómetro. Compruebe la señal blanca y asegúrese de que esté en la parte superior del círculo rojo durante la sangría.
- Verifique los resultados en la ventana principal del software en el gráfico de datos de tiempo y asegúrese de que el desplazamiento del piezo (línea azul) sea igual a la deflexión del voladizo (línea verde) ya que la hendidura comienza en contacto y no se espera ninguna deformación del material. Si las señales no son paralelas, consulte Discusión (solución de problemas del método).
- Cambie la ruta local en el menú de calibración estableciendo la ruta de almacenamiento de calibración en un directorio apropiado.
- Cuando la sonda se haya calibrado correctamente, mueva el piezo hacia arriba en 500 μm.
4. Medición del módulo de materiales blandos de Young
- Nanoindentación de hidrogeles
- Cargue la placa de Petri que contiene la(s) muestra(s) en la etapa del microscopio y mueva manualmente la sonda del nanopenetrador a la posición x-y deseada sobre la muestra.
- Deslice manualmente la sonda en solución, teniendo cuidado de dejar 1-2 mm entre la sonda y la superficie de la muestra en esta etapa. Espere 5 minutos para que la sonda se equilibre en el medio.
- Enfoque el plano z del microscopio óptico para que la sonda sea claramente visible.
- Realice una sola sangría para ajustar los parámetros experimentales como se describe a continuación.
- Configure un nuevo experimento en la ventana principal del software. Haga clic en Configurar experimento, que abrirá una nueva ventana. Agregue un paso Buscar superficie . Todos los parámetros del paso Buscar superficie se pueden cambiar en el menú Opciones del software si es necesario.
NOTA: La superficie de búsqueda bajará la sonda hasta que se encuentre la superficie y, a continuación, retraerá la sonda a una distancia definida por Z sobre la superficie (μm), por encima de la superficie de la muestra. Si el voladizo seleccionado es demasiado rígido para la muestra o la muestra está pegajosa, después del paso es probable que la sonda siga en contacto con la muestra, lo que dará lugar a una curva sin una línea de base (Figura 4C). Para resolver este problema, aumente la Z sobre la superficie (μm). - Agregue un paso de sangría . Seleccione la pestaña Perfil y haga clic en Control de desplazamiento. Deje el perfil de sangría predeterminado.
- Haga clic en Ejecutar experimento en la ventana principal del software. Esto encontrará la superficie y realizará una sola hendidura. Si la sangría única no tiene el aspecto esperado, ajuste los parámetros experimentales como se describe en la Figura 4 y Discusión (solución de problemas del método).
- Configure un nuevo experimento en la ventana principal del software. Haga clic en Configurar experimento, que abrirá una nueva ventana. Agregue un paso Buscar superficie . Todos los parámetros del paso Buscar superficie se pueden cambiar en el menú Opciones del software si es necesario.
- Una vez que la sangría se vea como se desea, configure el escaneo de matriz para que se sangra un área suficiente de la muestra. Haga clic en Configurar experimento, agregue un paso Buscar superficie con los parámetros experimentales previamente determinados y agregue un paso de escaneo de matriz .
- Para hidrogeles planos, configure una exploración matricial que contenga 50-100 puntos (es decir, 5 x 10 o 10 x 10 en x e y) espaciados a 10-100 μm (es decir, dx = dy = 10-100 μm). Haga clic en Usar posición de etapa para iniciar el escaneo de matriz desde la posición de etapa actual. Asegúrese de que la casilla Buscar superficie automática esté marcada para buscar la superficie en cada sangría utilizando los parámetros experimentales establecidos.
- Para evitar el muestreo excesivo, establezca el tamaño del paso en al menos el doble del radio de contacto (
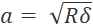 , donde δ es la profundidad de sangría).
, donde δ es la profundidad de sangría). - Configure el perfil de escaneo de matriz en el control de desplazamiento. Asegúrese de que el perfil no viola los supuestos del modelo de Hertz (consulte Discusión, pasos críticos en el protocolo).
- Deje el número de segmentos en 5, que es el valor predeterminado, y utilice el perfil de desplazamiento predeterminado. Si es necesario, cambie el perfil de desplazamiento en términos de desplazamiento máximo y tiempo para cada segmento inclinado, lo que afectará la profundidad máxima de hendidura y la velocidad de deformación, respectivamente. No exceda las tasas de deformación > 10 μm/s (ver Discusión, limitaciones del método).
- Introduzca un valor para la velocidad de aproximación, que determina la rapidez con la que se desplaza la sonda hacia la muestra antes del contacto. Haga coincidir la velocidad de retracción con la velocidad de aproximación (consulte la nota a continuación).
NOTA: Para voladizos blandos y entornos ruidosos, se recomienda una velocidad de aproximación de 1.000-2.000 nm/s. Para voladizos más rígidos y entornos controlados, esto se puede aumentar. - Guarde el experimento configurado en la ruta de experimento deseada y seleccione un directorio donde se guardarán los datos en la ruta de guardado, en la ficha General de la ventana Configurar experimento. Haga clic en Ejecutar experimento.
- Para evitar el muestreo excesivo, establezca el tamaño del paso en al menos el doble del radio de contacto (
- Una vez que se complete el escaneo de la matriz, eleve la sonda en 200-500 μm y mueva la sonda a un área diferente de la muestra lo suficientemente lejos de la primera área.
- Repita el experimento al menos dos veces para que se adquieran suficientes datos sobre cada muestra (es decir, al menos dos escaneos matriciales por muestra, que contengan 50-100 curvas cada uno).
- Nanoindentación de células
- Cargue la muestra en el microscopio como se describió anteriormente.
- Para la hendidura de una sola celda, enfoque el plano z de modo que tanto las celdas como la sonda sean visibles con un aumento de 20x o 40x, dependiendo del tamaño y la propagación de la celda.
- Mueva la sonda por encima de la celda que se va a sangrar.
- Configure un nuevo experimento en la ventana principal del software. Haga clic en Configurar experimento, que abrirá una nueva ventana. Agregue un paso Buscar superficie y sangría con parámetros predeterminados en el modo de desplazamiento.
- Haga clic en Ejecutar experimento, que encontrará la superficie y realizará una sola sangría. Compruebe si la sangría se ha realizado correctamente. Si la curva no tiene el aspecto esperado, ajuste los parámetros experimentales (consulte la Figura 4 y Discusión, solución de problemas del método).
- Si la sangría se realizó correctamente, agregue un escaneo de matriz al experimento. Siga los pasos dados para los experimentos de nanoindentación de hidrogeles; configurar el escaneo de matriz para que el tamaño del paso permita sangrar un área pequeña de la celda; 25 puntos espaciados a 0,5-5 μm para las células HEK293T.
- Dependiendo del tamaño de la celda, adapte el escaneo de la matriz para asegurarse de que la punta no se incline fuera del límite de la celda, es decir, haciendo una geometría de mapa diferente o sondeando menos puntos.
- Haga clic en Ejecutar experimento y espere a que se complete.
- Una vez completado el escaneo de la matriz, levante la sonda fuera de contacto (50 μm en el plano z ).
- Mueva la sonda por encima de una nueva celda y repita el proceso (consulte Discusión, pasos críticos en el protocolo).
- Limpieza de la sonda y apagado del instrumento
- Siga los pasos indicados en el Protocolo suplementario para limpiar la sonda y apagar el dispositivo de nanoindentación.
5. Análisis de datos
- Descarga e instalación del software
- Siga los pasos indicados en el Protocolo Suplementario para descargar e instalar el software para el análisis de datos28,29.
- Proyección de curvas F-z y producción de conjuntos de datos limpios en formato JSON
- Inicie prepare.py desde la línea de comandos en el equipo laboratorio como se describe en los pasos 2 a 3.
- Si usa una computadora con Windows, mantenga presionada la tecla Mayús mientras hace clic derecho en la carpeta NanoPrepare y haga clic en Abrir ventana de PowerShell aquí. Escriba el comando python prepare.py y presione la tecla Enter . Aparecerá una GUI en su pantalla (Figura S2).
- Si usa una computadora MacOS, haga clic derecho en la carpeta NanoPrepare y haga clic en Nuevo terminal en la carpeta. Escriba el comando python3 prepare.py y presione la tecla Intro , que iniciará la GUI (Figura S2).
- Seleccione el formato de datos O11NEW en la lista desplegable. Si los datos no se cargan correctamente, vuelva a iniciar la GUI y seleccione O11OLD.
NOTA: El formato O11NEW funciona para datos obtenidos utilizando dispositivos de nanoindentación de detección de fibra óptica superior con virola con la versión de software 3.4.1. Este formato también funcionará para versiones de software anteriores, al menos las pertenecientes a nanoindentadores instalados en 2019-2020. - Haga clic en Cargar carpeta. Seleccione una carpeta que contenga los datos que se van a analizar: escaneo de matriz única o escaneos de matriz múltiple. El gráfico superior (curvas sin procesar) se rellenará con el conjunto de datos cargado. Para visualizar una curva específica, haga clic en ella. Esto lo resaltará en verde y lo mostrará en el gráfico inferior (Curva actual).
- Limpie el conjunto de datos utilizando las pestañas presentes en la parte derecha de la GUI como se describe a continuación.
- Utilice el botón Segmento para seleccionar el segmento correcto a analizar, que es el segmento hacia adelante de las curvas F-z . El número específico depende del número de segmentos seleccionados en el software de nanoindentación al realizar experimentos.
- Utilice el botón Recortar 50 nm para recortar las curvas en 50 nm en el extremo izquierdo (si L está marcado), derecha (si R está marcado) o ambos lados (si tanto R como L están marcados). Haga clic en este botón varias veces para recortar tanto como sea necesario. Utilice esta opción para eliminar los artefactos presentes al principio/al final de las curvas F-z.
- Inspeccione la pestaña Voladizo para la constante de resorte, la geometría de la punta y el radio de la punta. Inspeccione la ficha para asegurarse de que los metadatos se han leído correctamente.
- Utilice la ficha Filtrado para establecer un umbral de fuerza que descartará todas las curvas que no alcanzaron la fuerza dada. Las curvas descartadas se resaltarán en rojo.
- Utilice el botón de alternancia manual para eliminar manualmente las curvas que no se han adquirido correctamente. Elimine cualquier curva haciendo clic en la curva específica y seleccionando OUT, que resaltará la curva en rojo.
- Haga clic en Save JSON. Escriba un nombre adecuado para el conjunto de datos limpiado, que es un único archivo JSON. Envíe el archivo JSON a la computadora donde se instaló el software NanoAnalysis.
6. Análisis formal de datos
- Inicie el archivo nano.py desde la línea de comandos navegando a la carpeta NanoAnalysis e iniciando un terminal como se explicó anteriormente. Escriba el comando python nano.py o python3 nano.py (dependiendo del sistema operativo) y presione la tecla Enter . Aparecerá una GUI en su pantalla (Figura S3).
- En la parte superior izquierda de la GUI, haga clic en Cargar experimento y seleccione el archivo JSON. Esto rellenará la lista de archivos y el gráfico Curvas sin procesar que muestra el conjunto de datos en términos de curvas F-z . Los ejes F y z se muestran en relación con las coordenadas CP, que se calculan en segundo plano al cargar el conjunto de datos (consulte la nota siguiente). En el cuadro Estadísticas , compruebe los valores de los tres parámetros: Nactivado, N fallido y Nexcluido.
NOTA: Nactivated representa el número de curvas que se analizarán en el análisis posterior de espectros de Hertz/elasticidad y aparecerán en negro en el gráfico de curvas sin procesar . Nfailed representa el número de curvas en las que no se pudo encontrar un CP confiable y aparecen en azul en el gráfico. Estas curvas se descartarán automáticamente en el análisis posterior. Al abrir el software, algunas curvas pueden moverse automáticamente al conjunto fallido. Esto se debe a que el CP se calcula al abrir el software con el algoritmo de umbral predeterminado (ver más abajo). N excluido representa las curvas que se seleccionan manualmente para serexcluidas del análisis y aparecerán en rojo en el gráfico (ver más abajo). - Compruebe si el número de curvas fallidas, excluidas y activadas es razonable. Consulte el gráfico Curvas sin procesar para visualizar las curvas.
- Para visualizar una curva específica con más detalle, haga clic en ella. Esto lo resaltará en verde y lo mostrará en el gráfico Curva actual . Una vez que se ha seleccionado una sola curva, los parámetros R y k (que deben ser los mismos para todas las curvas) se rellenarán en el cuadro Estadísticas de la GUI.
- Cambie el estado de una curva determinada mediante el cuadro de alternancia . Haga clic en la curva específica cuyo estado desea cambiar y, a continuación, haga clic en Activado, Error o Excluido. El recuento en el cuadro Estadísticas se actualiza automáticamente.
NOTA: Para cambiar la vista del conjunto de datos en el gráfico Curvas sin procesar, utilice el cuadro Ver . Haga clic en Todo para mostrar todas las curvas (es decir, activadas, fallidas y excluidas en los colores respectivos). Haga clic en Error para mostrar las curvas activadas y fallidas y haga clic en Activado para mostrar solo las curvas activadas. Para restablecer el estado de todas las curvas entre activadas y excluidas, haga clic en Activado o Excluido en el cuadro Restablecer . - Una vez que el conjunto de datos se haya limpiado aún más, siga la canalización de análisis de datos que se describe a continuación.
- Filtre cualquier ruido presente en las curvas utilizando los filtros implementados en la GUI (Filtering Box), a saber, un filtro personalizado llamado filtro Prominency, el filtro Savitzky Golay30,31 (SAVGOL) y un filtro de suavizado basado en el cálculo de la mediana de los datos en una ventana determinada (filtro mediano). Consulte Discusión (pasos críticos en el protocolo) para obtener detalles sobre los filtros.
- Inspeccione las curvas filtradas en el gráfico Curva actual . La curva filtrada se muestra en negro, mientras que la versión no filtrada de la curva se muestra en verde.
NOTA: Se recomienda filtrar los datos lo menos posible para preservar las características de la señal original. El filtrado excesivo puede suavizar cualquier diferencia presente en los datos. Trabajar con el filtro de prominencia activado es suficiente para el análisis de Hertz de los datos de nanoindentación. Si los datos son particularmente ruidosos, entonces se puede aplicar adicionalmente un filtro SAVGOL o mediano. - Seleccione un algoritmo para encontrar el CP. En el cuadro Punto de contacto, elija uno de una serie de procedimientos numéricos que se han implementado en el software, a saber, la bondad de ajuste (GoF)32, la relación de varianzas (RoV)32, la segunda derivada 33 o el umbral 33. Consulte Discusión, pasos críticos en el protocolo para obtener detalles sobre los algoritmos.
NOTA: El CP es el punto en el que la sonda entra en contacto con el material y debe identificarse para convertir los datos F-z en datos F-δ (para materiales blandos, δ es finito y debe calcularse). El algoritmo seleccionado se aplicará a todas las curvas activas del conjunto de datos, y las curvas en las que el algoritmo no localice el CP de forma robusta se moverán al conjunto fallido. - Ajuste los parámetros del algoritmo para que se adapten a su conjunto de datos para que el CP se ubique correctamente como se detalla en la Discusión, pasos críticos en el protocolo. Para ver dónde se ha encontrado el CP en una sola curva, seleccione la curva haciendo clic en ella y haga clic en Inspeccionar. Compruebe la ventana emergente que aparece para identificar dónde se ha ubicado el CP.
- Compruebe si la línea roja que aparece, que es el parámetro que el algoritmo calculó en la región de interés seleccionada, tiene un valor máximo o mínimo que corresponde a la ubicación del CP (por ejemplo, para el GoF, el parámetro es el R2). Repita este proceso para todas las curvas si es necesario.
NOTA: Los ejes de la ventana emergente están en coordenadas absolutas para que se pueda mostrar la ubicación del CP. Por el contrario, los ejes del gráfico Curvas sin procesar y Curva actual se muestran en relación con el CP, es decir, la ubicación del CP es (0,0). - Haga clic en Análisis de hercios. Esto generará tres gráficos que se describen a continuación.
- Compruebe las curvas F-δ individuales en el conjunto de datos junto con el ajuste promedio de Hertz (línea discontinua roja). Ajuste la sangría en nm hasta la que se ajusta el modelo de Hertz en el cuadro Resultados en Sangría máxima (nm). Establézcalo en un máximo de ~ 10% de R para que el modelo de Hertz sea válido (consulte Discusión, pasos críticos en el protocolo).
- Compruebe la curva F-δ media con una banda de error que muestre una desviación estándar (DE) junto con el ajuste medio de Hertz (línea discontinua roja). Visualice el ajuste de Hertz promedio en el gráfico Curvas sin procesar como referencia y el ajuste de Hertz para cada curva en la curva actual.
- Compruebe que el diagrama de dispersión de E se origina al ajustar el modelo de Hertz a cada curva individual.
- Haga clic en el nombre del archivo, la curva F-z , la curva F-δ o en un punto del gráfico de dispersión para resaltar la curva en cada gráfico. Si un punto de datos en el diagrama de dispersión parece estar fuera de la distribución de los datos, haga clic en él e inspeccione la curva a la que pertenece. Verifique que el CP se haya localizado correctamente haciendo clic en el botón Inspeccionar . Excluya la curva del análisis si es necesario.
- Inspeccione el cuadro Resultados para la media calculada E y su SD (Eγ ± σ) y asegúrese de que sean razonables para el experimento dado.
- En el cuadro Guardar , haga clic en Hertz. En la ventana emergente, introduzca el nombre del archivo y el directorio. Una vez hecho esto, haga clic en Guardar. Se creará un archivo .tsv. Abra el archivo .tsv en cualquier software adicional de preferencia y utilice los valores para el análisis estadístico y el trazado posterior.
NOTA: El archivo contiene la E obtenida de cada curva y la media E y su DE. Además, el archivo contiene metadatos asociados con el análisis, incluido el número de curvas analizadas, R, k y la sangría máxima utilizada para el modelo de Hertz. - Este paso es opcional. Haga clic en Promedio F-Ind para exportar la fuerza promedio y la sangría promedio, junto con una SD en la fuerza.
- Para obtener datos de nanoindentación celular, haga clic en Análisis de espectros de elasticidad (consulte Resultados representativos y discusión). Inspeccionar las dos gráficas producidas, a saber, E en función de la profundidad de indentación (E(δ)) para cada curva, y la media E(δ) con banda de error que muestra una SD (línea roja sólida y área sombreada) ajustada por un modelo (línea discontinua negra), que permite estimar el módulo de Young de la corteza de actina de la célula, el módulo de Young a granel de la célula, y el grosor de la corteza de actina. Además, verifique el promedio de E(δ) en el gráfico superior en rojo.
- Asegúrese de que la casilla Interpolar esté marcada, lo que garantiza que la derivada necesaria para realizar el análisis de espectros de elasticidad se calcula en la señal interpolada (consulte Resultados representativos).
- Inspeccione el cuadro Resultados, informando el módulo de Young de la corteza (E 0 ± σ), el módulo de Young de la célula (Eb ± σ) y el grosor de la corteza (d 0 ± σ).
NOTA: Los espectros de elasticidad promedio pueden parecer ruidosos al principio, con oscilaciones sinusoidales prominentes. Como resultado, la ecuación (3) puede no ajustarse correctamente. Si este es el caso, aumentar iterativamente la longitud de la ventana del filtro SAVGOL34 de suavizado resuelve este problema. - Una vez finalizado el análisis, haga clic en ES en el cuadro Guardar . Esto exportará un archivo .tsv en el directorio especificado, que contiene la elasticidad promedio en función de la profundidad de sangría promedio y el radio de contacto, los metadatos asociados con el experimento (ver arriba) y los parámetros del modelo estimados explicados anteriormente. Finalmente, también se informa la elasticidad promedio sin tener en cuenta la dependencia de δ y su DE.
- Cierre el software e ingrese los resultados guardados en cualquier otro software de preferencia para trazar aún más los datos y realizar análisis estadísticos.
- Este paso es opcional: exporte gráficos desde la GUI haciendo clic derecho en el gráfico y seleccionando Exportar. Exporte el gráfico en .svg, de modo que parámetros como fuente, tamaño de fuente, estilo de línea, etc. se puede editar en otro software de su elección.
NOTA: Los algoritmos y filtros CP personalizados se pueden programar y agregar a los ya existentes. Véase la Nota complementaria 1 para más detalles.
Resultados
Siguiendo el protocolo, se obtiene un conjunto de curvas F-z . Lo más probable es que el conjunto de datos contenga curvas buenas y curvas que se descartarán antes de continuar con el análisis. En general, las curvas deben descartarse si su forma es diferente de la que se muestra en la Figura 4A. La Figura 5AI muestra un conjunto de datos de ~100 curvas obtenidas en un hidrogel PAAm blando de E 0.8KPa 35 esperado carg...
Discusión
Este protocolo muestra cómo adquirir de forma robusta datos de nanoindentación de espectroscopía de fuerza utilizando un nanoindentador superior de virola disponible comercialmente tanto en hidrogeles como en células individuales. Además, se proporcionan instrucciones para el uso de un software de código abierto programado en Python que comprende un flujo de trabajo preciso para el análisis de datos de nanoindentación.
Pasos críticos en el protocolo
Se ha determina...
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
GC y MAGO reconocen a todos los miembros del CeMi. MSS reconoce el apoyo a través de una subvención del programa EPSRC (EP/P001114/1).
GC: software (contribución al desarrollo de software y algoritmos), análisis formal (análisis de datos de nanoindentación), validación, investigación (experimentos de nanoindentación en geles de poliacrilamida), curación de datos, redacción (borrador original, revisión y edición), visualización (figuras y gráficos). MAGO: investigación (preparación de geles y muestras de células, experimentos de nanoindentación en células), redacción (borrador original, revisión y edición), visualización (figuras y gráficos). NA: validación, redacción (revisión y edición). IL: software (contribución al desarrollo de software y algoritmos), validación, escritura (revisión y edición); MV: conceptualización, software (diseño y desarrollo de software original y algoritmos), validación, recursos, redacción (borrador original, revisión y edición), supervisión, administración de proyectos, adquisición de fondos MSS: recursos, redacción (revisión y edición), supervisión, administración de proyectos, adquisición de fondos. Todos los autores leyeron y aprobaron el manuscrito final.
Materiales
| Name | Company | Catalog Number | Comments |
| 12 mm coverslips | VWR | 631-1577P | |
| 35 mm cell treated culture dishes | Greiner CELLSTAR | 627160 | |
| Acrylamide | Sigma-Aldrich | A4058 | |
| Acrylsilane | Alfa Aesar | L16400 | |
| Ammonium Persulfate | Merk | 7727-54-0 | |
| Bisacrylamide | Merk | 110-26-9 | |
| Chiaro nanoindenter | Optics 11 Life | no catologue number | |
| Ethanol | general | ||
| Fetal bovine serum | Gibco | 16140071 | |
| High glucose DMEM | Gibco | 11995065 | |
| Isopropanol | general | ||
| Kimwipe | Kimberly Clark | 21905-026 | |
| Microscope glass slides | VWR | 631-1550P | |
| MilliQ system | Merk Millipore | ZR0Q008WW | |
| OP1550 Interferometer | Optics11 Life | no catalogue number | |
| Optics 11 Life probe (k = 0.02-0.005 N/m, R = 3-3.5 um) | Optics 11 Life | no catologue number | |
| Optics 11 Life probe (k = 0.46-0.5 N/m, R = 50-55 um) | Optics 11 Life | no catologue number | |
| Penicillin/Streptomycin | Gibco | 15140122 | |
| RainX rain repellent | RainX | 26012 | |
| Standard petri dishes (90 mm) | Thermo Scientific | 101RTIRR | |
| Tetramethylethylenediamine | Sigma-Aldrich | 110-18-9 | |
| Vaccum dessicator | Thermo Scientific | 531-0250 | |
| Software | |||
| Data acquisition software (v 3.4.1) | Optics 11 Life | ||
| GitHub Desktop (Optional) | Microsoft | ||
| Python 3 | Python Software Foundation | ||
| Visual Studio Code (Optional) | Microsoft |
Referencias
- Discher, D. E., Janmey, P. Y. W. Tissue cells feel and respond to the stiffness of their substrate. Science. 310 (5751), 1139-1143 (2005).
- Roca-Cusachs, P., Conte, V., Trepat, X. Quantifying forces in cell biology. Nature Cell Biology. 19 (7), 742-751 (2017).
- Guimarães, C. F., Gasperini, L., Marques, A. P., Reis, R. L. The stiffness of living tissues and its implications for tissue engineering. Nature. Reviews. Materials. 5, 351-370 (2020).
- Moeendarbary, E., Harris, A. R. Cell mechanics: Principles, practices, and prospects. Wiley Interdisciplinary. Reviews. Systems. Biology and Medicine. 6 (5), 371-388 (2014).
- Butcher, D. T., Alliston, T., Weaver, V. M. A tense situation: Forcing tumour progression. Nature Reviews Cancer. 9 (2), 108-122 (2009).
- Kubánková, M., et al. Physical phenotype of blood cells is altered in COVID-19. Biophysical Journal. 120 (14), 2838-2847 (2021).
- Engler, A. J., Sen, S., Sweeney, H. L., Discher, D. E. Matrix elasticity directs stem cell lineage specification. Cell. 126, 677-689 (2006).
- Ciccone, G., et al. What caging force cells feel in 3D hydrogels: A rheological perspective. Advanced Healthcare Materials. 9 (17), 2000517 (2020).
- Wu, P. H., et al. A comparison of methods to assess cell mechanical properties. Nature Methods. 15 (7), 491-498 (2018).
- McKee, C. T., Last, J. A., Russell, P., Murphy, C. J. Indentation versus tensile measurements of young's modulus for soft biological tissues. Tissue Engineering B Reviews. 17 (3), 155-164 (2011).
- Humphrey, J. D., Delange, S. L. . An Introduction to Biomechanics Solids and Fluids, Analysis and Design. , 271-371 (2004).
- Prevedel, R., Diz-Muñoz, A., Ruocco, G., Antonacci, G. Brillouin microscopy: an emerging tool for mechanobiology. Nature Methods. 16 (10), 969-977 (2019).
- Krieg, M., et al. Atomic force microscopy-based mechanobiology. Nature Reviews Physics. 1, 41-57 (2019).
- Norman, M. D. A., Ferreira, S. A., Jowett, G. M., Bozec, L., Gentleman, E. Measuring the elastic modulus of soft culture surfaces and three-dimensional hydrogels using atomic force microscopy. Nature Protocols. 16 (5), 2418-2449 (2021).
- Gavara, N. A beginner's guide to atomic force microscopy probing for cell mechanics. Microscopy Research and Technique. 80 (1), 75-84 (2017).
- Whitehead, A. J., Kirkland, N. J., Engler, A. J. Atomic force microscopy for live-cell and hydrogel measurement. Methods in Molecular Biology. 2299, 217-226 (2021).
- Chavan, D., et al. Ferrule-top nanoindenter: An optomechanical fiber sensor for nanoindentation. The Review of Scientific Instruments. 83 (11), 115110 (2012).
- Van Hoorn, H., Kurniawan, N. A., Koenderink Ac, G. H., Iannuzzi, D. Local dynamic mechanical analysis for heterogeneous soft matter using ferrule-top indentation. Soft Matter. 12 (12), 3066-3073 (2016).
- Baldini, F., et al. Biomechanics of cultured hepatic cells during different steatogenic hits. Journal of the Mechanical Behavior of Biomedical Materials. 97, 296-305 (2019).
- Emig, R., et al. Piezo1 channels contribute to the regulation of human atrial fibroblast mechanical properties and matrix stiffness sensing. Cells. 10 (3), 663 (2021).
- Dobre, O., et al. A hydrogel platform that incorporates laminin isoforms for efficient presentation of growth factors - Neural growth and osteogenesis. Advanced Functional Materials. 31 (21), 2010225 (2021).
- Antonovaite, N., Beekmans, S. V., Hol, E. M., Wadman, W. J., Iannuzzi, D. Regional variations in stiffness in live mouse brain tissue determined by depth-controlled indentation mapping. Scientific Reports. 8 (1), 12517 (2018).
- Wu, G., Gotthardt, M., Gollasch, M. Assessment of nanoindentation in stiffness measurement of soft biomaterials: kidney, liver, spleen and uterus. Scientific Reports. 10 (1), 18784 (2020).
- Lüchtefeld, I., et al. Elasticity spectra as a tool to investigate actin cortex mechanics. Journal of Nanobiotechnology. 18 (1), 147 (2020).
- Caliari, S. R., Burdick, J. A. A practical guide to hydrogels for cell culture. Nature Methods. 13 (5), 405-414 (2016).
- Blumlein, A., Williams, N., McManus, J. J. The mechanical properties of individual cell spheroids. Scientific Reports. 7 (1), 7346 (2017).
- Mirsandi, H., et al. Influence of wetting conditions on bubble formation from a submerged orifice. Experiments in Fluids. 61, 83 (2020).
- Vassalli, M., Ciccone, G. . CellMechLab/NanoPrepare: v0.1.1. Zendo. , (2021).
- Vassalli, M., Ciccone, G., Lüchtefeld, I. CellMechLab/nanoindentation: v1.0.0. Zendo. , (2021).
- Savitzky, A., Golay, M. J. E. Smoothing and differentiation of data by simplified least squares procedures. Analytical Chemistry. 36 (8), 1627-1639 (1964).
- Schafer, R. W. What is a savitzky-golay filter. IEEE Signal Processing Magazine. 28 (4), 111-117 (2011).
- Gavara, N. Combined strategies for optimal detection of the contact point in AFM force-indentation curves obtained on thin samples and adherent cells. Scientific Reports. 6, 21267 (2016).
- Lin, D. C., Dimitriadis, E. K., Horkay, F. Robust strategies for automated AFM force curve analysis-I. Non-adhesive indentation of soft, inhomogeneous materials. Journal of Biomechanical Engineering. 129 (3), 430-440 (2007).
- Virtanen, P., et al. SciPy 1.0: fundamental algorithms for scientific computing in Python. Nature Methods. 17 (3), 261-272 (2020).
- Tse, J. R., Engler, A. J. Preparation of hydrogel substrates with tunable mechanical properties. Current Protocols in Cell Biology. , (2010).
- Pharr, G. M., Oliver, W. C., Brotzen, F. R. On the generality of the relationship among contact stiffness, contact area, and elastic modulus during indentation. Journal of Materials Research. 7 (3), 613-617 (1992).
- Kumar, R., Saha, S., Sinha, B. Cell spread area and traction forces determine myosin-II-based cortex thickness regulation. Biochimica et Biophysica Acta - Molecular Cell Research. 1866 (12), 118516 (2019).
- Kunda, P., Pelling, A. E., Liu, T., Baum, B. Moesin controls cortical rigidity, cell rounding, and spindle morphogenesis during mitosis. Current Biology: CB. 18 (2), 91-101 (2008).
- Allen, M., Poggiali, D., Whitaker, K., Marshall, T. R., Kievit, R. A. Raincloud plots: a multi-platform tool for robust data visualization. Wellcome Open Research. 4, 63 (2019).
- Clark, A. G., Paluch, E. Mechanics and regulation of cell shape during the cell cycle. Results and Problems in Cell Differentiation. 53, 31-73 (2011).
- Langan, T. J., Rodgers, K. R., Chou, R. C. Synchronization of mammalian cell cultures by serum deprivation. Methods in Molecular Biology. 1524, 97-105 (2017).
- Hodgkinson, T., et al. The use of nanovibration to discover specific and potent bioactive metabolites that stimulate osteogenic differentiation in mesenchymal stem cells. Science Advances. 7 (9), 7921 (2021).
- Kloxin, A. M., Kloxin, C. J., Bowman, C. N., Anseth, K. S. Mechanical properties of cellularly responsive hydrogels and their experimental determination. Advanced Materials (Deerfield Beach, Fla). 22 (31), 3484-3494 (2010).
- Loessner, D., et al. Functionalization, preparation and use of cell-laden gelatin methacryloyl-based hydrogels as modular tissue culture platforms. Nature Protocols. 11 (4), 727-746 (2016).
- Yue, K., et al. Synthesis, properties, and biomedical applications of gelatin methacryloyl (GelMA) hydrogels. Biomaterials. 73, 254-271 (2015).
- Sarrigiannidis, S. O., et al. A tough act to follow: collagen hydrogel modifications to improve mechanical and growth factor loading capabilities. Materials Today. Bio. 10, 100098 (2021).
- Karoutas, A., et al. The NSL complex maintains nuclear architecture stability via lamin A/C acetylation. Nature Cell Biology. 21 (10), 1248-1260 (2019).
- Ryu, H., et al. Transparent, compliant 3D mesostructures for precise evaluation of mechanical characteristics of organoids. Advanced Materials (Deerfield Beach, Fla). 33 (25), 2100026 (2021).
- Carvalho, D. T. O., Feijão, T., Neves, M. I., Da Silva, R. M. P., Barrias, C. C. Directed self-assembly of spheroids into modular vascular beds for engineering large tissue constructs Biofabrication Directed self-assembly of spheroids into modular vascular beds for engineering large tissue constructs. Biofabrication. 13 (3), 035008 (2021).
- Chaudhuri, O., Cooper-White, J., Janmey, P. A., Mooney, D. J., Shenoy, V. B. Effects of extracellular matrix viscoelasticity on cellular behaviour. Nature. 584 (7822), 535-546 (2020).
- Cantini, M., Donnelly, H., Dalby, M. J., Salmeron-Sanchez, M. The plot thickens: The emerging role of matrix viscosity in cell mechanotransduction. Advanced Healthcare Materials. 9 (8), 1901259 (2020).
- Elosegui-Artola, A. The extracellular matrix viscoelasticity as a regulator of cell and tissue dynamics. Current Opinion in Cell Biology. 72, 10-18 (2021).
- Chaudhuri, O. Viscoelastic hydrogels for 3D cell culture. Biomaterials Science. 5 (8), 1480-1490 (2017).
- Nguyen, T. D., Gu, Y. Determination of strain-rate-dependent mechanical behavior of living and fixed osteocytes and chondrocytes using atomic force microscopy and inverse finite element analysis. Journal of Biomechanical Engineering. 136 (10), 101004 (2014).
- Mokbel, M., Hosseini, K., Aland, S., Fischer-Friedrich, E. The Poisson Ratio of the Cellular Actin Cortex Is Frequency Dependent. Biophysical Journal. 118 (8), 1968-1976 (2020).
- Javanmardi, Y., Colin-York, H., Szita, N., Fritzsche, M., Moeendarbary, E. Quantifying cell-generated forces: Poisson's ratio matters. Communications Physics. 4, 237 (2021).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados