Uso del pH-metro
Panoramica
Fonte: Laboratorio del Dr. Zhongqi He - Dipartimento dell'Agricoltura degli Stati Uniti
Acidi e basi sono sostanze in grado di donare protoni (H+) e ioni idrossido (OH-), rispettivamente. Sono due estremi che descrivono le sostanze chimiche. Mescolare acidi e basi può annullare o neutralizzare i loro effetti estremi. Una sostanza che non è né acida né basica è neutra. I valori di concentrazione di protoni ([H+]) per la maggior parte delle soluzioni sono scomodamente piccoli e difficili da confrontare in modo che sia stata introdotta una quantità più pratica, il pH. Il pH era originariamente definito come il logaritmo decimale del reciproco della concentrazione molare dei 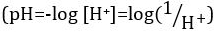 protoni, ma è stato aggiornato al logaritmo decimale del reciproco dell'attività degli ioni
protoni, ma è stato aggiornato al logaritmo decimale del reciproco dell'attività degli ioni 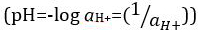 idrogeno. La prima definizione è ora occasionalmente espressa come p[H]. La differenza tra p[H] e pH è piuttosto piccola. È stato affermato che pH = p[H] + 0,04. È pratica comune utilizzare il termine "pH" per entrambi i tipi di misurazioni.
idrogeno. La prima definizione è ora occasionalmente espressa come p[H]. La differenza tra p[H] e pH è piuttosto piccola. È stato affermato che pH = p[H] + 0,04. È pratica comune utilizzare il termine "pH" per entrambi i tipi di misurazioni.
La scala del pH varia tipicamente da 0 a 14. Per una soluzione 1 M di un acido forte, pH=0 e per una soluzione 1 M di una base forte, pH=14. Pertanto, i valori di pH misurati si troveranno per lo più nell'intervallo da 0 a 14, sebbene i valori al di fuori di tale intervallo siano del tutto possibili. L'acqua pura è neutra con pH=7. Un pH inferiore a 7 è acido e un pH superiore a 7 è basico. Poiché la scala del pH è logaritmica, il pH è una quantità adimensionale. Ogni valore di pH intero inferiore a 7 è 10 volte più acido del numero intero successivo. Ad esempio, un pH di 4 è 10 volte più acido di un pH di 5 e 100x (10 x 10) più acido di un pH di 6. Lo stesso vale per i valori di pH superiori a 7, ognuno dei quali è 10 volte più basico (o alcalino) rispetto al successivo valore intero inferiore. Ad esempio, un pH di 10 è 10 volte più semplice di un pH di 9.
Procedura
1. Calibrazione del pH
- Accendere il contatore premendo il pulsante "power".
- Collegare la sonda di compensazione automatica della temperatura (ATC) se è disponibile e/o non è con l'elettrodo.
- Verificare che la modalità di misurazione sia pH. In caso contrario, premere il pulsante "MODE" fino a quando non viene visualizzata la modalità "pH" sul display LCD.
- Consultare la guida di riferimento rapido nella parte inferiore del misuratore o nelle vicinanze per assistenza, se necessario.<
Risultati
La figura 1 mostra il pH dei terreni agricoli influenzati dalla gestione delle colture e dall'irrigazione delle acque sotterranee. Questi campioni di terreno sono stati raccolti da 5 campi di patate sotto diverse pratiche di rotazione delle colture con o senza irrigazione delle acque sotterranee. Il pH più basso si osserva nei terreni del campo 4 sia nelle serie irrigate a pioggia che in quella sotterranea. L'irrigazione delle acque sotterranee ha costantemente aumentato il pH del suolo in tutti e 5 i campi. Le informazioni.
Applicazione e Riepilogo
Il pH è uno dei parametri chimici più comunemente misurati delle soluzioni acquose. È un parametro critico nel trattamento delle acque e delle acque reflue per applicazioni municipali e industriali, produzione chimica, ricerca agricola e produzione. È anche fondamentale nel monitoraggio ambientale, nella ricerca chimica e nelle scienze della vita, nella ricerca biochimica e farmaceutica, nella produzione elettronica e in molte altre applicazioni. La Figura 2 elenca i valori di pH di alcune sostanze c...
Vai a...
Video da questa raccolta:

Now Playing
Uso del pH-metro
General Chemistry
346.6K Visualizzazioni

Vetreria di laboratorio e relativi usi
General Chemistry
657.4K Visualizzazioni

Soluzioni e concentrazioni
General Chemistry
274.7K Visualizzazioni

Determinazione della densità di un solido e di un liquido
General Chemistry
556.5K Visualizzazioni

Determinazione della composizione percentuale di massa in una soluzione acquosa
General Chemistry
383.7K Visualizzazioni

Determinazione della formula empirica (minima)
General Chemistry
183.0K Visualizzazioni

Determinazione delle regole di solubilità di composti ionici
General Chemistry
141.5K Visualizzazioni

Introduzione alla titolazione
General Chemistry
425.1K Visualizzazioni

Legge dei gas perfetti
General Chemistry
78.6K Visualizzazioni

Determinazione spettrofotometrica di una costante di equilibrio
General Chemistry
158.6K Visualizzazioni

Principio di Le Châtelier
General Chemistry
265.7K Visualizzazioni

Depressione del punto di congelamento per l'identificazione di un composto sconosciuto
General Chemistry
160.7K Visualizzazioni

Determinazione dell'equazione cinetica e dell'ordine di reazione
General Chemistry
196.2K Visualizzazioni

Utilizzo della calorimetria a scansione differenziale per misurare cambiamenti nell'entalpia
General Chemistry
44.5K Visualizzazioni

Complessi chimici di coordinazione
General Chemistry
91.6K Visualizzazioni